Ipogonadismo gonadotropo negli uomini. Ipogonadismo negli uomini: sintomi e trattamento. Cause e meccanismi di sviluppo dell'ipogonadismo negli uomini
Pochissime persone pensano all'enorme ruolo che gli ormoni svolgono nel nostro corpo. Il sistema endocrino è secondo per importanza solo al sistema nervoso ed è responsabile del normale funzionamento di tutto il corpo, compresa la procreazione. Nella sua patologia si osservano malattie come il diabete mellito, il gigantismo, l'ipotiroidismo e persino l'ipogonadismo.
Ipogonadismo: cos'è negli uomini?
La sindrome dell'ipogonadismo significa sottosviluppo delle gonadi o ridotta funzionalità. Fondamentalmente, la sua patogenesi è caratterizzata da una diminuzione della produzione di steroidi maschili, compaiono segni di infantilismo, cioè c'è uno sviluppo inverso da uomo a ragazzo, a causa di.
IMPORTANTE: la concentrazione di androgeni dipende non solo dallo stato normale degli organi che lo producono direttamente, ma anche dal sistema endocrino situato nel cervello. Secondo la Classificazione Internazionale delle Malattie, 10a revisione (ICD 10), all'ipogonadismo può essere assegnato il codice E29 se è associato a disfunzione testicolare ed E23 se è una conseguenza della patologia dell'ipofisi.
Tipi
Esistono molti disturbi che portano al complesso di sintomi descritto, tuttavia, per comodità, è classificato in 3 tipi principali.
Ipogonadismo ipergonadotropo
Causato da un danno al sistema ipotalamo-ipofisi, che domina le altre ghiandole endocrine. Cioè, infatti, è responsabile della produzione di assolutamente tutti gli ormoni nel nostro corpo e la vitalità umana dipende dal suo lavoro.
L'ipotalamo controlla la ghiandola pituitaria e la seconda sintetizza le gonadotropine: ormone follicolo-stimolante (FSH) e ormone luteinizzante (LH), che regolano l'intera attività del sistema riproduttivo. In questo tipo di ipogonadismo si verifica una produzione eccessiva o anormale di questi ormoni.
Ipogonadismo normogonadotropo
Questo tipo differisce dal precedente in quanto la ghiandola pituitaria funziona normalmente, ma il problema sorge direttamente nelle gonadi. La formazione di testosterone nelle cellule di Leydig dei testicoli viene interrotta, solitamente a causa di cambiamenti infiammatori o cicatriziali.
Ipogonadismo ipogonadotropo
È caratterizzato da una diminuzione della funzione secretoria del sistema endocrino dominante: diminuisce la sintesi delle gonadotropine nelle strutture del cervello, il che comporta il sottosviluppo dei testicoli e, di conseguenza, una diminuzione della produzione di steroidi.
Cause
Molti ricercatori dividono le cause dell’ipogonadismo in due grandi gruppi.
Congenito (primario):
- completa assenza di testicoli;
- non scendere nello scroto;
- Sindrome di Klinefelter (cromosoma X extra nei maschi, formula 47, XXY);
- Sindrome di Heller-Nelson (sviluppo improprio delle cellule di Leydig nei testicoli, che porta a una diminuzione della produzione di testosterone);
- la malattia di de la Chapelle (un disturbo della divergenza dei cromosomi sessuali, a seguito della quale una persona sembra un uomo, ma ha un set femminile di cromosomi 46, XX);
- Complesso di sintomi di Morris (completa insensibilità dei recettori nel corpo agli androgeni) e sindrome di Reifenstein (insensibilità parziale);
- Sindrome di Jacobs (47, XYY);
- distrofia miotonica (una malattia genetica caratterizzata da debolezza dei muscoli del viso e delle braccia, nonché alterazioni della tiroide, del pancreas e delle gonadi);
- Malattia di Del Castillo (durante lo sviluppo nel grembo materno non si formano le cellule primarie delle gonadi);
- sottosviluppo delle cellule di Leydig e, di conseguenza, produzione insufficiente del principale ormone maschile;
- Sindrome di Kallmann (diminuzione ereditaria della produzione di FSH e LH);
- complesso dei sintomi adrenogenitali (deficit genetico dell'enzima che forma gli steroidi).
Acquistato (secondario):
- castrazione;
- atrofia bilaterale, cioè diminuzione del volume e perdita di funzione;
- gli estrogeni in eccesso inibiscono la sintesi di FSH attraverso un meccanismo di feedback;
- orchite;
- esposizione alle radiazioni;
- nell'area della ghiandola pituitaria;
- tumori dell'ipotalamo, dell'ipofisi o dei testicoli;
- infortuni;
- rallentando la degradazione degli estrogeni;
- uso incontrollato di farmaci (citostatici);
- complesso di sintomi iperprolattinemici (che inibisce la secrezione di testosterone);
- con insufficienza renale cronica;
- con cirrosi epatica;
- con anoressia nervosa;
- per altre malattie endocrinologiche (tireotossicosi, ecc.);
- per lesioni della colonna lombare con danni al midollo spinale;
- Carenza di androgeni legata all’età negli uomini.
Sintomi e segni
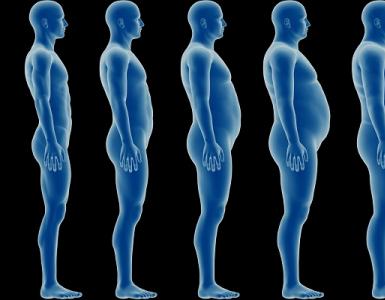
Il testosterone e le gonadotropine influenzano non solo il sistema riproduttivo, ma anche il sistema muscolo-scheletrico. Di conseguenza, se l'ipogonadismo ipofisario è congenito o acquisito durante la maturazione sessuale, si osservano cambiamenti nella normalità delle proporzioni.
Si forma uno scheletro simile a un eunuco: alta statura e arti lunghi. Le ossa diventano sottili e fragili. I muscoli scheletrici sono scarsamente espressi, il grasso si deposita sui fianchi e sui glutei (tipo femminile). Non ci sono cambiamenti nella laringe, la voce rimane alta, come quella di un bambino. La barba, i baffi, i peli pubici e le ascelle sono debolmente espressi. I genitali sono ridotti, il pene è piccolo, non ci sono pieghe sullo scroto e non c'è erezione. Spesso si osserva anche la ginecomastia (ingrossamento benigno delle ghiandole mammarie negli uomini).

Se l'ipogonadismo inizia a progredire in età adulta, i cambiamenti si osservano principalmente nel sistema riproduttivo:
- crescente impotenza;
- scomparsa di erezioni adeguate e spontanee;
- restringimento testicolare.
I peli smettono di crescere sul viso, sulle ascelle e sull'inguine. Si indebolisce, tuttavia, non scompare del tutto. Molto spesso questi uomini soffrono di depressione, nevrosi e frequenti sbalzi d'umore. Può anche svilupparsi ginecomastia.
Diagnosi di ipogonadismo negli uomini
1764 0
Secondo la maggior parte delle definizioni, ipogonadismo significa anche un disturbo della spermatogenesi.
Da un punto di vista funzionale, questo è corretto, poiché il testicolo ha due funzioni: la spermatogenesi e la produzione di testosterone, quindi l'ipogonadismo comporta una violazione di queste funzioni.
Ma da un punto di vista clinico è corretto parlare di ipogonadismo solo quando la produzione di testosterone è ridotta e l'infertilità, soprattutto quando è preservata la secrezione di testosterone, viene identificata come forma separata.
A seconda del momento in cui si manifesta, si distinguono l'ipogonadismo congenito e quello acquisito: a seconda del livello di danno: ipogonadismo primario (testicolare) e centrale (secondario, ipotalamo-ipofisario). Recentemente, ipogonadismo legato all'età, o Deficit di androgeni legato all’età (AAD), che è acquisito e più spesso ha carattere di ipogonadismo misto; così come l'ipogonadismo causato dall'obesità, anch'esso misto.
Nell'ipogonadismo primario (testicolare), il livello delle gonadotropine aumenta secondo il principio del feedback. quindi è chiamato ipergonadotropo. Nell’ipogonadismo secondario (centrale), i livelli di gonadotropine sono ridotti, motivo per cui è chiamato ipogonadismo ipogonadotropo. Le cause dell'ipogonadismo primario e secondario sono presentate nella tabella. 6.1. Con l'ipogonadismo legato all'età e l'ipogonadismo causato dall'obesità, molto spesso non vi è alcun aumento o diminuzione ormone luteinizzante (LG), cioè. si verifica ipogonadismo normogonadotropo.
Caratteristiche delle forme cliniche di ipogonadismo
Le principali cause dell'ipogonadismo ipergonadotropo congenito (primario) sono presentate nella tabella. 6.1.Tabella 6.1. Ipogonadismo congenito ipergonadotropo (primario).
Malattie e condizioni che portano all’ipogonadismo primario acquisito (ipergonadotropo):
Orchite;
parotite;
tubercolosi;
brucellosi;
sifilide;
Castrazione chirurgica;
lesione testicolare;
orchite autoimmune da radiazioni;
epididimite (raro);
vescicolite (raro);
Infarto testicolare (negli adulti) e torsione testicolare (nei bambini);
malattie del fegato (cirrosi e tumori del fegato);
malattie tratto gastrointestinale (Tratto gastrointestinale)(enteropatie: colite ulcerosa, morbo di Crohn);
malattie renali ( fallimento renale cronico (fallimento renale cronico), emodialisi);
malattie polmonari (malattie polmonari croniche ostruttive);
Malattie endocrine (diabete mellito, patologia della tiroide e delle ghiandole surrenali (ipercorticismo), sindrome metabolica e obesità);
malattie del sangue (anemia renale e falciforme);
emocromatosi;
infezioni generalizzate ( Virus dell'AIDS (HIV), tubercolosi, lebbra);
distrofia muscolare;
Lesioni al midollo spinale e al cervello, epilessia;
fibrosi cistica e sindrome di Young;
orchiectomia bilaterale per cancro alla prostata;
esposizione a farmaci, radiazioni, calore, tossine, veleni industriali (citootatici, antimetaboliti, barbiturici, anabolizzanti e androgeni esogeni, spironolattone, farmaci antipertensivi, verapamil, aminoglutetimide, antiandrogeni, corticosteroidi, ketoconazolo, metoclopramide, sulfasalazina, disolfuro di carbonio, dibromocloropropano, acrilammide , arsenico , metalli pesanti, dimetildicloroinil fosfato, benzene, toluene, diossina, xilene, benzina, tetracloruro di carbonio, toluene diammina, tricloretil fosfato, trifosfato, cloruro di vinile).
Tabella 6.2. Ipogonadismo ipogonadotropo (secondario).

Tabella 6.3. Disturbi ipotalamici

Tabella 6.4. Disturbi ipofisari

Cause di disfunzione ipotalamica che portano alla formazione di ipogonadismo secondario (ipogonadotropo):
cambiamenti post-traumatici;
processi tumorali;
malattie granulomatose (tubercolosi, sarcoidosi);
malattie sistemiche:
Cardiovascolare,
- renale,
- endocrino (ipotiroidismo, ipertiroidismo),
- tessuto connettivo (lupus eritematoso sistemico, sclerodermia, dermatomiosite).
Cause di insufficienza ipofisaria che porta a ipogonadismo secondario (ipogonadotropo):
Cambiamenti postencefalici;
processi sclerosanti e proliferativi post-traumatici;
processi tumorali;
ipofisectomia;
insufficienza vascolare del cervello e della ghiandola pituitaria.
Forme rare di ipogonadismo
Forme rare di ipogonadismo negli uomini comprendono la sindrome di Reifenstein (mascolinizzazione incompleta), la sindrome di femminilizzazione testicolare, il deficit di 5α-reduttasi e la persistenza ovarica (Tabella 6.5).Tabella 6.5. Caratteristiche delle forme rare di ipogonadismo

Sindrome di femminilizzazione testicolare: esiste un'insensibilità completa o parziale dei recettori degli androgeni al testosterone. Nella forma completa della femminilizzazione testicolare, a causa del completo sottosviluppo dei genitali esterni maschili, il sesso femminile viene stabilito alla nascita e in futuro, di regola, un ragazzo così genetico vive nel sesso femminile civile.
Nella forma completa di femminilizzazione testicolare, è un grave errore cercare di selezionare il sesso genetico eseguendo operazioni di mascolinizzazione per ripristinare il sesso maschile, poiché, a causa della completa insensibilità agli androgeni, nonostante il loro contenuto normale, esiste un quadro clinico di ipogonadismo, resistente alla terapia farmacologica.
Con una forma incompleta di femminilizzazione testicolare alla nascita, si osserva un sottosviluppo dei genitali esterni, dell'ipospadia, del micropene o del pene piccolo, che successivamente richiedono un intervento chirurgico. Nonostante i normali livelli di testosterone, esiste un quadro clinico di ipogonadismo. Ai pazienti viene prescritta una terapia con alte dosi di farmaci androgeni. Il criterio per l'efficacia della terapia è il quadro clinico e la normalizzazione del PH.
Forme di ipogonadismo indotte da farmaci
L'ipogonadismo può svilupparsi durante l'assunzione di alcuni farmaci; le principali forme di questo tipo di ipogonadismo sono presentate nella tabella. 6.6.Tabella 6.6. Forme di ipogonadismo indotte da farmaci (secondo Jockenhovel F., 2004)


Classificazione operativa dell'ipogonadismo
Ipogonadismo ipogonadotropo (secondario o terziario).
Congenito:Sindrome di Kallmann.
Sindromi di Prader-Willi, Lawrence-Moon-Biedl, Pasqualini, Maddock.
Tumori.
Lesioni granulomatose (tubercolosi, sarcoidosi).
Infezioni.
Lesioni.
Conseguenze della chirurgia e delle radiazioni.
Emorragie.
Lesioni autoimmuni.
Emocromatosi.
Lesioni funzionali acquisite della regione ipotalamo-ipofisi:
Iperprolattinemia.
Malnutrizione, anoressia nervosa.
Attività fisica intensa, stress.
Obesità.
Malattie della tiroide (tireotossicosi, ipotiroidismo).
Farmaci.
Ipogonadismo ipergonadotropo (primario).
Congenito:Le sindromi di Klinefelter, Noonan.
Criptorchidismo.
Insufficienza degli enzimi della steroidogenesi nei testicoli.
Lesioni organiche acquisite della regione ipotalamo-ipofisi:
Trauma o torsione dei testicoli.
Castrazione.
Orchite.
Irradiazione testicolare.
Chemioterapia.
Flusso sanguigno alterato nei testicoli dopo l'intervento chirurgico.
Esposizione al calore eccessivo.
Impatto dei fattori ambientali.
Medicinali.
Alcol.
Droghe.
Ipogonadismo primario o secondario:
Uremia.
Sindrome da immunodeficienza progressiva (AIDS).
Medicinali.
Malattie croniche gravi.
Ipercorticismo.
Manifestazioni cliniche e diagnosi dell'ipogonadismo
Nella tabella sono presentate le caratteristiche dei vari tipi di ipogonadismo maschile in base ai cambiamenti nei livelli ormonali. 6.7.Tabella 6.7. Caratteristiche dei vari tipi di ipogonadismo maschile

Le manifestazioni cliniche dell'ipogonadismo dipendono dal momento della sua insorgenza", e quindi si distinguono forme pre-puberali e post-puberali di ipogonadismo. Nella tabella La tabella 6.8 presenta le principali manifestazioni cliniche di varie forme di ipogonadismo a seconda del momento in cui si manifesta.
Tabella 6.8. Le principali manifestazioni cliniche dell'ipogonadismo negli uomini dipendono dai tempi in cui si verifica

Per valutare clinicamente la gravità dell’ipogonadismo maschile, viene eseguito il seguente esame:
1. Valutazione dello sviluppo somatico generale (altezza, peso, valutazione del tipo di costituzione sessuale, valutazione della presenza e gravità dei caratteri sessuali primari e secondari).
2. Determinazione della circonferenza della vita e indice di massa corporea (IMC). Secondo la moderna definizione dell'IDF - International Diabetes Federation (2005), il criterio per l'obesità centrale (addominale) è una circonferenza vita (WC) superiore a 94 cm negli uomini e superiore a 80 cm nelle donne. L’obesità addominale è spesso associata a ipogonacismo, disfunzione erettile e sindrome metabolica.
La sindrome metabolica comprende la presenza di obesità centrale in combinazione con almeno due dei seguenti disturbi:
Aumento dei livelli di trigliceridi superiore a 1,7 mmol/L (150 mg/dL).
Abbassare i livelli di colesterolo lipoproteine ad alta densità (HDL) meno di 1,04 mmol/L (40 mg/dL) negli uomini.
Promozione pressione sanguigna (BP) più di 130/85 mmHg. Arte. o assumendo farmaci antipertensivi.
Iperglicemia a digiuno superiore a 5,6 mmol/l (100 mg/dl).
Diabete mellito precedentemente diagnosticato o ridotta tolleranza al glucosio.
L'IMC si calcola utilizzando la formula: BMI = peso corporeo (kg) / altezza (m)2.
Per adulti:
Sovrappeso - BMI >25 kg/m2;
obesità - BMI > 30 kg/mg;
“pre-obesità” - BMI 25,0-29,9 kg/m2.
3. Valutazione dello stadio dello sviluppo sessuale (pene, testicoli, peli pubici) secondo Tanner. 4. Valutazione della presenza e della gravità della ginecomastia secondo Tanner.
5. Dati antropometrici secondo Decourt-Dumik.
Durante un esame antropometrico utilizzando il metodo Decourt-Dumik, è necessario misurare i seguenti indicatori:
Circonferenza del torace.
altezza della gamba (dal pavimento al grande trocantere).
altezza.
larghezza del bacino (tra i grandi trocanteri).
larghezza delle spalle.
Normalmente la differenza tra la larghezza delle spalle e la larghezza del bacino negli uomini dovrebbe essere superiore a 10-12 cm Una diminuzione di questo valore indica la presenza di segni di carenza di androgeni.
Inoltre, viene calcolato l'indice trocanterico:
Indice trochateral = altezza (cm) / lunghezza gamba (cm)
Normalmente, l'indice trocanterico è 1,93-1,97. Una diminuzione dell'indice trocanterico ad un valore inferiore a 1,92 indica la presenza di segni di fisico eunucoide (carenza di androgeni o ipogonadismo).
6. Misurazione del volume testicolare (orchidometro Prader o testometro Demchenko).
7. Determinare la natura dei peli pubici è un indicatore clinico abbastanza accurato della saturazione di androgeni nel corpo maschile. Con livelli normali di testosterone, i peli pubici si estendono verso l'ombelico a forma di diamante (modello di peli maschili). Con l'ipogonadismo si osserva un tipo femminile di peli pubici, in cui è presente una linea orizzontale del bordo superiore della crescita dei peli pubici.
8. Misurazione della lunghezza del pene a riposo e durante l'erezione. È stata dimostrata una chiara correlazione tra la lunghezza del pene in estensione e in erezione (D. Smith, 2004). Se è impossibile valutare la lunghezza del pene eretto, cosa che nella maggior parte dei casi avviene durante l'esame medico, è possibile misurare la lunghezza dell'organo in stato allungato e confrontarla con le deviazioni medie di dimensione.
Trattamento dell'ipogonadismo
Non ci sono difficoltà nel trattamento dell’ipogonadismo. In ogni caso, la terapia dovrebbe portare alla completa normalizzazione delle manifestazioni cliniche e dei livelli sierici di testosterone. Con l'ipogonadismo primario è possibile solo un tipo di terapia: la terapia con farmaci androgeni esogeni. La terapia farmacologica per l'infertilità con ipogonadismo primario è impossibile.Per l'ipogonadismo secondario sono possibili due approcci: terapia con farmaci esogeni e terapia stimolante gonado corionicatropina (HG), mirato a stimolare la secrezione di testosterone endogeno. Se l'obiettivo è ripristinare la spermatogenesi, allora si dovrebbe dare la preferenza alla terapia con gonadotropine, che nella metà dei casi consente di ripristinare o migliorare la spermatogenesi. Per tutte le forme congenite di ipogonadismo, la terapia dovrebbe durare tutta la vita.
Preparati a base di testosterone usati per trattare l'ipogonadismo maschile

Riso. 6.6. Quota di varie forme di farmaci androgeni sul mercato farmaceutico russo (2007)
Preparazioni orali di testosterone:
Testosterone undecanoato (Andriol),
metiltestosterone (vietato in molti paesi del mondo),
fluossimesterone.
mesterolone (Proviron, Vistimon - interrotto).
Andriol è un preparato orale di testosterone che viene assorbito nella linfa bypassando il fegato. Quando si utilizza questo farmaco, è abbastanza difficile creare una concentrazione costante e stabile dell'ormone nel sangue (rapidi cambiamenti non fisiologici della concentrazione), poiché l'assorbimento dipende dallo stato del tratto gastrointestinale.
Si consiglia di assumere il farmaco con cibi grassi, che ne migliorano l'assorbimento nell'intestino. È usato nel trattamento delle forme lievi di ipogonadismo legato all'età, nel trattamento del ritardo puberale costituzionale nei ragazzi e nella carenza di androgeni nelle donne (non registrato per questa indicazione).
Il metiltestosterone e il fluoxymesterone sono farmaci epatotossici vietati per la produzione e l'uso in molti paesi del mondo. L'unico paese al mondo in cui viene prodotto e prescritto il metiltestosterone. è la Russia.
Il Mesterolone è un derivato 5a-diidrotestosterone (5a-DHT). Non viene distrutto nel fegato e non subisce aromatizzazione. Poiché non ha l’intera gamma di effetti del testosterone, non è adatto per la terapia sostitutiva a lungo termine dell’ipogonadismo.La produzione del farmaco è stata interrotta e non è disponibile in Russia.
Preparazioni iniettabili di testosterone:
Testosterone propionato e fenilpropionato.
Testosterone capronato (decanoato) e isocapronato.
Entag del testosterone.
Testosterone cypionato.
Testosterone undecanoato (Nebido).
Testosterone biciclato.
Combinazione di esteri di testosterone (Sustanon-250, Omnadren-250).
Microsfera di testosterone.
Il testosterone propionato ha un'emivita breve e deve essere somministrato ogni 2-3 giorni, quindi di solito non viene utilizzato come farmaco singolo. Tali trasmissioni. Come il cypionate e l'enantato, hanno una durata d'azione media, di solito vengono utilizzati una volta ogni 7-14 giorni.
Nel nostro paese, i farmaci combinati più comuni per la somministrazione intramuscolare sono quelli contenenti una miscela di testosterone capronato, isocapronato, propionato e fenilpropionato (Sustanon-250, società Organon). Il testosterone propionato inizia ad agire rapidamente, ma entro la fine del primo giorno il suo effetto praticamente cessa, l'effetto del fenilpropionato e dell'isocapronato si osserva dopo circa un giorno, l'effetto dura fino a due settimane. Il farmaco ad azione più lunga è il capronato; il suo effetto può durare fino a 3-4 settimane.
Recentemente sono stati sintetizzati nuovi esteri di testosterone, come il biciclato e l'undecanoato (Nebido), la durata d'azione di quest'ultimo raggiunge i tre mesi. Il farmaco preferito tra le forme iniettabili è il farmaco Nebido (Bayer Schering Pharma), la cui farmacocinetica differisce dagli altri esteri del testosterone.
Nebido è un'iniezione a lunga durata d'azione di estere undecanoato di testosterone (soluzione oleosa di testosterone undecanoato 1000 mg in 4 ml di olio di ricino). Nebido è un farmaco per somministrazione parenterale (si consiglia un'iniezione lenta e profonda del farmaco nel muscolo gluteo) a rilascio lento del principio attivo, che viene utilizzato 4 volte l'anno e allo stesso tempo mantiene la concentrazione di testosterone nel sangue entro i limiti fisiologici durante l'intero periodo tra le iniezioni.
I livelli sierici di testosterone aumentano il giorno successivo alla somministrazione intramuscolare del farmaco, raggiungendo le concentrazioni massime dopo 7-10 giorni. L'emivita è di circa 90 giorni. Le proprietà farmacodinamiche del testosterone undecanoato sono identiche agli effetti fisiologici del testosterone. Iniezioni ripetute di Nebido promuovono un graduale aumento del livello di testosterone totale nel plasma sanguigno entro valori fisiologici, la normalizzazione delle concentrazioni di diidrotestosterone, estradiolo e globulina legante gli steroidi sessuali (SSSG).
Uno studio sul livello degli ormoni gonadotropici ha rivelato una diminuzione graduale e stabile di LH e ormone che stimola i follicoli (FSH) con l’uso a lungo termine di Nebido. Nel valutare l'effetto del farmaco sul metabolismo dei lipidi, una diminuzione del livello di colesterolo totale e lipoproteine a bassa densità (LDL). Potrebbe verificarsi un moderato aumento della concentrazione di emoglobina sierica entro i valori fisiologici.
Le manifestazioni cliniche dell'azione di Nebido si esprimono soggettivamente nel miglioramento del benessere generale e della funzione sessuale, nel miglioramento dell'umore, nella stabilizzazione del background psico-emotivo e nell'aumento della soddisfazione soggettiva per la vita sessuale. Con la terapia a lungo termine sono stati notati anche cambiamenti oggettivi: diminuzione del grasso e aumento della massa muscolare dei pazienti, aumento della densità minerale ossea. Con il regime di somministrazione del farmaco selezionato, il monitoraggio del testosterone sierico nel sangue deve essere effettuato una volta all'anno.
L'uso del farmaco durante il primo anno richiede il monitoraggio dei livelli di testosterone 12 settimane dopo l'iniezione per selezionare un regime adeguato per la somministrazione della terapia sostitutiva (per alcuni pazienti è sufficiente somministrare il farmaco una volta ogni 12-16 settimane).
Le microsfere (impianti) di testosterone da 1200 mg vengono utilizzate solo in Inghilterra, Australia e Sud Africa; vengono iniettate sotto la pelle dell'addome utilizzando uno speciale trequarti. Fornire effetti di testosterone per 4-6 mesi.
Forme cutanee di testosterone:
Cerotti di testosterone, cutanei e scrotali (Testoderm, Androderm, Virormon);
gel per uso esterno (Androgel);
Gel 5a-diidrotestosterone (Andractim).
Andractim è l'unica preparazione cutanea di 5a-diidrotestosterone. Disponibile sotto forma di gel idroalcolico al 2,5% e non fornisce tutti gli effetti del testosterone. Utilizzato solo in Francia e Uruguay. Viene utilizzato per aumentare le dimensioni dei genitali esterni quando sono sottosviluppati. Non registrato in Russia,
Androgel (società Solvay) è l'unico gel di testosterone all'1% in Russia che, con l'applicazione cutanea quotidiana, garantisce una concentrazione fisiologica costante dell'ormone nel sangue. Il gel transdermico viene applicato sulla pelle pulita una volta al giorno, preferibilmente al mattino (solitamente sulla parte superiore del braccio, sulla parte superiore del braccio o sull'addome). Il farmaco non deve essere applicato sui genitali a causa del possibile effetto irritante dell'alcol. Androgel fornisce un apporto transdermico costante di testosterone per 24 ore e mantiene i livelli circolanti di testosterone entro i limiti normali per gli uomini sani.
Dopo aver applicato Androgel, non è consigliabile fare la doccia, nuotare o avere rapporti sessuali per 5 ore, necessarie per il completo assorbimento del testosterone dalla superficie della pelle. Androgel 5 g contiene 50 mg di testosterone. Circa il 10% della dose applicata quotidianamente sulla superficie cutanea entra nella circolazione sistemica. Dopo aver interrotto l'uso di Androgel, la concentrazione media di testosterone ritorna al livello originale il 4° giorno dopo l'ultima applicazione.
Contemporaneamente all'aumento dei livelli di testosterone, aumenta la concentrazione di estradiolo, non superando i valori tipici degli uomini sani, e la concentrazione di 5a-diidrotestosterone, cioè. Androgel ha lo spettro completo dell’azione del testosterone.
Numerosi studi hanno dimostrato l'efficacia e la sicurezza di Androgel nel trattamento dell'ipogonadismo negli uomini.Sotto l'influenza del farmaco, sullo sfondo di un aumento della concentrazione di testosterone nel sangue, si osserva un miglioramento dell'umore e della funzione sessuale, una diminuzione del riassorbimento osseo e un miglioramento della qualità delle erezioni spontanee e adeguate.
Durante il trattamento con Androgel, per aggiustare la dose, 14 giorni dopo l'inizio della terapia, viene determinato il livello di testosterone nel sangue. Se è inferiore alla norma o non si ottiene l'effetto clinico desiderato, è possibile aumentare la dose giornaliera di Androgel 1% da 5 ga 7,5 go fino a 10 g dopo aver consultato un medico. La correzione del regime posologico deve essere effettuata gradualmente, 2,5 g al giorno.
Sulla base di numerosi studi, Androgel ha dimostrato di essere ben tollerato. Durante la terapia con Androgel. come gli altri androgeni. è necessario monitorare la funzionalità epatica, lo stato del sangue rosso (emoglobina, ematocrito), il livello antigene specifico della prostata (PSA) condizioni del sangue e della prostata (esame rettale digitale).
Il farmaco è disponibile in buste di alluminio in confezioni di cartone da 30 pezzi. Ogni bustina contiene 1 dose del farmaco - rispettivamente 2,5 o 5 g di gel contenente. 25 o 50 mg di testosterone
Il farmaco non è indicato per le donne e la sua sicurezza ed efficacia nei bambini non sono state stabilite.
Anche l’industria farmaceutica e i farmaci per la somministrazione sublinguale di androgeni non sono stati risparmiati. È stata creata una forma di preparazione di testosterone con ciclodestrina, che ne consente l'uso per via sublinguale.
Attualmente, un nuovo gruppo di farmaci con proprietà androgene viene studiato attivamente. Questi sono i cosiddetti modulatori selettivi del recettore degli androgeni (SARM). Come questi, esistono e vengono già utilizzati con successo nella pratica modulatori dei recettori degli estrogeni come il tamoxifene. raloxifene. keossifene. Droloxifene.
Il meccanismo d'azione di questi farmaci è che, agendo sui recettori degli steroidi, mostrano solo un certo spettro della loro attività e non hanno una serie di effetti indesiderati (in relazione agli androgeni, ad esempio, sulla prostata e sui lipidi nel sangue), ciò è dovuto al loro diverso grado di agonismo nei confronti dei recettori presenti nei vari tessuti. Un esempio di tale composto è il 7a-metil-19-nortestosterone (Metil NorTestosreron - MENT).
Inoltre, questo composto non viene metabolizzato in diidrotestosterone? allo stesso tempo è capace di aromatizzazione. Negli studi, il MENT ha mostrato un effetto più potente sui gonadotropi e meno sul tessuto prostatico. Attualmente sono in corso esperimenti con questo composto; viene testato come contraccettivo per gli uomini e per l'uso in caso di ipogonadismo.
La ricerca della forma più conveniente, efficace e sicura di preparati androgeni continua. Si può presumere che non esista un farmaco ideale; ognuno di essi presenterà alcuni vantaggi e svantaggi di cui il medico dovrà tenere conto individualmente nel trattamento dei pazienti (Tabelle 6.9 e 6.10).
Tabella 6.9. Classificazione dei farmaci androgeni in base ai metodi di utilizzo

Tabella 6.10. Criteri per valutare l'efficacia della terapia con testosterone

Terapia stimolante dell'ipogonadismo con preparati di gonadotropina corionica
L'obiettivo della terapia è stimolare la spermatogenesi e la sintesi del testosterone endogeno mantenendo la funzione di riserva delle gonadi.La funzione di riserva delle gonadi è considerata intatta se, dopo iniezioni di hCG per tre giorni alla dose di 1500-2000 UI, il livello inizialmente basso di testosterone aumenta di oltre il 30-50% rispetto al livello originale. In questo caso, puoi contare sull'effetto della terapia stimolante con farmaci hCG (Tabella 6.11). In caso di risposta negativa al test con gonadotropina corionica umana (hCG) mostrato Terapia sostitutiva con androgerone (AZT) preparati a base di testosterone (Tabella 6.12).
Tabella 6.11. Preparati di gonadotropina corionica utilizzati nel trattamento dell'ipogonadismo secondario

Tabella 6.12. Caratteristiche comparative della terapia con gonadotropina corionica umana e AZT con preparati a base di testosterone

Controindicazioni alla terapia con gonadotropina corionica umana, ipersensibilità al farmaco
Analoghi dell'FSH
Per compensare la carenza di FSH e stimolare la spermatogenesi, vengono utilizzati gli analoghi dell'FSH: gonadotropine della menopausa (menotropina - Menagon, Pergonal, Humegon; urofol-litropina - Metrodin). Attualmente esiste una preparazione di FSH ricombinante (Gonal-F), prodotta in flaconi da 75 UI e fiale da 150 UI. Utilizzato 150 UI 3 volte a settimana insieme all'hCG per 4-18 mesi, nel trattamento dell'infertilità endocrina.
S.Yu. Kalinchenko, I.A. Tyuzikov
Di norma, l'ipogonadismo ipogonadotropo è associato al sottosviluppo degli organi genitali e alle caratteristiche sessuali secondarie. Anche il metabolismo dei grassi e delle proteine nella patologia viene interrotto, causando obesità, cachessia, disturbi nel sistema scheletrico e interruzioni nel funzionamento del cuore.
Quali medici devo contattare?
Va notato che esiste una differenza tra ipogonadismo ipogonadotropo maschile e femminile.
La diagnosi e il trattamento della malattia vengono effettuati congiuntamente da endocrinologi, ginecologi e ginecologi-endocrinologi se il paziente è una donna e andrologi se il paziente è un uomo.
Si verifica una diminuzione della produzione di ormoni sessuali, che provoca un aumento del livello delle gonadotropine, che stimolano le ovaie.
L'analisi rileva un alto livello di ormoni che stimolano i follicoli e la luteina, nonché un basso livello di estrogeni. Un livello ridotto di estrogeni provoca atrofia o sottosviluppo degli organi genitali femminili, delle ghiandole mammarie e assenza di mestruazioni.
Se la funzione ovarica era compromessa prima della pubertà, allora vi è un'assenza di caratteristiche sessuali secondarie.

L'ipogonadismo ipogonadotropo nelle donne nella sua forma primaria si osserva nelle seguenti condizioni:
- disturbo congenito a livello genetico;
- ipoplasia ovarica congenita;
- processi infettivi (sifilide, tubercolosi, parotite, radiazioni, rimozione chirurgica delle ovaie);
- danno di natura autoimmune;
- sindrome delle ovaie policistiche.
L'ipogonadismo ipogonadotropo secondario nelle donne si verifica a causa della patologia della ghiandola pituitaria e dell'ipotalamo. Si distingue per un basso contenuto o la completa cessazione della produzione di gonadotropine che regolano la funzione ovarica. Questo processo è innescato dall'infiammazione nell'area del cervello. Tali malattie hanno un effetto dannoso e sono accompagnate da una diminuzione del livello di effetto delle gonadotropine sulle ovaie.
Che relazione c'è tra malattie come l'ipogonadismo ipogonadotropo nelle donne e la gravidanza? Anche lo sviluppo intrauterino sfavorevole del feto può influenzare l'insorgenza della patologia.

I sintomi della malattia nelle donne
I sintomi vividi della malattia durante il periodo fertile sono periodi irregolari o la loro assenza.
Bassi livelli di ormoni femminili portano al sottosviluppo degli organi genitali, delle ghiandole mammarie, alla ridotta deposizione di tessuto adiposo e alla scarsa crescita dei capelli.
Se la malattia è congenita, i caratteri sessuali secondari non compaiono. Le donne hanno il bacino stretto e le natiche piatte.
Se la malattia si verifica prima della pubertà, le caratteristiche sessuali apparse rimangono preservate, ma le mestruazioni si fermano e i tessuti genitali si atrofizzano.
Effettuare la diagnostica
Con l'ipogonadismo si verifica una diminuzione dei livelli di estrogeni e un aumento delle gonadotropine. L'ecografia rivela un utero ridotto, diagnostica l'osteoporosi e la formazione scheletrica ritardata.
Trattamento della patologia nelle donne
Come viene eliminato l'ipogonadismo ipogonadotropo nelle donne? Il trattamento prevede la terapia sostitutiva. Alle donne vengono prescritti farmaci e ormoni sessuali (etinilestradiolo).
In caso di mestruazioni vengono prescritti contraccettivi orali contenenti estrogeni e gestageni, nonché i farmaci Triziston e Trikvilar.
I farmaci "Klimen", "Trisequence", "Klimonorm" sono prescritti ai pazienti dopo i 40 anni.
Il trattamento con farmaci ormonali è controindicato nelle seguenti condizioni:
- tumori oncologici nell'area delle ghiandole mammarie e degli organi genitali;
- malattie del cuore e dei vasi sanguigni;
- patologia renale ed epatica;
- tromboflebite.

Prevenzione
Una malattia come l'ipogonadismo ipogonadotropo ha una prognosi favorevole. La prevenzione consiste nella popolazione e nella sorveglianza delle donne incinte, nonché nelle misure sanitarie.
La condizione patologica del sistema riproduttivo umano, in cui vi è una diminuzione della secrezione di ormoni sessuali e, in risposta a ciò, un aumento della secrezione di ormoni gonadotropici, è chiamata ipogonadismo ipergonadotropico.
Questa malattia può colpire sia uomini che donne. È pericoloso a causa dello sviluppo dell'infertilità e dell'insorgenza di altre malattie che rappresentano una minaccia diretta per la vita umana.
Spesso le caratteristiche dell'ipogonadismo iperprolattinemico sono sfumate, quindi la sua diagnosi può essere difficile. Tuttavia, una volta identificata la malattia, è possibile correggerla facilmente.
Nella classificazione della malattia dell'ipogonadismo si distinguono tre tipi di patologia:
- Primaria, con danno direttamente alle gonadi (testicoli nei maschi e ovaie nelle femmine), con aumento della secrezione di LH e FSH.
- Secondaria quando si verificano disfunzioni del sistema ipotalamo-ipofisi, con aumento di LH e FSH.
- Norgonadotropico - con livelli normali di LH e FSH, manifestazione di sintomi di ipogonadismo.
Esiste anche l'ipogonadismo iperprolattinemico, una patologia dell'ipofisi in cui inizia la produzione incontrollata di prolattina. Porta a gravi disturbi nel corpo.
Sindrome dell'ipogonadismo ipergonadotropo
L'ipergonadotropo è una forma particolare di ipogonadismo, o meglio la sua forma primaria.
Una caratteristica distintiva dell'ipogonadismo primario è il verificarsi di uno sviluppo sessuale ritardato sullo sfondo di una funzione attenuata delle gonadi e del sottosviluppo degli organi genitali.
Esistono forme congenite e acquisite della malattia. Con cause sconosciute, questa malattia è chiamata idiopatica.

Cause di ipogonadismo ipergonadotropo congenito
Tra i fattori che portano alla forma primaria di ipogonadismo ci sono i seguenti:
- cambiamenti genetici nel gruppo di geni XY e XX;
- anomalia congenita dei testicoli e delle ovaie, fino alla loro assenza;
- processi autoimmuni che iniziano nel periodo uterino dello sviluppo.
Anche l'ipotiroidismo, che colpisce un bambino nel grembo materno affetto da danni alla ghiandola tiroidea, può essere considerato causa di una patologia di tipo congenito.
Cause dell'HS acquisita
L'ipogonadismo ipergonadotropo primario acquisito può avere cause leggermente diverse:
- traumi ai genitali e alle ghiandole;
- sottoposti a trattamenti con potenti sostanze chimiche;
- i ragazzi possono sperimentare una discesa ritardata dei testicoli nello scroto;
- , ricevendo una grande dose di radiazioni;
- malattie del fegato, dei reni, dei polmoni, del tratto gastrointestinale;
- esposizione ad alcol, droghe;
- malattie infettive (tubercolosi, sifilide, parotite).
La forma acquisita della malattia lascia il sistema riproduttivo nel suo sviluppo al livello da cui ha iniziato a manifestarsi la patologia.
Può iniziare il suo sviluppo all'età di 12-13 anni, quindi, ad esempio, l'utero e le ghiandole mammarie di una ragazza possono rimanere sottosviluppate.
La forma acquisita può manifestarsi in età adulta, sopprimendo la libido e portando alla completa atrofia del sistema riproduttivo.
La sindrome dell'ipogonadismo ipergonadotropo può manifestarsi nelle ragazze con l'assenza di crescita del seno e di crescita secondaria dei capelli fino a 13 anni e con l'assenza di mestruazioni fino a 15 anni. Nei ragazzi si manifesta con una pubertà ritardata entro i 14 anni.

Forma secondaria e sue cause
La forma secondaria, cioè l'ipogonadismo ipogonadotropo, può essere anche congenita o acquisita.
Le forme congenite comprendono principalmente varie anomalie genetiche della ghiandola pituitaria. Tali sindromi sono rare, ma sono state studiate abbastanza bene. Ci sono più di 20 patologie di questo tipo in totale.
Ci sono anche diverse ragioni per lo sviluppo delle forme acquisite:
- tumori oncologici nella ghiandola pituitaria;
- irradiazione a lungo termine;
- ictus o emorragie nella ghiandola pituitaria.
La diagnosi della forma secondaria può essere più difficile, poiché le ghiandole e gli organi genitali esterni possono apparire sani. Per completare il quadro, quando si studia questo tipo di malattia, sarà necessario eseguire una risonanza magnetica del cervello.

I sintomi di questa malattia
I segni di patologia possono variare a seconda del momento di insorgenza della malattia.
Esistono ipogonadismo prepuberale, che è caratterizzato dalle seguenti manifestazioni:
- Crescita elevata con preservazione della funzione GH e crescita bassa con assenza di secrezione di GH.
- Figura corporea sproporzionata. Nei ragazzi si sviluppa secondo il principio femminile, con deposizione di grasso sull'addome e sui glutei. In entrambi i sessi resta la tendenza ad allungare le gambe e le braccia e ad accorciare il busto.
- Flaccidità muscolare, ingrossamento del seno secondo il principio femminile.
- Mancanza di caratteristiche sessuali secondarie: crescita dei capelli, voce ruvida.
- Nei ragazzi il pene rimane entro i 5 cm, mentre lo scroto è leggero e senza rughe.
I sintomi del periodo postpuberale della sindrome da ipogonadismo negli uomini includono quanto segue:
- Libido non risvegliata o sua attenuazione.
- Disfunzione erettile.
- Incapacità di raggiungere l'orgasmo.
- Incapacità di eiaculare.
- Riduzione della quantità di peli pubici, diradamento e caduta.
- Pene più di 5 cm, scroto con rughe e pigmentazione medie.
Ha caratteristiche pronunciate che sono evidenti in qualsiasi fase di sviluppo dell'organismo. Questa patologia può portare alla sterilità, che non può essere curata.

Complicazioni
Se la secrezione degli ormoni gonadotropici viene interrotta, possono verificarsi le seguenti complicazioni:
- aumento di peso ampio e rapido;
- dislipidemia;
- aterosclerosi vascolare;
- malattia ischemica.
Inoltre, si verificano tutti i tipi di disfunzioni del sistema riproduttivo, che non portano solo disagio, ma possono anche causare infertilità e, infine, portare al cancro alla prostata o alle ovaie.
Interessante!
L'ipogonadismo normgonadotropo si verifica negli uomini di età superiore alla mezza età, il più delle volte affetti da obesità grave.

Ipogonadismo iperprolattinemico
A causa di un eccesso di prolattina può verificarsi un disturbo della funzione sessuale del corpo, chiamato ipogonadismo iperprolattinemico.
La sua secrezione aumenta a causa della mutazione dei prolattotrofi, cellule dell'ipofisi in cui avviene la sintesi di questo ormone.
Cause dell'ipogonadismo iperprolattinemico
Perché appare una condizione come questa?
Ci sono diversi fattori che portano a questo disturbo:
- , che influenza la funzione ormonale del cervello;
- tossicodipendenza;
- ipotiroidismo;
- insufficienza renale;
- mantenere alti livelli di prolattina per 3 anni dopo il parto.
Inoltre, i pazienti con ipogonadismo iperprolattinemico possono mantenere involontariamente un disturbo ipofisario controllando costantemente la presenza di secrezioni nelle ghiandole mammarie. In questo caso, alla patologia principale si aggiunge un disturbo nevrotico.

Sintomi
Gli indicatori clinici della malattia dell'ipogonadismo iperprolattinemico possono variare nella loro manifestazione: dalla completa assenza di sintomi alla manifestazione di un quadro clinico vivido.
Le manifestazioni più comuni di questa malattia sono:
- interruzioni del ciclo mestruale, cambiamenti nella sua durata o completa scomparsa;
- impossibilità di concepimento, aborto spontaneo;
- la secrezione dai capezzoli, può verificarsi sia nelle donne che negli uomini, si verifica in circa il 25% dei casi;
- le donne possono avere disturbi della libido, sensazione di secchezza e bruciore nella vagina;
- gli uomini perdono l'erezione;
- emicranie, depressione;
- sul viso, sul petto, aumento di peso in eccesso.
Nelle donne vengono spesso rilevate ipoplasia uterina e anovulazione. Gli uomini affetti dalla malattia dell'ipogonadismo iperprolattinemico soffrono di infertilità, ovvero dell'assenza di spermatozoi vitali nel seme.

Misure diagnostiche
Un singolo aumento della prolattina non può essere una conferma diretta dell'ipogonadismo iperprolattinemico. Il risultato del test della prolattina deve essere ottenuto tre volte.
Sono escluse le seguenti malattie:
- PCOS (questa è l'abbreviazione di una patologia chiamata);
- patologia della tiroide;
- insufficienza renale;
- insufficienza epatica;
- fallimento dovuto all’abuso di farmaci.
Per confermare la diagnosi di ipogonadismo iperprolattinemico saranno necessari i seguenti studi:
- Esame del paziente dal punto di vista della presenza dell'intero complesso di manifestazioni patologiche.
- Lo screening del sangue per gli ormoni, mentre una concentrazione di prolattina superiore a 3000 mU/l indicherà la presenza di un tumore nella ghiandola pituitaria.
- Risonanza magnetica del cervello.
Di per sé, un aumento della prolattina nel sangue potrebbe non essere sempre indice di ipogonadismo iperprolattinemico; ad esempio, aumenta durante l'allattamento al seno o interruzioni occasionali del sistema riproduttivo dovute allo stress.
Terapia della malattia
Le principali direzioni di trattamento della sindrome dell'ipogonadismo ipergonadotropo possono essere considerate i seguenti metodi:
- Trattamento con ormoni (negli uomini vengono utilizzati preparati a base di testosterone).
- Ripristino di uno stato mentale normale con l'aiuto di antidepressivi medicinali.
- Ripristino della libido e della funzione erettile.
- Misure preventive per prevenire prematuri.
I farmaci di base del corso sono farmaci ormonali. Sono selezionati individualmente, tenendo conto delle caratteristiche della sindrome.
L'ipogonadismo negli uomini non è una malattia indipendente, ma una sindrome patologica (complesso di sintomi) che deriva da molte cause ed è una manifestazione di varie malattie. Il termine deriva dal latino ipo - inferiore, mancanza, gonadis - ghiandole sessuali che producono ormoni e determinano il sesso.
Molto spesso, nei ragazzi si verifica l'ipogonadismo, chiamato anche insufficienza dello sviluppo sessuale, ma può svilupparsi anche negli uomini adulti a causa di determinati fattori. Questa è una grande tragedia per il sesso più forte, accompagnata dalla perdita delle caratteristiche sessuali esterne, da una diminuzione delle capacità sessuali e da gravi disturbi di salute. Un grosso problema è anche il disadattamento sociale dei pazienti, quando diventano emarginati nei gruppi, nella società e spesso nelle famiglie.
La patologia ha un codice secondo l'ICD-10 (classificazione internazionale delle malattie) E29 - disfunzione testicolare, sottoparagrafo E29.1 - ipofunzione testicolare.
Per comprendere il meccanismo di sviluppo dell'ipogenitalismo, è necessario sapere come funziona normalmente il sistema ormonale maschile. È composto da 2 parti: le gonadi (testicoli), che producono androgeni (testosterone, diidrotestosterone) e la ghiandola pituitaria, situata alla base del cervello. Produce ormoni gonadotropici: ormone follicolo-stimolante (FSH), ormone luteinizzante (LH) e prolattina. Gli androgeni influenzano anche la funzione della ghiandola pituitaria: meno ce ne sono, più gonadotropine vengono prodotte, e viceversa.
La classificazione della patologia si basa sui fattori causali alla base di essa. Tutti i tipi di ipogonadismo sono divisi in 2 grandi gruppi:
- Primario
- Secondario.
Ipogenitalismo primario (ipogonadismo)
Questo è l'ipogenitalismo testicolare (dal latino testiculos - testicoli), su cui si basa funzione diminuita direttamente le gonadi. A causa di questi disturbi si distinguono 2 tipi di ipogenitalismo:
- Congenito, derivante da varie anomalie e patologie genetiche: anarchismo (assenza di testicoli), ipoplasia (sottosviluppo), ermafroditismo maschile, anomalie dello sviluppo cromosomico (sindrome di Klinefelter, Noonan, Sherishevsky-Turner).
- Acquisita quando il bambino è nato normale, ma lo sviluppo delle gonadi è stato influenzato da vari fattori: traumi, tumori, infezioni, processi autoimmuni, fattori ambientali dannosi (radiazioni, sostanze chimiche). In questi casi, negli uomini si sviluppa l'ipogonadismo ipergonadotropo, quando la ghiandola pituitaria aumenta la stimolazione dei testicoli, aumentando la produzione di ormoni.
- In relazione all'età, sviluppandosi sullo sfondo di una diminuzione della funzione ormonale dei testicoli nell'andropausa, è normotropico, senza interruzione della funzione pituitaria.
Ipogonadismo secondario
Si tratta di ipogonadismo ipogonadotropo, non associato a patologia testicolare, si sviluppa a causa di un'insufficiente stimolazione della ghiandola pituitaria a causa di una carenza di ormoni gonadotropici. Inoltre è disponibile in 2 tipologie:
- Congenito, causato da malattie ereditarie:
- nanismo ipofisario – sottosviluppo generale dovuto alla ridotta funzionalità della ghiandola pituitaria;
- produzione insufficiente di ormone follicolo-stimolante (FSH);
- insufficienza della produzione dell’ormone luteinizzante (LH) – sindrome di Pasqualini;
- insufficienza ipofisi-surrene - sindrome di Meddock;
- tumore congenito della base del cervello - craniofaringeoma, che comprime la ghiandola pituitaria;
- anomalia del cervello con sottosviluppo della ghiandola pituitaria, disturbi della vista e dell'olfatto - sindrome di Kallmann;
- idiopatico, che si verifica quando la produzione dell’embrione di gonadotropina corionica umana (hCG) diminuisce a causa di vari fattori sfavorevoli, complicando la gravidanza.