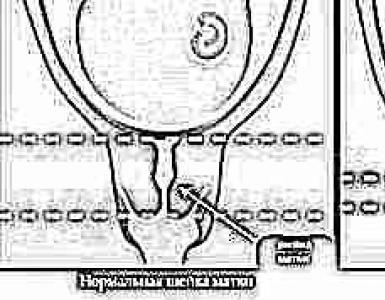
Viene presentato l'arco riflesso autonomo più semplice. Arco riflesso autonomo (vegetativo). Posizione dei gangli e struttura delle vie
Il sistema nervoso autonomo, come quello somatico, funziona secondo il principio della regolazione dei riflessi. Il substrato morfologico dei riflessi autonomi è un arco riflesso, la cui struttura differisce significativamente dalla struttura dell'arco riflesso di un riflesso somatico.
Consideriamo la struttura di un semplice arco riflesso autonomo di tre neuroni. Il primo collegamento dell'arco riflesso è un neurone sensibile (afferente), il cui corpo si trova nel ganglio spinale (per la divisione simpatica) o nel ganglio sensibile del nervo cranico (per la divisione parasimpatica). Si tratta di neuroni viscerosensibili, i cui processi periferici (dendriti) hanno terminazioni sensibili, viscerocettori, negli organi e nei tessuti. I processi centrali (assoni) nelle radici dorsali dei nervi spinali o nelle radici sensoriali dei nervi cranici sono diretti ai nuclei del midollo spinale o del cervello. Questa parte dell'arco riflesso del riflesso autonomo è simile all'arco riflesso somatico. Pertanto, i nodi sensibili sono nodi misti animale-vegetativi.
Il secondo collegamento dell'arco riflesso autonomo è efferente ed è rappresentato da due neuroni. A questo livello si possono tracciare le differenze tra archi somatici e autonomi. Il corpo del primo neurone efferente (o del secondo interneurone) dell'arco riflesso autonomo è localizzato nei nuclei autonomi, null. intermediolaterali, corna laterali del midollo spinale per l'arco simpatico o nei nuclei parasimpatici, null. parasimpatico sacrale, midollo spinale sacrale e nei nuclei parasimpatici del tronco encefalico per l'arco parasimpatico, in contrapposizione ai nuclei sensoriali del corno dorsale o del tronco cerebrale per l'arco somatico. Gli assoni di questi interneuroni si estendono oltre il sistema nervoso centrale come parte delle radici anteriori dei nervi spinali o nella porzione parasimpatica delle coppie III, VII, IX, X di nervi cranici e, separandosi dai nervi spinali o cranici, si avvicinano a uno dei i gangli autonomi. L'interneurone dell'arco somatico termina con una sinapsi sui nuclei motori delle corna anteriori o del tronco cerebrale, rimanendo all'interno del sistema nervoso centrale.
Il secondo neurone efferente (effettore) dell'arco autonomo si trova completamente all'esterno del sistema nervoso centrale. Il suo corpo giace in uno dei gangli autonomi, gangll. trunci simpatici, gangll. prevertebrali, gangli. terminali. Nell'arco somatico, il corpo del terzo neurone (effettore) si trova nei nuclei delle corna anteriori del midollo spinale.
La fibra del primo neurone efferente dell'arco riflesso autonomo è pregangliare. È ricoperto da una guaina mielinica ed è di colore bianco. La fibra del secondo neurone efferente è postgangliare. non ha guaina mielinica ed è di colore grigiastro. Pertanto, le caratteristiche principali dell'arco riflesso autonomo sono la natura a due neuroni della sua parte efferente e la posizione del terzo neurone (effettore) all'esterno del sistema nervoso centrale.
13.1. DISPOSIZIONI GENERALI
Il sistema nervoso autonomo può essere considerato come un complesso di strutture che costituiscono le parti periferiche e centrali del sistema nervoso, fornire la regolazione delle funzioni di organi e tessuti, volta a mantenere una relativa costanza dell'ambiente interno nel corpo (omeostasi). Inoltre, il sistema nervoso autonomo è coinvolto nell'implementazione di influenze trofiche-adattative, nonché in varie forme di attività fisica e mentale.
Le strutture del sistema nervoso autonomo che compongono il cervello e il midollo spinale costituiscono la sua sezione centrale, il resto è periferico. Nella sezione centrale è consuetudine distinguere le strutture vegetative soprasegmentali e segmentali. Inclusione soprasegmentale aree della corteccia cerebrale (localizzate principalmente mediobasale), nonché alcune formazioni del diencefalo, principalmente l'ipotalamo. Strutture segmentali della parte centrale del sistema nervoso autonomo localizzato nel tronco encefalico e nel midollo spinale. Nel sistema nervoso periferico la sua parte vegetativa è rappresentata da nodi, tronchi e plessi vegetativi, fibre afferenti ed efferenti, nonché cellule e fibre vegetative situate in strutture solitamente considerate animali (gangli spinali, tronchi nervosi, ecc.), sebbene in realtà abbiano una carattere misto.
Tra le formazioni vegetative soprasegmentali riveste particolare importanza la parte ipotalamica del diencefalo, la cui funzione è in gran parte controllata da altre strutture cerebrali, inclusa la corteccia cerebrale. L'ipotalamo garantisce l'integrazione delle funzioni dell'animale (somatiche) e del sistema nervoso autonomo filogeneticamente più antico.
Il sistema nervoso autonomo è anche conosciuto come autonomo per la sua certa, anche se relativa, autonomia, o viscerale a causa del fatto che attraverso di esso viene effettuata la regolazione delle funzioni degli organi interni.
13.2. STORIA DELLA PROBLEMATICA
Le prime informazioni sulle strutture e funzioni delle strutture vegetative sono associate al nome di Galeno (130 ca.-200 ca.), poiché fu lui a studiare i nervi cranici
hai descritto il nervo vago e il tronco borderline, che lui chiamava simpatico. Nel libro "Struttura del corpo umano" di A. Vesalius (1514-1564), pubblicato nel 1543, viene fornita un'immagine di queste formazioni e vengono descritti i gangli del tronco simpatico.
Nel 1732, J. Winslow (Winslow J., 1669-1760) identificò tre gruppi di nervi, i cui rami, esercitando un'influenza amichevole l'uno sull'altro (“simpatia”), si estendono agli organi interni. Il termine “sistema nervoso autonomo” per designare le strutture nervose che regolano la funzione degli organi interni fu introdotto nel 1807 dal medico tedesco I. Reill I. L'anatomista e fisiologo francese M.F. Bicha (Bicha M.F., 1771-1802) credeva che i nodi simpatici sparsi in diverse parti del corpo agiscano in modo indipendente (autonomo) e da ciascuno di essi escano rami che li collegano tra loro e assicurano la loro influenza sugli organi interni. Nel 1800 propose anche divisione del sistema nervoso in vegetativo (pianta) e animale (animale). Nel 1852, il fisiologo francese Claude Bernard (1813-1878) dimostrò che l'irritazione del tronco del nervo simpatico cervicale porta alla vasodilatazione, descrivendo così la funzione vasomotoria dei nervi simpatici. Ha anche stabilito che un'iniezione nella parte inferiore del quarto ventricolo del cervello ("iniezione di zucchero") modifica lo stato del metabolismo dei carboidrati nel corpo.
Alla fine del 19° secolo. Il fisiologo inglese J. Langley (Langley J.N., 1852-1925) coniò il termine "sistema nervoso autonomo" notando che la parola "autonomo" indica senza dubbio un grado di indipendenza dal sistema nervoso centrale maggiore di quanto non sia in realtà. Sulla base delle differenze morfologiche, nonché dei segni di antagonismo funzionale delle singole strutture vegetative, J. Langley ha identificato comprensivo E parasimpatico divisioni del sistema nervoso autonomo. Ha anche dimostrato che nel sistema nervoso centrale ci sono centri del sistema nervoso parasimpatico nel mesencefalo e nel midollo allungato, nonché nei segmenti sacrali del midollo spinale. Nel 1898, J. Langley stabilì nella parte periferica del sistema nervoso autonomo (nel percorso dalle strutture del sistema nervoso centrale all'organo di lavoro) la presenza di dispositivi sinaptici situati nei nodi vegetativi, in cui gli impulsi nervosi efferenti passano da neurone a neurone. Notò che la parte periferica del sistema nervoso autonomo contiene fibre nervose pregangliari e postgangliari e descrisse in modo abbastanza accurato la struttura generale del sistema nervoso autonomo (autonomo).
Nel 1901, T. Elliott suggerì la trasmissione chimica degli impulsi nervosi nei nodi vegetativi e nel 1921, nel processo di studi sperimentali, questa posizione fu confermata dal fisiologo austriaco O. Loewi (Loewi O., 1873-1961) e , gettò così le basi per la dottrina dei mediatori (neurotrasmettitori). Nel 1930, il fisiologo americano W. Cannone(Cannon W., 1871-1945), studiando il ruolo del fattore umorale e dei meccanismi autonomici nel mantenimento della relativa costanza dell'ambiente interno del corpo, coniato il termine"omeostasi" e nel 1939 stabilì che se in una serie funzionale di neuroni in uno degli anelli il movimento degli impulsi nervosi viene interrotto, la conseguente denervazione generale o parziale degli anelli successivi della catena provoca un aumento della sensibilità di tutti i recettori situati in loro all'azione eccitatoria o inibitoria
sostanze chimiche (compresi i farmaci) con proprietà simili ai corrispondenti mediatori (Legge di Cannon-Rosenbluth).
Un ruolo significativo nella comprensione delle funzioni del sistema nervoso autonomo fu svolto dal fisiologo tedesco E. Hering (Hering E., 1834-1918), che scoprì i riflessi sinocarotidei, e dal fisiologo domestico L.A. Orbeli (1882-1958), che creò la teoria dell'influenza adattativo-trofica del sistema nervoso simpatico. Molti neurologi clinici, compresi i nostri connazionali M.I., hanno contribuito all'espansione delle idee sulle manifestazioni cliniche del danno al sistema nervoso autonomo. Astvatsaturov, G.I. Markelov, N.M. Itsenko, I.I. Rusetsky, A.M. Grinstein, N.I. Grashchenkov, N.S. Četverikov, A.M. Wayne.
13.3. STRUTTURA E FUNZIONI DEL SISTEMA NERVOSO AUTONOMO
Tenendo conto delle peculiarità della struttura e della funzione della parte segmentale del sistema nervoso autonomo, si distingue principalmente divisioni simpatica e parasimpatica (Fig. 13.1). Il primo fornisce principalmente processi catabolici, il secondo - anabolici. Composto dalle divisioni simpatica e parasimpatica del sistema nervoso autonomo comprende sia strutture afferenti che efferenti, nonché strutture intercalari. Già sulla base di questi dati è possibile delineare uno schema per la costruzione di un riflesso autonomo.
13.3.1. Arco del riflesso autonomo (principi di costruzione)
La presenza di sezioni afferenti ed efferenti del sistema nervoso autonomo, nonché di formazioni associative (intercalari) tra loro, garantisce la formazione di riflessi autonomici, i cui archi sono chiusi a livello spinale o cerebrale. Loro collegamento afferente è rappresentato da recettori (principalmente chemocettori) situati in quasi tutti gli organi e tessuti, nonché da fibre vegetative che si estendono da essi - i dendriti dei primi neuroni autonomi sensibili, che assicurano la conduzione degli impulsi autonomi in direzione centripeta ai corpi di questi neuroni si trovano nella colonna vertebrale, nei gangli cerebrali o nei loro analoghi situati nei nervi cranici. Successivamente, gli impulsi autonomi, seguendo gli assoni dei primi neuroni sensoriali attraverso le radici spinali dorsali, entrano nel midollo spinale o nel cervello e terminano nei neuroni intercalari (associativi) che fanno parte dei centri autonomi segmentali del midollo spinale o del tronco encefalico. neuroni associativi, a loro volta presentano numerose connessioni intersegmentali verticali e orizzontali e sono sotto il controllo di strutture vegetative soprasegmentali.
Parte efferente dell'arco dei riflessi autonomi è costituito da fibre pregangliari, che sono assoni di cellule dei centri autonomi (nuclei) della parte segmentale del sistema nervoso centrale (tronco cerebrale, midollo spinale
Riso. 13.1.Sistema nervoso autonomo.
1 - corteccia cerebrale; 2 - ipotalamo; 3 - nodo ciliare; 4 - nodo pterigopalatino; 5 - nodi sottomandibolari e sublinguali; 6 - nodo auricolare; 7 - nodo simpatico cervicale superiore; 8 - grande nervo splancnico; 9 - nodo interno; 10 - plesso celiaco; 11 - nodi celiaci; 12 - piccolo interno
nervo; 13, 14 - plesso mesenterico superiore; 15 - plesso mesenterico inferiore; 16 - plesso aortico; 17 - nervo pelvico; 18 - plesso ipogastrico; 19 - muscolo ciliare, 20 - sfintere della pupilla; 21 - dilatatore della pupilla; 22 - ghiandola lacrimale; 23 - ghiandole della mucosa nasale; 24 - ghiandola sottomandibolare; 25 - ghiandola sublinguale; 26 - ghiandola parotide; 27 - cuore; 28 - ghiandola tiroidea; 29 - laringe; 30 - muscoli della trachea e dei bronchi; 31 - polmone; 32 - stomaco; 33 - fegato; 34 - pancreas; 35 - ghiandola surrenale; 36 - milza; 37 - rene; 38 - intestino crasso; 39 - intestino tenue; 40 - detrusore della vescica; 41 - sfintere della vescica; 42 - gonadi; 43 - genitali.
cervello), che lasciano il cervello come parte delle radici spinali anteriori e raggiungono alcuni gangli autonomici periferici. Qui gli impulsi vegetativi vengono trasmessi ai neuroni i cui corpi si trovano nei gangli e poi lungo le fibre postgangliari, che sono gli assoni di questi neuroni, fino agli organi e ai tessuti innervati.
13.3.2. Strutture afferenti del sistema nervoso autonomo
Il substrato morfologico della parte afferente della parte periferica del sistema nervoso autonomo non presenta differenze fondamentali rispetto alla parte afferente della parte periferica del sistema nervoso animale. I corpi dei primi neuroni sensoriali autonomi si trovano negli stessi gangli spinali o nei loro analoghi nei gangli dei nervi cranici, che contengono anche i primi neuroni delle vie sensoriali animali. Di conseguenza, questi nodi sono formazioni animale-vegetative (somato-vegetative), che possono essere considerate come uno dei fatti che indicano la delineazione poco chiara dei confini tra le strutture animali e autonome del sistema nervoso.
I corpi del secondo e dei successivi neuroni autonomici sensoriali si trovano nel midollo spinale o nel tronco encefalico; i loro processi hanno contatti con molte strutture del sistema nervoso centrale, in particolare con i nuclei del diencefalo, principalmente il talamo e l'ipotalamo, così come con altre parti del cervello incluse nel sistema limbico complesso reticolare. Nella parte afferente del sistema nervoso autonomo si può notare un'abbondanza di recettori (interorecettori, viscerorecettori) situati in quasi tutti gli organi e tessuti.
13.3.3. Strutture efferenti del sistema nervoso autonomo
Se la struttura della parte afferente del sistema nervoso autonomo e animale può essere molto simile, allora la parte efferente del sistema nervoso autonomo è caratterizzata da caratteristiche morfologiche molto significative, mentre non sono identiche nelle sue parti parasimpatica e simpatica .
13.3.3.1. La struttura della parte efferente della divisione parasimpatica del sistema nervoso autonomo
La divisione centrale del sistema nervoso parasimpatico è divisa in tre parti: mesencefalico, bulbare e sacrale.
Parte mesencefalica compongono le coppie nuclei parasimpatici di Yakubovich-Westphal-Edinger, legati al sistema dei nervi oculomotori. Parte periferica Divisione mesencefalica del sistema nervoso periferico è costituito da assoni di questo nucleo, costituente la porzione parasimpatica del nervo oculomotore, che penetra attraverso la fessura orbitaria superiore nella cavità orbitaria, con fibre parasimpatiche pregangliari incluse in essa portata situato nel tessuto dell'orbita nodo ciliare (ganglio ciliare), in cui gli impulsi nervosi passano da neurone a neurone. Le fibre parasimpatiche postgangliari che emergono da esso partecipano alla formazione dei nervi ciliari corti (nn. ciliares breves) e terminano nei muscoli lisci da essi innervati: nel muscolo che restringe la pupilla (m. sphincter pupille), e nel muscolo ciliare (m. ciliaris), riduzione di cui fornisce l'alloggio della lente.
A parte bulbare Il sistema nervoso parasimpatico comprende tre paia di nuclei parasimpatici: il salivare superiore, il salivare inferiore e il dorsale. Gli assoni delle cellule di questi nuclei costituiscono le porzioni parasimpatiche del nervo intermedio di Wriesberg (che corre in parte come parte del nervo facciale), nervi glossofaringei e vago. Queste strutture parasimpatiche di questi nervi cranici sono costituite da fibre pregangliari, che terminano nei nodi vegetativi. Nel sistema dei nervi intermedi e glossofaringei Questo pterigopalatino (g. pterigopalatum), orecchio (g. otico), linfonodi sublinguali e sottomandibolari(g. sublingualis E G. sottomandibolare). Originato da questi nodi parasimpatici postgangliare nervoso raggiungono le fibre innervato da essi ghiandola lacrimale, ghiandole salivari e ghiandole mucose della cavità nasale e orale.
Gli assoni del nucleo parasimpatico dorsale del nervo vago emergono dal midollo allungato nella sua composizione, lasciando, Così, la cavità cranica attraverso il foro giugulare. Successivamente terminano in numerosi nodi autonomi del sistema nervoso vago. Già a livello del foro giugulare, dove il due nodi di questo nervo (superiore e inferiore), parte delle fibre pregangliari termina in essi. Successivamente, le fibre postgangliari partono dal ganglio superiore, formandosi rami meningei, coinvolto nell'innervazione della dura madre, e ramo auricolare; parte dal ganglio inferiore del nervo vago ramo faringeo. Successivamente, altri nervi vengono separati dal tronco del nervo vago. fibre pregangliari che formano il nervo depressivo cardiaco e in parte il nervo laringeo ricorrente; nella cavità toracica originano dal nervo vago rami tracheali, bronchiali ed esofagei, nella cavità addominale - anteriore e posteriore gastrico e celiaco. Le fibre pregangliari che innervano gli organi interni terminano nei nodi periorgano parasimpatico e intraorgano (intramurali),
situato nelle pareti degli organi interni o in prossimità di essi. Fibre postgangliari che originano da questi nodi fornire innervazione parasimpatica degli organi toracici e addominali. L'eccitante influsso parasimpatico su questi organi ha un effetto più lento.
battito cardiaco lento, restringimento del lume bronchiale, aumento della peristalsi dell'esofago, dello stomaco e dell'intestino, aumento della secrezione di succo gastrico e duodenale, ecc.
Parte sacra il sistema nervoso parasimpatico costituisce accumuli di cellule parasimpatiche nella sostanza grigia dei segmenti S II - S IV del midollo spinale. Gli assoni di queste cellule lasciano il midollo spinale come parte delle radici anteriori, quindi passano lungo i rami anteriori dei nervi spinali sacrali e si separano da essi sotto forma nervi pudendi (nn.pudendi), che prendono parte alla formazione inferiore plesso ipogastrico E stanno finendo nell'intraorgano linfonodi parasimpatici del bacino. Gli organi in cui si trovano questi nodi sono innervati da fibre postgangliari che si estendono da essi.
13.3.3.2. La struttura della sezione efferente della divisione simpatica del sistema nervoso autonomo
La sezione centrale del sistema nervoso autonomo simpatico è rappresentata dalle cellule delle corna laterali del midollo spinale a livello dall'VIII segmento cervicale al III-IV lombare. Queste cellule autonome formano collettivamente il centro simpatico spinale, o colonna intermedia (autonomica).
Componenti del centro simpatico spinale Celle di Jacobson (piccolo, multipolare) associati ai centri vegetativi superiori, inclusi nel sistema del complesso limbico-reticolare, che, a loro volta, hanno connessioni con la corteccia cerebrale e sono influenzati dagli impulsi emanati dalla corteccia. Gli assoni delle cellule simpatiche di Jacobson emergono dal midollo spinale come parte delle radici spinali anteriori. Successivamente, passando attraverso il foro intervertebrale come parte dei nervi spinali, essi cadono nei loro rami bianchi di collegamento (rami communicantes albi). Ogni ramo di collegamento bianco entra in uno dei nodi paravertebrali (paravertebrali) che fanno parte del tronco simpatico borderline. Qui parte delle fibre del ramo di collegamento bianco termina e forma la sinapsi contatti con le cellule simpatiche di questi nodi, l'altra parte delle fibre passa attraverso il nodo paravertebrale in transito e raggiunge le cellule di altri nodi del tronco simpatico di confine o gangli simpatici prevertebrali (prevertebrali).
I nodi del tronco simpatico (nodi paravertebrali) si trovano in una catena su entrambi i lati della colonna vertebrale, con rami di collegamento internodali che passano tra di loro (rami comunicanti intergangliari), e così si formano tronchi simpatici di confine (trunci sympathici dexter et sinister), costituito da una catena di 17-22 nodi simpatici, tra i quali vi sono connessioni trasversali (tracti transversalis). I tronchi simpatici borderline si estendono dalla base del cranio al coccige e hanno 4 sezioni: cervicale, toracica, lombare e sacrale.
Alcune delle cellule private della guaina mielinica degli assoni situate nei nodi del confine del tronco simpatico formano rami di collegamento grigi (rami communicantes grisei) e quindi entrano nelle strutture del sistema nervoso periferico: come parte del ramo anteriore del nervo spinale, del plesso nervoso e dei nervi periferici, si avvicina a vari tessuti, fornendo la loro innervazione simpatica. Questa parte svolge, in particolare,
innervazione simpatica dei muscoli pilomotori, nonché delle ghiandole sudoripare e sebacee. Un'altra parte delle fibre postgangliari del tronco simpatico forma plessi che si diffondono lungo i vasi sanguigni. La terza parte delle fibre postgangliari, insieme alle fibre pregangliari che passano accanto ai gangli del tronco simpatico, formano i nervi simpatici, che vanno principalmente agli organi interni. Lungo il percorso, le fibre pregangliari incluse nella loro composizione terminano nei gangli simpatici prevertebrali, da cui partono anche le fibre postgangliari coinvolte nell'innervazione di organi e tessuti. Tronco simpatico cervicale:
1) Nodi simpatici cervicali - superiore, centrale e inferiore. Nodo cervicale superiore (gangl. cervicale superius) situato vicino all'osso occipitale a livello delle prime tre vertebre cervicali lungo la superficie dorsomediale dell'arteria carotide interna. Nodo cervicale medio (gangl. cervicale medio) instabile, localizzato a livello delle IV-VI vertebre cervicali, anteriormente all'arteria succlavia, medialmente alla 1a costa. Nodo cervicale inferiore (gangl. cervicale inferiore) nel 75-80% delle persone si fonde con il primo (meno spesso con il secondo) nodo toracico e se ne forma uno grande nodo cervicotoracico (gangl. cervicothoracicum), o così chiamato nodo stellare (gangl. stellatum).
A livello cervicale del midollo spinale non sono presenti corni laterali e cellule vegetative; pertanto le fibre pregangliari che vanno ai gangli cervicali sono assoni di cellule simpatiche, i cui corpi si trovano nei corni laterali delle quattro o cinque cellule toraciche superiori. segmenti; entrano nel nodo cervicotoracico (stellato). Alcuni di questi assoni terminano in questo nodo e gli impulsi nervosi che li percorrono vengono trasferiti qui al neurone successivo. L'altra parte passa attraverso il nodo del tronco simpatico in transito e gli impulsi che viaggiano lungo di essi vengono commutati al neurone simpatico successivo nel nodo simpatico medio-alto o cervicale superiore.
Le fibre postgangliari che si estendono dai nodi cervicali del tronco simpatico emettono rami che forniscono innervazione simpatica agli organi e ai tessuti del collo e della testa. Fibre postgangliari che originano dal ganglio cervicale superiore formano i plessi delle arterie carotidi, controllare il tono della parete vascolare di queste arterie e dei loro rami, nonché forniscono innervazione simpatica alle ghiandole sudoripare, al muscolo liscio che dilata la pupilla (m. dilatator pupillae), alla placca profonda del muscolo che solleva la palpebra superiore (lamina profunda m. levator palpebrae superioris) e al muscolo orbitale (m. orbitalis ). Dal plesso delle arterie carotidi partono anche rami coinvolti nell'innervazione ghiandole lacrimali e salivari, follicoli piliferi, arteria tiroidea, nonché quelle che innervano la laringe e la faringe, che sono coinvolte nella formazione del nervo cardiaco superiore, che fa parte del nervo cardiaco plesso.
Dagli assoni dei neuroni situati nel nodo simpatico cervicale medio, il nervo cardiaco medio, coinvolti nella formazione del plesso cardiaco.
Le fibre postgangliari derivanti dal ganglio simpatico cervicale inferiore o formate in connessione con la sua fusione con il ganglio toracico superiore del ganglio cervicotoracico o stellato formano il plesso simpatico dell'arteria vertebrale, conosciuto anche come nervo spinale. Questo plesso circonda l'arteria vertebrale, passa con essa attraverso il canale osseo formato dalle aperture nei processi trasversali delle vertebre C VI-C II ed entra nella cavità cranica attraverso il forame magno.
2) La parte toracica del tronco simpatico paravertebrale è composta da 9-12 nodi. Ognuno di essi ha un ramo di collegamento bianco. I rami comunicanti grigi vanno a tutti i nervi intercostali. I rami viscerali dei primi quattro nodi sono diretti al cuore, ai polmoni, alla pleura, dove, insieme ai rami del nervo vago, formano i corrispondenti plessi. Si formano rami da 6-9 nodi nervo splancnico maggiore, che passa nella cavità addominale ed entra nodo celiaco, fa parte del complesso del plesso celiaco (solare). (plesso celiaco). Si formano i rami degli ultimi 2-3 nodi del tronco simpatico nervo splancnico minore, alcuni dei cui rami si diramano nei plessi surrenali e renali.
3) La parte lombare del tronco simpatico paravertebrale è costituita da 2-7 nodi. I rami di collegamento bianchi si adattano solo ai primi 2-3 nodi. I rami comunicanti grigi si estendono da tutti i gangli simpatici lombari ai nervi spinali, e i tronchi viscerali formano il plesso aortico addominale.
4) Parte sacra Il tronco simpatico paravertebrale è costituito da quattro paia di gangli sacrali e da un paio di gangli coccigei. Tutti questi gangli sono collegati ai nervi spinali sacrali e danno rami agli organi e ai plessi neurovascolari del bacino.
Gangli simpatici prevertebrali caratterizzato da incostanza di forma e dimensione. I loro accumuli e le fibre vegetative associate formano i plessi. Topograficamente si distinguono i plessi prevertebrali del collo, le cavità toracica, addominale e pelvica. Nella cavità toracica i più grandi sono il plesso cardiaco, mentre nella cavità addominale i più grandi sono i plessi celiaco (solare), aortico, mesenterico e ipogastrico.
Dei nervi periferici, il nervo mediano e lo sciatico, nonché il nervo tibiale, sono i più ricchi di fibre simpatiche. Il loro danno, solitamente traumatico, è più spesso causato dal danno ad altri nervi periferici causalgia. Il dolore nella causalgia è bruciante, estremamente doloroso, difficile da localizzare e tende a diffondersi ben oltre la zona innervata dal nervo interessato, nella quale, tra l'altro, di solito si nota una grave iperpatia. I pazienti affetti da causalgia sono caratterizzati da un certo sollievo della condizione e da una diminuzione del dolore quando la zona di innervazione viene inumidita (sintomo dello straccio bagnato).
L'innervazione simpatica dei tessuti del tronco e degli arti, nonché degli organi interni, è di natura segmentale, in questo caso le zone dei segmenti non corrispondono ai metameri caratteristici dell'innervazione spinale somatica. I segmenti simpatici (cellule delle corna laterali del midollo spinale che costituiscono il centro simpatico spinale) da C VIII a Th III forniscono innervazione simpatica ai tessuti della testa e del collo, i segmenti Th IV - Th VII - tessuti del cingolo scapolare e braccio, segmenti Th VIII Th IX - il torso; i segmenti situati più in basso, che contengono le corna laterali, Th X - Th III, forniscono innervazione simpatica agli organi della cintura pelvica e delle gambe.
L'innervazione simpatica degli organi interni è fornita da fibre autonome collegate a determinati segmenti del midollo spinale. Il dolore derivante dal danno agli organi interni può irradiarsi alle aree dei dermatomeri corrispondenti a questi segmenti (Zone Zakharyin-Ged) . Tale dolore riferito, o iperestesia, si manifesta come riflesso viscerosensoriale (Fig. 13.2).

Riso. 13.2.Le zone di dolore riflesso (zone Zakharyin-Ged) sul busto nelle malattie degli organi interni sono un riflesso viscerosensoriale.
Le cellule vegetative sono di piccole dimensioni, le loro fibre sono prive di polpa o hanno una guaina mielinica molto sottile e appartengono ai gruppi B e C. A questo proposito, la velocità di trasmissione degli impulsi nervosi nelle fibre vegetative è relativamente bassa.
13.3.4. Divisione metasimpatica del sistema nervoso autonomo
Oltre alle divisioni parasimpatica e simpatica, i fisiologi distinguono la divisione metasimpatica del sistema nervoso autonomo. Con questo termine si indica un complesso di formazioni microgangliari situate nelle pareti degli organi interni che hanno attività motoria (cuore, intestino, ureteri, ecc.) e ne garantiscono l'autonomia. La funzione dei gangli nervosi è quella di trasmettere influenze centrali (simpatiche, parasimpatiche) ai tessuti e, inoltre, garantire l'integrazione delle informazioni che arrivano lungo gli archi riflessi locali. Le strutture metasimpatiche sono formazioni indipendenti in grado di funzionare con completo decentramento. Diversi (5-7) nodi vicini ad essi correlati sono combinati in un unico modulo funzionale, le cui unità principali sono cellule oscillatrici che garantiscono l'autonomia del sistema, interneuroni, motoneuroni e cellule sensoriali. I singoli moduli funzionali formano un plesso, grazie al quale, ad esempio, si organizza un'onda peristaltica nell'intestino.
Le funzioni della divisione metasimpatica del sistema nervoso autonomo non dipendono direttamente dall'attività del sistema simpatico o parasimpatico
sistemi nervosi, ma possono essere modificati sotto la loro influenza. Ad esempio, l'attivazione dell'influenza parasimpatica aumenta la motilità intestinale e l'influenza simpatica la indebolisce.
13.3.5. Strutture vegetative soprasegmentali
A rigor di termini, l'irritazione di qualsiasi parte del cervello è accompagnata da una sorta di risposta vegetativa, ma nelle sue strutture sopratentoriali non esistono territori compatti che possano essere classificati come formazioni vegetative specializzate. Tuttavia, ci sono strutture vegetative soprasegmentali del cervello e del diencefalo, avendo l'influenza più significativa, principalmente integrativa, sullo stato di innervazione vegetativa di organi e tessuti.
Queste strutture comprendono il complesso limbico-reticolare, in primis l'ipotalamo, nel quale è consuetudine distinguere la parte anteriore - trofotropico e posteriore - ergotropico dipartimenti. Strutture del complesso limbico-reticolare hanno numerose connessioni dirette e di feedback con la nuova corteccia (neocorteccia) degli emisferi cerebrali, che controlla e in una certa misura corregge il loro stato funzionale.
Ipotalamo e altre parti del complesso limbico-reticolare avere un effetto regolatore globale sulle parti segmentali del sistema nervoso autonomo, creare un relativo equilibrio tra le attività delle strutture simpatiche e parasimpatiche, finalizzato al mantenimento di uno stato di omeostasi nell'organismo. Inoltre, la regione ipotalamica del cervello, il complesso dell'amigdala, la vecchia e antica corteccia delle regioni mediobasi degli emisferi cerebrali, il giro dell'ippocampo e altre parti del complesso limbico-reticolare effettuare l'integrazione tra le strutture autonomiche, il sistema endocrino e la sfera emotiva, influenzare la formazione di motivazioni, emozioni, memoria e comportamento.
La patologia delle formazioni soprasegmentali può portare a reazioni multisistemiche, in cui i disturbi autonomici sono solo una componente di un quadro clinico complesso.
13.3.6. Mediatori e loro influenza sullo stato delle strutture vegetative
La conduzione degli impulsi attraverso gli apparati sinaptici sia del sistema nervoso centrale che di quello periferico avviene grazie a mediatori, o neurotrasmettitori. Nel sistema nervoso centrale i mediatori sono numerosi e la loro natura non è stata studiata in tutte le connessioni sinaptiche. Sono stati meglio studiati i mediatori delle strutture nervose periferiche, in particolare quelle legate al sistema nervoso autonomo. Va inoltre notato che nella parte afferente (centripeta, sensibile) del sistema nervoso periferico, che è costituita principalmente da cellule pseudounipolari con i loro processi, non sono presenti apparati sinaptici. Nelle strutture efferenti (Tabella 13.1) della parte animale (somatica) del sistema nervoso periferico, sono presenti solo strutture nervose

Schema 13.1.Apparato simpatico e mediatori del sistema nervoso periferico SNC - sistema nervoso centrale; PNS - sistema nervoso periferico; PS - strutture parasimpatiche del sistema nervoso centrale; C - strutture simpatiche del sistema nervoso centrale; a - fibra motoria somatica; b - fibre autonome pregangliari; c - fibre autonome postgangliari; CERCHIO - dispositivi sinaptici; mediatori: ACh - acetilcolina; NA – noradrenalina.
sinapsi muscolari. Il mediatore che assicura la conduzione degli impulsi nervosi attraverso queste sinapsi è l'acetilcolina-H (ACh-H), sintetizzata nei motoneuroni periferici situati nelle strutture del sistema nervoso centrale, e proveniente da lì lungo i loro assoni con una corrente asso nelle vescicole sinaptiche situato vicino alla membrana presinaptica.
La parte periferica efferente del sistema nervoso autonomo è costituita da fibre pregangliari che emergono dal sistema nervoso centrale (tronco encefalico, midollo spinale), nonché da gangli autonomi, in cui gli impulsi vengono commutati attraverso l'apparato sinaptico dalle fibre pregangliari alle cellule situate nel gangli. Successivamente, gli impulsi lungo gli assoni che si estendono da queste cellule (fibre postgangliari) raggiungono una sinapsi, che assicura la commutazione dell'impulso da queste fibre al tessuto innervato.
Così, tutti gli impulsi vegetativi nel percorso dal sistema nervoso centrale al tessuto innervato passano due volte attraverso l'apparato sinaptico. La prima delle sinapsi si trova nel ganglio parasimpatico o simpatico; la commutazione dell'impulso qui in entrambi i casi avviene tramite lo stesso trasmettitore della sinapsi neuromuscolare animale - acetilcolina-N (ACH-N). Le seconde sinapsi, parasimpatiche e simpatiche, in cui gli impulsi passano dalla fibra postgangliare alla struttura innervata, non sono identiche nel trasmettitore rilasciato. Per il reparto parasimpatico è l'acetilcolina-M (AC-M), per il reparto simpatico è principalmente la norepinefrina (NA). Ciò è di notevole importanza, poiché con l'aiuto di alcuni farmaci è possibile influenzare la conduzione degli impulsi nervosi nella zona della loro transizione attraverso la sinapsi. Tali farmaci comprendono i colinomimetici H e M e gli anticolinergici H e M, nonché gli agonisti adrenergici e i bloccanti adrenergici. Quando si prescrivono questi farmaci, è necessario tenere conto del loro effetto sulle strutture sinaptiche e prevedere quale tipo di reazione ci si dovrebbe aspettare alla somministrazione di ciascuno di essi.
L'effetto di un farmaco può influenzare la funzione delle sinapsi appartenenti a diverse parti del sistema nervoso se la neurotrasmissione in esse è fornita da un mediatore identico o simile nella struttura chimica. Pertanto, l'introduzione di bloccanti gangliari, che sono anticolinergici H, ha un effetto bloccante sulla conduzione degli impulsi dalla fibra pregangliare alla cellula situata nel ganglio sia nei gangli simpatici che parasimpatici e può anche sopprimere la conduzione dei nervi impulsi attraverso le sinapsi neuromuscolari della parte animale del sistema nervoso periferico.
In alcuni casi è possibile influenzare la conduzione degli impulsi attraverso una sinapsi con mezzi che influenzano diversamente la conduttività degli apparati sinaptici. Pertanto, l'effetto colinomimetico viene esercitato non solo dall'uso di colinomimetici, in particolare dall'acetilcolina, che tra l'altro si disintegra rapidamente e viene quindi utilizzata raramente nella pratica clinica, ma anche dai farmaci anticolinesterasici del gruppo degli inibitori della colinesterasi (prozerina, galantamina, calemina, ecc. ), che porta alla protezione dalla rapida distruzione delle molecole ACh che entrano nella fessura sinaptica.
Le strutture del sistema nervoso autonomo sono caratterizzate dalla capacità di rispondere attivamente a molti stimoli chimici e umorali. Questa circostanza determina la labilità delle funzioni vegetative con i minimi cambiamenti nella composizione chimica dei tessuti, in particolare del sangue, sotto l'influenza di cambiamenti nelle influenze endogene ed esogene. Permette inoltre di influenzare attivamente l'equilibrio autonomo introducendo nell'organismo alcuni agenti farmacologici che migliorano o bloccano la conduzione degli impulsi autonomici attraverso l'apparato sinaptico.
Il sistema nervoso autonomo influenza la vitalità del corpo (Tabella 13.1). Regola lo stato dei sistemi cardiovascolare, respiratorio, digestivo, genito-urinario ed endocrino, dei mezzi fluidi e della muscolatura liscia. Allo stesso tempo, il sistema vegetativo svolge una funzione trofica-adattativa, regola le risorse energetiche del corpo, fornendo Così tutti i tipi di attività fisiche e mentali, preparare organi e tessuti, compresi il tessuto nervoso e i muscoli striati, per il livello ottimale della loro attività e il corretto svolgimento delle loro funzioni inerenti.
Tabella 13.1.Funzioni delle divisioni simpatica e parasimpatica del sistema nervoso autonomo

Fine del tavolo. 13-1

*Per la maggior parte delle ghiandole sudoripare, di alcuni vasi sanguigni e dei muscoli scheletrici, il trasmettitore simpatico è l'acetilcolina. La midollare del surrene è innervata dai neuroni simpatici colinergici.
Durante i periodi di pericolo e di lavoro intenso, il sistema nervoso autonomo è chiamato a soddisfare i crescenti bisogni energetici dell'organismo e lo fa aumentando l'attività dei processi metabolici, aumentando la ventilazione polmonare, trasferendo il sistema cardiovascolare e respiratorio ad una modalità più intensa , modificando l'equilibrio ormonale, ecc.
13.3.7. Studio delle funzioni autonome
Le informazioni sui disturbi autonomici e sulla loro localizzazione possono aiutare a risolvere il problema della natura e della posizione del processo patologico. A volte l’identificazione dei segni di squilibrio autonomo è di particolare importanza.
I cambiamenti nelle funzioni dell'ipotalamo e di altre strutture soprasegmentali del sistema nervoso autonomo portano a disturbi autonomici generalizzati. Il danno ai nuclei autonomi nel tronco encefalico e nel midollo spinale, nonché alle parti periferiche del sistema nervoso autonomo, è solitamente accompagnato dallo sviluppo di disturbi autonomici segmentali in una parte più o meno limitata del corpo.
Quando si esamina il sistema nervoso autonomo, è necessario prestare attenzione al fisico del paziente, alle condizioni della sua pelle (iperemia, pallore, sudorazione, untuosità, ipercheratosi, ecc.), alle sue appendici (calvizie, ingrigimento; fragilità, opacità, ispessimento, deformazione di chiodi); la gravità dello strato di grasso sottocutaneo, la sua distribuzione; condizione delle pupille (deformazione, diametro); lacrimazione; salivazione; funzionalità degli organi pelvici (urgenza urinaria, incontinenza urinaria, ritenzione urinaria, diarrea, stipsi). È necessario farsi un’idea del carattere del paziente, del suo umore prevalente, del benessere, delle prestazioni, del grado di emotività, della capacità di adattamento ai cambiamenti della temperatura esterna.
tour. È necessario ottenere informazioni sullo stato somatico del paziente (frequenza, labilità, ritmo del polso, pressione sanguigna, mal di testa, sua natura, storia di attacchi di emicrania, funzioni dell'apparato respiratorio, digestivo e altri), sullo stato del sistema endocrino, risultati termometrici, parametri di laboratorio . Prestare attenzione alla presenza di manifestazioni allergiche nel paziente (orticaria, asma bronchiale, angioedema, prurito essenziale, ecc.), angiotrofoneurosi, acroangiopatia, simpatalgia, manifestazioni di “mal di mare” durante l'utilizzo dei trasporti, “malattia dell'orso”.
Un esame neurologico può rivelare anisocoria, dilatazione o costrizione delle pupille che non corrispondono all'illuminazione disponibile, alterata reazione delle pupille alla luce, convergenza, accomodazione, iperreflessia tendinea totale con possibile espansione delle zone riflessogene, reazione motoria generale, alterazioni della dermografismo locale e riflesso.
Dermografismo locale è causata da una leggera irritazione della pelle con un oggetto contundente, ad esempio il manico di un martello, o l'estremità arrotondata di una bacchetta di vetro. Normalmente, con lieve irritazione della pelle, dopo pochi secondi appare una striscia bianca. Se l'irritazione cutanea è più intensa, la striscia risultante sulla pelle sarà rossa. Nel primo caso il dermografismo locale è bianco, nel secondo il dermografismo locale è rosso.
Se sia l'irritazione cutanea debole che quella più intensa provocano la comparsa di dermografismo bianco locale, si può parlare di aumento del tono vascolare della pelle. Se, anche con irritazioni minime della linea della pelle, si verifica un dermografismo rosso locale, ma non è possibile ottenere un dermografismo bianco, ciò indica una diminuzione del tono dei vasi cutanei, principalmente precapillari e capillari. Con una pronunciata diminuzione del tono, l'irritazione delle striature della pelle non solo porta alla comparsa di dermografismo rosso locale, ma anche alla penetrazione del plasma attraverso le pareti dei vasi sanguigni. Quindi è possibile la comparsa di dermografismo edematoso, orticarioide o elevato (dermografismo elevato).
Dermografismo riflesso o doloroso causato dall'irritazione della pelle con la punta di un ago o di uno spillo. Il suo arco riflesso si chiude nell'apparato segmentale del midollo spinale. In risposta alla stimolazione dolorosa, normalmente appare sulla pelle una striscia rossa larga 1-2 mm con stretti bordi bianchi, che dura diversi minuti.
Se il midollo spinale è danneggiato, nelle aree della pelle, la cui innervazione autonomica dovrebbe essere fornita dai segmenti interessati, e nelle parti inferiori del corpo, non vi è dermografismo riflesso. Questa circostanza può aiutare a chiarire il limite superiore del focus patologico nel midollo spinale. Il dermografismo riflesso scompare nelle aree innervate dalle strutture interessate del sistema nervoso periferico.
La condizione può anche avere un certo valore diagnostico topico riflesso pilomotorio (muscolo-capelli). Può essere causata da un'irritazione dolorosa o da freddo della pelle del muscolo trapezio (riflesso pilomotore superiore) o della regione glutea (riflesso pilomotore inferiore). La risposta in questo caso è la comparsa di una reazione pilomotoria diffusa sotto forma di “pelle d'oca” sulla metà corrispondente del corpo. La velocità e l'intensità della reazione indicano il grado
eccitabilità della divisione simpatica del sistema nervoso autonomo. L'arco del riflesso pilomotore si chiude nelle corna laterali del midollo spinale. Con lesioni trasversali del midollo spinale, che causano il riflesso pilomotore superiore, si può notare che la reazione pilomotoria si osserva non al di sotto del livello del dermatomero corrispondente al polo superiore del focus patologico. Quando viene evocato il riflesso pilomotorio inferiore, appare la pelle d'oca nella parte inferiore del corpo, che si estende verso l'alto fino al polo inferiore del focolaio patologico nel midollo spinale.
Va tenuto presente che i risultati dello studio del dermografismo riflesso e dei riflessi pilomotori forniscono solo informazioni indicative sull'argomento del focus patologico nel midollo spinale. Il chiarimento della localizzazione del focus patologico può richiedere un esame neurologico più completo e spesso metodi di esame aggiuntivi (mielografia, scansione MRI).
L'identificazione dei disturbi locali della sudorazione può essere di una certa importanza per la diagnosi topica. A questo scopo viene talvolta utilizzato l'amido di iodio. Prova di minore. Il corpo del paziente viene lubrificato con una soluzione di iodio in olio di ricino e alcool (iodi puri 16,0; olei risini 100,0; spiriti aetylici 900,0). Dopo che la pelle si è asciugata, viene cosparsa di amido. Quindi viene utilizzato uno dei metodi, che di solito provoca un aumento della sudorazione, mentre le zone sudate della pelle si scuriscono, poiché il sudore che appare favorisce la reazione dell'amido con lo iodio. Per provocare la sudorazione vengono utilizzati tre indicatori che influenzano diverse parti del sistema nervoso autonomo: diverse parti della parte efferente dell'arco riflesso della sudorazione. L'assunzione di 1 g di aspirina provoca un aumento della sudorazione, provocando la stimolazione del centro del sudore a livello dell'ipotalamo. Il riscaldamento del paziente in un bagno leggero colpisce principalmente i centri di sudorazione spinale. La somministrazione sottocutanea di 1 ml di una soluzione all'1% di pilocarpina provoca sudorazione, stimolando le terminazioni periferiche delle fibre autonome postgangliari situate nelle ghiandole sudoripare stesse.
Per determinare il grado di eccitabilità dell'apparato sinaptico neuromuscolare nel cuore si possono eseguire test ortostatici e clinostatici. Riflesso ortostatico si verifica quando il soggetto si sposta dalla posizione orizzontale a quella verticale. Prima del test ed entro il primo minuto dopo che il paziente si è spostato in posizione verticale, viene misurata la sua frequenza cardiaca. Normalmente, la frequenza cardiaca aumenta di 10-12 battiti al minuto. Test clinostatico controllato quando il paziente si sposta dalla posizione verticale a quella orizzontale. Il polso viene misurato anche prima del test e durante il primo minuto dopo che il paziente ha assunto una posizione orizzontale. Normalmente, la frequenza cardiaca rallenta di 10-12 battiti al minuto.
Test di Lewis (triade) - un complesso di reazioni vascolari che si sviluppano in sequenza all'iniezione intradermica di due gocce di una soluzione acidificata di istamina allo 0,01%. Nel sito di iniezione si verificano normalmente le seguenti reazioni: 1) comparsa di un punto rosso (eritema limitato) dovuto alla dilatazione locale dei capillari; 2) presto appare sopra una papula bianca (vescica), che si forma a causa dell'aumentata permeabilità dei vasi sanguigni della pelle; 3) l'iperemia cutanea si sviluppa attorno alla papula a causa dell'espansione delle arteriole. La diffusione dell'eritema oltre la papula può essere assente in caso di denervazione cutanea, mentre nei primi giorni successivi alla rottura del nervo periferico può conservarsi e scomparire nel tempo.
il fenomeno dei cambiamenti degenerativi nel nervo. L'anello rosso esterno che circonda la papula è solitamente assente nella sindrome di Riley-Day (disautonomia familiare). Il test può essere utilizzato anche per determinare la permeabilità vascolare e identificare le asimmetrie vegetative. È stata descritta dal cardiologo inglese Th. Lewis (1871-1945).
Durante l'esame clinico dei pazienti possono essere utilizzati altri metodi di studio del sistema nervoso autonomo, compreso lo studio della temperatura cutanea, la sensibilità della pelle alle radiazioni ultraviolette, l'idrofilicità della pelle, test farmacologici cutanei con farmaci come adrenalina, acetilcolina e alcuni altri farmaci vegetotropici , lo studio della resistenza elettrodermica, Riflesso oculare Danini-Aschner, capillaroscopia, pletismografia, riflessi del plesso autonomo (cervicale, epigastrico), ecc. La metodologia per la loro attuazione è descritta in manuali speciali e di riferimento.
Lo studio dello stato delle funzioni autonomiche può fornire importanti informazioni sulla presenza di una lesione funzionale o organica del sistema nervoso in un paziente, spesso aiutando a risolvere il problema della diagnosi topica e nosologica.
L'identificazione di asimmetrie autonome che vanno oltre le fluttuazioni fisiologiche può essere considerata un segno di patologia diencefalica. Cambiamenti locali nell'innervazione autonomica possono contribuire alla diagnosi topica di alcune malattie del midollo spinale e del sistema nervoso periferico. Dolore e disturbi vegetativi nelle zone Zakharyin-Ged, che si riflettono nella natura, possono indicare la patologia dell'uno o dell'altro organo interno. Segni di maggiore eccitabilità del sistema nervoso autonomo e labilità autonomica possono essere una conferma oggettiva della presenza di nevrosi o di una condizione simile alla nevrosi nel paziente. La loro identificazione a volte gioca un ruolo molto importante nella selezione professionale delle persone da lavorare in determinate specialità.
I risultati dello studio dello stato del sistema nervoso autonomo consentono in una certa misura di giudicare lo stato mentale di una persona, principalmente la sua sfera emotiva. Tale ricerca è alla base della disciplina che unisce fisiologia e psicologia ed è nota come psicofisiologia, confermando la relazione tra l'attività mentale e lo stato del sistema nervoso autonomo.
13.3.8. Alcuni fenomeni clinici dipendenti dallo stato delle strutture centrali e periferiche del sistema nervoso autonomo
Le funzioni di tutti gli organi e tessuti e, di conseguenza, dei sistemi cardiovascolare, respiratorio, genito-urinario, del tratto digestivo e degli organi di senso dipendono dallo stato del sistema nervoso autonomo. Influisce anche sulla funzionalità del sistema muscolo-scheletrico, regola i processi metabolici, garantendo la relativa costanza dell'ambiente interno del corpo e la sua vitalità. L'irritazione o l'inibizione delle funzioni delle singole strutture autonomiche porta all'autonomia
squilibrio, che in un modo o nell’altro influisce sulla condizione di una persona, sulla sua salute e sulla qualità della sua vita. A questo proposito, vale solo la pena sottolineare l'eccezionale diversità delle manifestazioni cliniche causate dalla disfunzione autonomica e attirare l'attenzione sul fatto che i rappresentanti di quasi tutte le discipline cliniche sono preoccupati per i problemi che ne derivano.
Successivamente abbiamo l'opportunità di soffermarci solo su alcuni fenomeni clinici che dipendono dallo stato del sistema nervoso autonomo, con cui un neurologo deve confrontarsi nel lavoro quotidiano (vedi anche Capitoli 22, 30, 31).
13.3.9. Disfunzione autonomica acuta, manifestata dall'estinzione delle reazioni autonomiche
Lo squilibrio autonomo è solitamente accompagnato da manifestazioni cliniche, la cui natura dipende dalle sue caratteristiche. La disfunzione autonomica acuta (pandisautonomia) dovuta all'inibizione delle funzioni autonomiche è causata da una violazione acuta della regolazione autonomica, manifestata totalmente, in tutti i tessuti e organi. Durante il periodo di questo fallimento multisistemico, che di solito è associato a disturbi immunitari nelle fibre mieliniche periferiche, immobilità e areflessia delle pupille, si verificano secchezza delle mucose, ipotensione ortostatica, rallentamento della frequenza cardiaca, motilità intestinale interrotta e ipotensione della vescica. . Le funzioni mentali, la condizione dei muscoli, compresi i muscoli oculomotori, la coordinazione dei movimenti e la sensibilità rimangono intatte. Potrebbe verificarsi un cambiamento nella curva degli zuccheri a seconda del tipo di diabete e un aumento del contenuto proteico nel liquido cerebrospinale. La disfunzione autonomica acuta può regredire gradualmente dopo un certo tempo e nella maggior parte dei casi si verifica il recupero.
13.3.10. Disfunzione autonomica cronica
La disfunzione autonomica cronica si verifica durante periodi prolungati di riposo a letto o in condizioni di assenza di gravità. Si manifesta principalmente come vertigini e disturbi della coordinazione che, una volta tornati alla normalità, diminuiscono gradualmente nel corso di diversi giorni. La violazione delle funzioni autonomiche può essere causata da un sovradosaggio di alcuni farmaci. Pertanto, un sovradosaggio di farmaci antipertensivi porta a ipotensione ortostatica; quando si usano farmaci che influenzano la termoregolazione, si verificano cambiamenti nelle reazioni vasomotorie e nella sudorazione.
Alcune malattie possono causare disturbi autonomici secondari. Pertanto, il diabete mellito e l'amiloidosi sono caratterizzati da manifestazioni di neuropatia, in cui sono possibili grave ipotensione ortostatica, cambiamenti nelle reazioni pupillari, impotenza e disfunzione della vescica. Con il tetano si verificano ipertensione arteriosa, tachicardia e iperidrosi.
13.3.11. Disturbi della termoregolazione
La termoregolazione può essere rappresentata come un sistema di autogoverno cibernetico, mentre il centro termoregolatore, che fornisce un insieme di reazioni fisiologiche del corpo volte a mantenere una relativa costanza della temperatura corporea, è localizzato nell'ipotalamo e nelle aree adiacenti del diencefalo. Le informazioni gli fluiscono dai termorecettori situati in vari organi e tessuti. Il centro di termoregolazione, a sua volta, regola i processi di produzione e trasferimento di calore nel corpo attraverso connessioni nervose, ormoni e altre sostanze biologicamente attive. In caso di disturbi della termoregolazione (negli esperimenti sugli animali, quando il tronco encefalico viene reciso), la temperatura corporea diventa eccessivamente dipendente dalla temperatura ambiente (poichilotermia).
Lo stato della temperatura corporea è influenzato dai cambiamenti nella produzione e nel trasferimento di calore per vari motivi. Se la temperatura corporea sale a 39°C, i pazienti di solito avvertono malessere, sonnolenza, debolezza, mal di testa e dolori muscolari. A temperature superiori a 41,1°C, i bambini spesso soffrono di convulsioni. Se la temperatura sale a 42,2°C o più, possono verificarsi cambiamenti irreversibili nel tessuto cerebrale, apparentemente dovuti alla denaturazione delle proteine. Le temperature superiori a 45,6°C sono incompatibili con la vita. Quando la temperatura scende a 32,8 °C, la coscienza viene compromessa, a 28,5 °C inizia la fibrillazione atriale e un'ipotermia ancora maggiore provoca la fibrillazione dei ventricoli del cuore.
Quando la funzione del centro termoregolatore nell'area preottica dell'ipotalamo è compromessa (disturbi vascolari, più spesso emorragie, encefaliti, tumori), ipertermia centrale endogena. È caratterizzato da cambiamenti nelle fluttuazioni giornaliere della temperatura corporea, cessazione della sudorazione, mancanza di risposta all'assunzione di farmaci antipiretici, alterazione della termoregolazione, in particolare dalla gravità della diminuzione della temperatura corporea in risposta al suo raffreddamento.
Oltre all'ipertermia causata dalla disfunzione del centro termoregolatore, aumento della produzione di calore può essere associato ad altri motivi. Lei possibile, in particolare, con tireotossicosi (la temperatura corporea può essere 0,5-1,1? C più alta del normale), aumento dell'attivazione della midollare del surrene, delle mestruazioni, della menopausa e altre condizioni accompagnate da squilibrio endocrino. L’ipertermia può anche essere causata da uno sforzo fisico estremo. Ad esempio, quando si corre una maratona, la temperatura corporea a volte sale fino a 39-41 °C. Motivo l’ipertermia può anche provocare una diminuzione del trasferimento di calore. A causa di ciò l'ipertermia è possibile con assenza congenita di ghiandole sudoripare, ittiosi, ustioni cutanee diffuse, nonché assunzione di farmaci che riducono la sudorazione (Anticolinergici M, inibitori MAO, fenotiazine, anfetamine, LSD, alcuni ormoni, in particolare progesterone, nucleotidi sintetici).
Gli agenti infettivi sono la causa esogena più comune di ipertermia. (batteri e loro endotossine, virus, spirochete, lieviti). Si ritiene che tutti i pirogeni esogeni influenzino le strutture termoregolatrici attraverso una sostanza intermedia - pirogeni endogeni (PE), identico all'interleuchina-1, che è prodotto da monociti e macrofagi.
Pirogeni endogeni nell'ipotalamo stimola la sintesi delle prostaglandine E, che modificano i meccanismi di produzione e trasferimento di calore migliorando la sintesi dell'adenosina monofosfato ciclico. Pirogeni endogeni, contenuto negli astrociti del cervello, può essere rilasciato durante un'emorragia cerebrale, una lesione cerebrale traumatica, causando un aumento della temperatura corporea, questo potrebbe attivare i neuroni responsabili del sonno a onde lente. Quest'ultima circostanza spiega la letargia e la sonnolenza durante l'ipertermia, che può essere considerata una delle reazioni protettive. Per processi infettivi o infiammazioni acute l’ipertermia gioca un ruolo importante nello sviluppo delle risposte immunitarie, che può essere protettivo, ma talvolta portare anche ad un aumento delle manifestazioni patologiche.
Ipertermia permanente non infettiva (febbre psicogena, ipertermia abituale) - febbre lieve permanente (37-38°C) per diverse settimane, meno spesso - diversi mesi e persino anni. La temperatura aumenta in modo monotono e non ha un ritmo circadiano, è accompagnata da una diminuzione o cessazione della sudorazione e dalla mancanza di risposta ai farmaci antipiretici (amidopirina, ecc.), violazione dell'adattamento al raffreddamento esterno. Caratteristica tolleranza soddisfacente all’ipertermia, mantenimento della capacità lavorativa. L'ipertermia permanente non infettiva si verifica più spesso nei bambini e nelle giovani donne durante periodi di stress emotivo e solitamente considerato come uno dei segni della sindrome da distonia autonomica. Tuttavia, soprattutto nelle persone anziane, può anche essere conseguenza di danni organici all'ipotalamo (tumore, disturbi vascolari, soprattutto emorragia, encefalite). Apparentemente si può considerare una variante della febbre psicogena Sindrome di Hines-Bennick (descritto da Hines-Bannick M.), derivante da uno squilibrio vegetativo, che si manifesta con debolezza generale (astenia), ipertermia permanente, grave iperidrosi e pelle d'oca. Può essere innescato da un trauma mentale.
Crisi termiche (ipertermia parossistica non infettiva) - improvvisi aumenti della temperatura fino a 39-41°C, accompagnati da uno stato di brivido, sensazione di tensione interna, iperemia facciale, tachicardia. La temperatura elevata persiste per diverse ore, dopo di che di solito si verifica una diminuzione litica, accompagnata da debolezza generale e debolezza, notate per diverse ore. Le crisi possono verificarsi in un contesto di temperatura corporea normale o di febbricola prolungata (ipertermia parossistica permanente). Con loro, i cambiamenti nel sangue, in particolare nella formula dei leucociti, sono insoliti. Le crisi termiche sono una delle possibili manifestazioni della distonia vegetativa e della disfunzione del centro termoregolatore, parte delle strutture ipotalamiche.
Ipertermia maligna - un gruppo di condizioni ereditarie caratterizzate da un forte aumento della temperatura corporea a 39-42 °C in risposta alla somministrazione di anestetici per inalazione, nonché di miorilassanti, in particolare ditilina, allo stesso tempo vi è un rilassamento muscolare insufficiente, la comparsa di fascicolazioni in risposta alla somministrazione di ditilina. Il tono dei muscoli masticatori spesso aumenta, si creano difficoltà per l’intubazione, che può essere un motivo per aumentare la dose di un miorilassante e (o) anestetico, porta allo sviluppo di tachicardia e nel 75% dei casi a rigidità muscolare generalizzata (forma rigida di reazione). In questo contesto, si può notare attività elevata
creatinfosfochinasi (CPK) E mioglobinuria, si sviluppano gravi sintomi respiratori e metabolici acidosi e iperkaliemia possono verificarsi fibrillazione ventricolare, diminuzione della pressione sanguigna, appare cianosi del marmo, sorge minaccia di morte.
Il rischio di sviluppare ipertermia maligna durante l'anestesia per inalazione è particolarmente elevato nei pazienti affetti da miopatia di Duchenne, miopatia del nucleo centrale, miotonia di Thomsen, miotonia condrodistrofica (sindrome di Schwartz-Jampel). Si presume che l'ipertermia maligna sia associata all'accumulo di calcio nel sarcoplasma delle fibre muscolari. Tendenza all'ipertermia maligna ereditato nella maggior parte dei casi con modalità autosomica dominante con diversa penetranza del gene patologico. Esiste anche l'ipertermia maligna, ereditaria secondo il tipo recessivo (sindrome di King).
Gli esami di laboratorio nei casi di ipertermia maligna rivelano segni di acidosi respiratoria e metabolica, iperkaliemia e ipermagnesemia, aumento dei livelli di lattato e piruvato nel sangue. Le complicanze tardive dell'ipertermia maligna comprendono un massiccio gonfiore dei muscoli scheletrici, edema polmonare, coagulazione intravascolare disseminata e insufficienza renale acuta.
Ipertermia maligna neurolettica insieme all'elevata temperatura corporea, si manifesta con tachicardia, aritmia, instabilità della pressione arteriosa, sudorazione, cianosi, tachipnea, mentre lo squilibrio idroelettrolitico si manifesta con aumento della concentrazione di potassio nel plasma, acidosi, mioglobinemia, mioglobinuria, aumento dell'attività di CPK, AST, ALT compaiono segni di sindrome DIC. Compaiono e aumentano le contratture muscolari e si sviluppa il coma. Si aggiungono polmonite e oliguria. Nella patogenesi è importante il ruolo della alterata termoregolazione e della disinibizione del sistema dopaminergico nella regione tubero-infundibolare dell'ipotalamo. La morte avviene più spesso dopo 5-8 giorni. L'autopsia rivela cambiamenti distrofici acuti nel cervello e negli organi parenchimali. Sindrome si sviluppa come risultato del trattamento a lungo termine con neurolettici, tuttavia, può svilupparsi in pazienti con schizofrenia che non hanno assunto antipsicotici e raramente in pazienti con parkinsonismo che hanno assunto farmaci L-DOPA per un lungo periodo.
Sindrome da freddo - una sensazione di freddo quasi costante in tutto il corpo o in singole parti: alla testa, alla schiena, ecc., solitamente associata a senestopatie e manifestazioni di sindrome ipocondriaca, talvolta a fobie. I pazienti hanno paura del freddo, delle correnti d'aria e di solito indossano abiti eccessivamente caldi. La loro temperatura corporea è normale; in alcuni casi viene rilevata un'ipertermia permanente. Visto come una delle manifestazioni della distonia autonomica con una predominanza dell'attività della divisione parasimpatica del sistema nervoso autonomo.
Per il trattamento dei pazienti con ipertermia non infettiva, è consigliabile utilizzare beta o alfa-bloccanti (fentolamina 25 mg 2-3 volte al giorno, pirroxano 15 mg 3 volte al giorno), trattamento riparativo generale. Per la bradicardia persistente e la discinesia spastica vengono prescritti preparati di belladonna (bellataminale, belloide, ecc.). Il paziente dovrebbe smettere di fumare e di abusare di alcol.
13.3.12. Disturbi della lacrimazione
La funzione secretoria delle ghiandole lacrimali è assicurata principalmente dall'influenza su di esse degli impulsi provenienti dal nucleo lacrimale parasimpatico, situato nel ponte vicino al nucleo del nervo facciale e che riceve impulsi stimolanti dalle strutture del complesso limbico-reticolare. Dal nucleo lacrimale parasimpatico, gli impulsi viaggiano lungo il nervo intermedio e il suo ramo - il nervo grande petroso - fino al ganglio pterigopalatino parasimpatico. Gli assoni delle cellule situate in questo ganglio costituiscono il nervo lacrimale, che innerva le cellule secretrici della ghiandola lacrimale. Gli impulsi simpatici passano alla ghiandola lacrimale dai gangli simpatici cervicali lungo le fibre del plesso carotideo e causano principalmente vasocostrizione nelle ghiandole lacrimali. Durante il giorno, la ghiandola lacrimale umana produce circa 1,2 ml di liquido lacrimale. La produzione di lacrime avviene principalmente durante i periodi di veglia e viene soppressa durante il sonno.
Una produzione lacrimale compromessa può manifestarsi sotto forma di secchezza oculare a causa della produzione insufficiente di liquido lacrimale da parte delle ghiandole lacrimali. L'eccessiva lacrimazione (epifora) è spesso associata a una violazione del deflusso delle lacrime nella cavità nasale attraverso il dotto nasolacrimale.
Secchezza degli occhi (xeroftalmia, alacrimia). può essere una conseguenza del danno alle ghiandole lacrimali stesse o di un disturbo della loro innervazione parasimpatica. Alterata secrezione del liquido lacrimale - uno dei segni caratteristici della sindrome delle mucose secche di Sjögren (HS Sjogren), Disautonomia congenita di Riley-Day, disautonomia totale acuta transitoria, sindrome di Mikulicz. La xeroftalmia unilaterale è più comune quando il nervo facciale è danneggiato prossimalmente all'origine del suo ramo - il nervo grande petroso. Un quadro tipico della xeroftalmia, spesso complicato dall'infiammazione dei tessuti del bulbo oculare, si osserva talvolta nei pazienti operati di neuroma dell'VIII nervo cranico, durante il quale sono state tagliate le fibre del nervo facciale deformate dal tumore.
Di solito si verifica prosoplegia dovuta a neuropatia del nervo facciale, in cui questo nervo è danneggiato al di sotto dell'origine del nervo grande petroso lacrimazione, derivante dalla paresi del muscolo orbicolare dell'occhio, della palpebra inferiore e, in relazione a ciò, da una violazione del deflusso naturale del liquido lacrimale attraverso il canale nasolacrimale. Lo stesso motivo è alla base della lacrimazione senile, associata ad una diminuzione del tono del muscolo orbicolare dell'occhio, nonché della rinite vasomotoria, della congiuntivite, che porta al gonfiore della parete del canale nasolacrimale. La lacrimazione parossistica eccessiva dovuta al gonfiore delle pareti del dotto nasolacrimale durante un attacco doloroso si verifica durante il dolore a grappolo e gli attacchi di prosopalgia vegetativa. La lacrimazione può essere un riflesso, innescato dall'irritazione della zona di innervazione del primo ramo del nervo trigemino. con epifora fredda (lacrimando per il freddo) carenza di vitamina A, esoftalmo grave. Aumento della lacrimazione durante il pasto caratteristica della sindrome delle “lacrime di coccodrillo”, descritto nel 1928 da F.A. Bogarde. Questa sindrome può essere congenita o verificarsi nella fase di recupero della neuropatia facciale. Nel parkinsonismo, la lacrimazione può essere una delle manifestazioni dell'attivazione generale dei meccanismi colinergici, nonché una conseguenza dell'ipomimia e del raro ammiccamento, che indebolisce la capacità del deflusso del liquido lacrimale attraverso il dotto nasolacrimale.
Il trattamento dei pazienti con disturbi della lacrimazione dipende dalle cause che li provocano. Con la xeroftalmia, è necessario monitorare le condizioni dell'occhio e adottare misure volte a mantenerne l'umidità e prevenire l'infezione, instillando negli occhi soluzioni oleose, albucide, ecc. Recentemente hanno iniziato a usare il liquido lacrimale artificiale.
13.3.13. Disturbi della salivazione
Secchezza delle fauci (iposalivazione, xerostomia) E salivazione eccessiva (ipersalivazione, scialorrea) può essere dovuto a vari motivi. L'ipo e l'ipersalivazione possono essere permanenti o parossistiche,
di notte la produzione di saliva è minore, mentre si mangia e anche alla vista del cibo e del suo odore aumenta la quantità di saliva secreta. In genere vengono prodotti da 0,5 a 2 litri di saliva al giorno. Sotto l'influenza degli impulsi parasimpatici, le ghiandole salivari producono abbondante saliva liquida, mentre l'attivazione dell'innervazione simpatica porta alla produzione di saliva più densa.
Ipersalivazionecomune nel parkinsonismo, nella sindrome bulbare e pseudobulbare, nella paralisi cerebrale; in queste condizioni patologiche esso può essere causato sia da un'iperproduzione di saliva che da disturbi nell'atto della deglutizione, quest'ultima circostanza porta solitamente al flusso spontaneo della saliva dalla bocca anche in caso di secrezione in quantità normale. L'ipersalivazione può essere una conseguenza della stomatite ulcerosa, dell'infestazione da elminti, della tossicosi delle donne in gravidanza, in alcuni casi è considerata psicogena.
Causa di iposalivazione persistente (xerostomia)È Sindrome di Sjogren(sindrome secca), in cui si verificano contemporaneamente xeroftalmia (secchezza degli occhi), secchezza della congiuntiva, della mucosa nasale, disfunzione di altre mucose e gonfiore nell'area delle ghiandole salivari parotidee. L'iposalivazione è un segno di glossodinia, stomalgia, disautonomia totale, lei può si verificano con diabete mellito, malattie del tratto gastrointestinale, digiuno, sotto l'influenza di alcuni farmaci (nitrazepam, preparati al litio, anticolinergici, antidepressivi, antistaminici, diuretici, ecc.), durante la radioterapia. Di solito si verifica secchezza delle fauci quando è eccitato a causa della predominanza delle reazioni simpatiche, è possibile in uno stato depresso.
Se la salivazione è compromessa, è opportuno chiarirne la causa e quindi effettuare un'eventuale terapia patogenetica. Gli anticolinergici possono essere usati come rimedio sintomatico per l'ipersalivazione, per la xerostomia - bromexina (1 compressa 3-4 volte al giorno), pilocarpina (capsule da 5 mg per via sublinguale 1 volta al giorno), acido nicotinico, preparati di vitamina A. Come trattamento sostitutivo artificiale viene utilizzata la saliva.
13.3.14. Disturbi della sudorazione
La sudorazione è uno dei fattori che influenzano la termoregolazione e dipende in una certa misura dallo stato del centro termoregolatore, che fa parte dell'ipotalamo ed esercita un'azione globale
influenza sulle ghiandole sudoripare che, in base alle caratteristiche morfologiche, alla localizzazione e alla composizione chimica del sudore che secernono, si differenziano in merocrine e apocrine, mentre il ruolo di queste ultime nella comparsa dell'iperidrosi è insignificante.
Pertanto, il sistema di termoregolazione è costituito principalmente da alcune strutture dell'ipotalamo (zona preottica della regione ipotalamica) (Guyton A., 1981), dalle loro connessioni con le ghiandole sudoripare tegumentarie e merocrine situate nella pelle. La parte ipotalamica del cervello, attraverso il sistema nervoso autonomo, provvede alla regolazione del trasferimento di calore, controllando lo stato del tono vascolare della pelle e la secrezione delle ghiandole sudoripare,
Inoltre, la maggior parte delle ghiandole sudoripare ha innervazione simpatica, ma il mediatore delle fibre simpatiche postgangliari che si avvicinano ad esse è l'acetilcolina. Non ci sono recettori adrenergici nella membrana postsinaptica delle ghiandole sudoripare merocrine, ma alcuni recettori colinergici possono anche rispondere all'adrenalina e alla norepinefrina circolanti nel sangue. È generalmente accettato che solo le ghiandole sudoripare dei palmi delle mani e delle piante dei piedi abbiano una doppia innervazione colinergica e adrenergica. Questo spiega la loro maggiore sudorazione durante lo stress emotivo.
L'aumento della sudorazione può essere una normale reazione agli stimoli esterni (esposizione termica, attività fisica, eccitazione). Allo stesso tempo, l'iperidrosi eccessiva, stabile, localizzata o generalizzata può essere una conseguenza di alcune malattie organiche neurologiche, endocrine, oncologiche, somatiche generali e infettive. Nei casi di iperidrosi patologica i meccanismi fisiopatologici sono diversi e sono determinati dalle caratteristiche della malattia di base.
Iperidrosi patologica locale osservato relativamente raramente. Nella maggior parte dei casi questo è il cosiddetto iperidrosi idiopatica, in cui si osserva un'eccessiva sudorazione principalmente sui palmi delle mani, sulle piante dei piedi e sulle ascelle. Appare tra i 15 ed i 30 anni, più spesso nelle donne. Nel corso del tempo, la sudorazione eccessiva può gradualmente interrompersi o diventare cronica. Questa forma di iperidrosi locale è solitamente associata ad altri segni di labilità vegetativa e viene spesso osservata nei parenti del paziente.
L'iperidrosi locale comprende anche l'iperidrosi associata all'ingestione di cibi o bevande calde, in particolare caffè e cibi piccanti. Il sudore appare principalmente sulla fronte e sul labbro superiore. Il meccanismo di questa forma di iperidrosi non è stato chiarito. La causa dell'iperidrosi locale in una delle forme è più definita prosopalgia vegetativa - Sindrome di Baillarger-Frey, descritto in francese mi dottori - nel 1847 J. Baillarger (1809-1890) e nel 1923 L. Frey (sindrome auricolotemporale), derivante da un danno al nervo auricolotemporale dovuto all'infiammazione della ghiandola salivare parotide. Pro- il fenomeno di un attacco in questa malattia è iperemia cutanea e aumento della sudorazione nella regione parotido-temporale. Il verificarsi di attacchi è solitamente provocato dal consumo di cibi caldi, dal surriscaldamento generale, dal fumo, dal lavoro fisico e dallo stress emotivo. La sindrome di Bailhardt-Frey può verificarsi anche nei neonati il cui nervo facciale è stato danneggiato durante il parto con il forcipe.
Sindrome del cordone timpanico caratterizzato da una maggiore sudorazione nella zona del mento, di solito in risposta ad una sensazione gustativa. Si verifica dopo operazioni sulla ghiandola sottomandibolare.
Iperidrosi generalizzata si verifica molto più spesso di quello locale. Fisiologico i suoi meccanismi sono diversi. Ecco alcune delle condizioni che causano l’iperidrosi.
1. Sudorazione termoregolatoria, che si verifica in tutto il corpo in risposta all'aumento della temperatura ambiente.
2. La sudorazione eccessiva generalizzata può essere una conseguenza dello stress psicogeno, una manifestazione di rabbia e soprattutto di paura; l'iperidrosi è una delle manifestazioni oggettive del dolore intenso avvertito dal paziente. Tuttavia, durante le reazioni emotive, la sudorazione può verificarsi in aree limitate: viso, palmi delle mani, piedi, ascelle.
3. Malattie infettive e processi infiammatori in cui nel sangue compaiono sostanze pirogene, che portano alla formazione di una triade: ipertermia, brividi, iperidrosi. Le sfumature dello sviluppo e le caratteristiche del decorso dei componenti di questa triade dipendono spesso dalle caratteristiche dell'infezione e dallo stato del sistema immunitario.
4. Cambiamenti nel livello del metabolismo in alcuni disturbi endocrini: acromegalia, tireotossicosi, diabete mellito, ipoglicemia, sindrome della menopausa, feocromocitoma, ipertermia di varia origine.
5. Malattie oncologiche (principalmente cancro, linfoma, morbo di Hodgkin), in cui i prodotti del metabolismo e della decomposizione del tumore entrano nel sangue, dando un effetto pirogeno.
Cambiamenti patologici nella sudorazione sono possibili con lesioni cerebrali accompagnate da disfunzione della sua regione ipotalamica. I disturbi della sudorazione possono essere provocati da incidenti cerebrovascolari acuti, encefalite e processi patologici occupanti spazio nella cavità cranica. Nel parkinsonismo si osserva spesso iperidrosi sul viso. L'iperidrosi di origine centrale è caratteristica della disautonomia familiare (sindrome di Riley-Day).
Lo stato di sudorazione è influenzato da molti farmaci (aspirina, insulina, alcuni analgesici, colinomimetici e farmaci anticolinesterasici - prozerina, calemina, ecc.). L'iperidrosi può essere scatenata dall'alcol, dalle droghe e può essere una delle manifestazioni dei sintomi di astinenza o delle reazioni di astinenza. Sudorazione patologica è una delle manifestazioni di avvelenamento da sostanze organofosforiche (OPS).
Occupa un posto speciale forma essenziale di iperidrosi, in cui la morfologia delle ghiandole sudoripare e la composizione del sudore non vengono modificate. L’eziologia di questa condizione è sconosciuta; il blocco farmacologico dell’attività delle ghiandole sudoripare non porta un successo sufficiente.
Quando si trattano pazienti con iperidrosi, possono essere raccomandati anticolinergici M (ciclodolo, akineton, ecc.), Piccole dosi di clonidina, Sonapax e beta-bloccanti. Gli astringenti applicati localmente sono più efficaci: soluzioni di permanganato di potassio, sali di alluminio, formalina, acido tannico.
Anidrosi(senza sudorazione) potrebbe essere una conseguenza della simpaticectomia. La lesione del midollo spinale è solitamente accompagnata da anidrosi sul tronco e sulle estremità sotto la lesione. Con la sindrome di Horner completa Insieme ai segni principali (miosi, pseudoptosi, endoftalmo) sul viso dal lato affetto si possono solitamente notare iperemia cutanea, dilatazione dei vasi congiuntivali e anidrosi. Può essere rilevata anidrosi nell'area innervata dai nervi periferici danneggiati. Anidrosi sul tronco
e le estremità inferiori potrebbero esserci una conseguenza del diabete mellito, in questi casi, i pazienti non tollerano bene il calore. Potrebbero verificarsi una maggiore sudorazione su viso, testa e collo.
13.3.15. Alopecia
Alopecia nevrotica (alopecia di Michelson) - calvizie che si verifica a causa di disturbi neurotrofici nelle malattie del cervello, principalmente nelle strutture della parte diencefalica del cervello. Il trattamento per questa forma del processo neurotrofico non è stato sviluppato. L'alopecia può essere una conseguenza dei raggi X o delle radiazioni radioattive.
13.3.16. Nausea e vomito
Nausea(nausea)- una peculiare sensazione dolorosa alla gola, nella regione epigastrica di un imminente bisogno di vomitare, segni di incipiente antiperistalsi. Si verifica a causa dell'eccitazione della parte parasimpatica del sistema nervoso autonomo, ad esempio a causa dell'eccessiva irritazione dell'apparato vestibolare o del nervo vago. Accompagnato da pallore, iperidrosi, salivazione abbondante e spesso bradicardia e ipotensione arteriosa.
Vomito(vomito, vomito)- un atto riflesso complesso, manifestato con espulsione involontaria, eruzione del contenuto del tratto digestivo (principalmente lo stomaco) attraverso la bocca, meno spesso attraverso il naso. Può essere causato dall'irritazione diretta del centro del vomito, la zona dei chemocettori situata nel tegmento del midollo allungato (vomito cerebrale). Un fattore così irritante può essere un processo patologico focale (tumore, cisticercosi, emorragia, ecc.), Così come l'ipossia, gli effetti tossici di anestetici, oppiacei, ecc.). Vomito cerebrale si verifica più spesso a causa dell'aumento della pressione intracranica, appare spesso al mattino a stomaco vuoto, di solito senza preavviso e ha un carattere zampillante. La causa del vomito cerebrale può essere encefalite, meningite, lesione cerebrale, tumore al cervello, accidente cerebrovascolare acuto, edema cerebrale, idrocefalo (tutte le sue forme tranne quelle indirette o sostitutive).
Vomito psicogeno - possibile manifestazione di una reazione nevrotica, nevrosi, disturbi mentali.
Spesso La causa del vomito sono vari fattori che irritano secondariamente i recettori del nervo vago a diversi livelli: nel diaframma, organi del tubo digerente. In quest'ultimo caso, la parte afferente dell'arco riflesso è costituita principalmente dalla porzione principale sensibile del nervo vago, mentre la parte efferente è costituita dalle porzioni motorie dei nervi trigemino, glossofaringeo e vago. Può verificarsi anche vomito una conseguenza della sovraeccitazione dell'apparato vestibolare (mal di mare, malattia di Meniere, ecc.).
L'atto del vomito consiste in contrazioni successive di vari gruppi muscolari (diaframma, addominali, piloro, ecc.), mentre l'epiglottide scende, la laringe e il palato molle si sollevano, il che porta all'isolamento (non sempre sufficiente) delle vie respiratorie dal vomito .
peso Il vomito può essere una reazione protettiva dell'apparato digerente all'ingresso o alla formazione di sostanze tossiche al suo interno. Nelle gravi condizioni generali del paziente, il vomito può causare aspirazione delle vie respiratorie; il vomito ripetuto è una delle cause della disidratazione.
13.3.17. Singhiozzo
Singhiozzo(singolo)- contrazione mioclonica involontaria dei muscoli respiratori, simulando un'inspirazione fissa, mentre improvvisamente le vie aeree ed il flusso d'aria che le attraversa vengono bloccate dall'epiglottide e si avverte un suono caratteristico. Nelle persone sane, il singhiozzo può essere una conseguenza dell'irritazione del diaframma causata dall'eccesso di cibo o dal consumo di bevande fredde. In questi casi, i singhiozzi sono isolati e di breve durata. Il singhiozzo persistente può essere una conseguenza dell'irritazione delle parti inferiori del tronco encefalico a causa di incidenti cerebrovascolari, un tumore sottotentoriale o una lesione traumatica del tronco encefalico, aumento dell'ipertensione intracranica e in questi casi è un segno che segnala una minaccia per la vita del paziente. Può essere pericolosa anche l'irritazione del nervo spinale C IV, nonché del nervo frenico da parte di un tumore della tiroide, dell'esofago, del mediastino, dei polmoni, di una malformazione artero-venosa, di un linfoma del collo, ecc.. Malattie gastrointestinali, pancreatite, subfrenica ascesso e intossicazione possono anche causare singhiozzo alcol, barbiturici, stupefacenti. Sono possibili anche singhiozzi ripetuti come una delle manifestazioni di una reazione nevrotica.
13.3.18. Disturbi dell'innervazione del sistema cardiovascolare
I disturbi dell'innervazione del muscolo cardiaco influenzano lo stato dell'emodinamica generale. L'assenza di influenze simpatiche sul muscolo cardiaco limita l'aumento della gittata sistolica del cuore e l'insufficienza delle influenze del nervo vago porta alla comparsa di tachicardia a riposo, mentre sono possibili vari tipi di aritmia, lipotimia e sincope. . L'interruzione dell'innervazione del cuore nei pazienti con diabete mellito porta a fenomeni simili. I disturbi autonomici generali possono essere accompagnati da attacchi di calo della pressione arteriosa ortostatica che si verificano durante movimenti improvvisi quando il paziente cerca di assumere rapidamente una posizione verticale. La distonia vegetativa-vascolare può anche manifestarsi con labilità del polso, cambiamenti nel ritmo dell'attività cardiaca e tendenza alle reazioni angiospastiche, in particolare al mal di testa vascolare, una variante della quale sono varie forme di emicrania.
Nei pazienti con ipotensione ortostatica, è possibile una forte diminuzione della pressione sanguigna sotto l'influenza di molti farmaci: antipertensivi, antidepressivi triciclici, fenotiazine, vasodilatatori, diuretici, insulina. Il cuore umano denervato funziona secondo la regola di Frank-Starling: la forza di contrazione delle fibre miocardiche è proporzionale al valore iniziale del loro allungamento.
13.3.19. Disturbo dell'innervazione simpatica della muscolatura liscia dell'occhio (sindrome di Bernard-Horner)
Sindrome di Bernard-Horner, O La sindrome di Horner. L'innervazione simpatica della muscolatura liscia dell'occhio e delle sue appendici è fornita da impulsi nervosi provenienti dalle strutture nucleari della parte posteriore della parte ipotalamica del cervello, che lungo i percorsi discendenti passano attraverso il tronco e il midollo spinale cervicale e terminano in Jacobson cellule che si formano nelle corna laterali dei segmenti C VIII-D I del midollo spinale Centro ciliospinale di Budge-Weller. Da esso, lungo gli assoni delle cellule di Jacobson, passando attraverso le corrispondenti radici anteriori, i nervi spinali e i rami comunicanti bianchi, entrano nella sezione cervicale della catena simpatica paravertebrale, raggiungendo il ganglio simpatico cervicale superiore. Successivamente, gli impulsi continuano il loro viaggio lungo le fibre postgangliari, che partecipano alla formazione del plesso simpatico delle arterie carotidi comune ed interna, e raggiungono il seno cavernoso. Da qui, insieme all'arteria oftalmica, penetrano nell'orbita e innervare i seguenti muscoli lisci: muscolo pupillare dilatatore, muscolo orbitale e muscolo cartilagineo della palpebra superiore (m. dilatator pupillae, m. orbitalis E M. tarsale superiore).
L'interruzione dell'innervazione di questi muscoli, che si verifica quando qualsiasi parte del percorso degli impulsi simpatici che arrivano loro dalla parte posteriore dell'ipotalamo è danneggiata, porta alla loro paresi o paralisi. A questo proposito, dal lato del processo patologico, La sindrome di Horner o Claude Bernard-Horner, manifestando costrizione della pupilla (miosi paralitica), leggero enoftalmo e la cosiddetta pseudoptosi (abbassamento della palpebra superiore), che causa un certo restringimento della fessura palpebrale (Fig. 13.3). A causa della conservazione dell'innervazione parasimpatica dello sfintere della pupilla dal lato della sindrome di Horner, la reazione della pupilla alla luce rimane intatta.
A causa dell'interruzione delle reazioni vasocostrittrici sulla metà omolaterale del viso La sindrome di Horner è solitamente accompagnata da iperemia della congiuntiva e della pelle; sono possibili anche eterocromia dell'iride e ridotta sudorazione. I cambiamenti nella sudorazione del viso possono aiutare a chiarire il tema del danno alle strutture simpatiche nella sindrome di Horner. Con la localizzazione postgangliare del processo, la sudorazione ridotta sul viso è limitata a un lato del naso e all'area paramediana della fronte. Se la sudorazione è disturbata su tutta la metà del viso, il danno alle strutture simpatiche è pregangliare.
Poiché la ptosi della palpebra superiore e la costrizione della pupilla possono avere origini diverse, per accertarsi che in questo caso vi siano manifestazioni della sindrome di Horner, è possibile verificare la reazione delle pupille all'instillazione di una soluzione anticolinergica M in entrambe occhi. Successivamente, con la sindrome di Horner, apparirà un'anisocoria pronunciata, poiché, a parte le manifestazioni di questa sindrome, la dilatazione della pupilla sarà assente o apparirà leggermente.
Pertanto, la sindrome di Horner indica una violazione dell'innervazione simpatica dei muscoli lisci dell'occhio e della corrispondente metà del viso. Può essere una conseguenza del danno ai nuclei della parte posteriore dell'ipotalamo, alla via simpatica centrale a livello del tronco encefalico o del midollo spinale cervicale, al centro ciliospinale, alle fibre pregangliari che si estendono da esso,

Riso. 13.3.Innervazione simpatica dell'occhio.
a - diagramma dei percorsi: 1 - cellule vegetative dell'ipotalamo; 2 - arteria oftalmica; 3 - arteria carotide interna; 4, 5 - nodi medi e superiori della catena simpatica paravertebrale; 6 - nodo a stella; 7 - corpo del neurone simpatico nel centro ciliospinale del midollo spinale; b - aspetto del paziente con una violazione dell'innervazione simpatica dell'occhio sinistro (sindrome di Bernard-Horner).
il ganglio cervicale superiore e le fibre simpatiche postgangliari che provengono da esso, formando il plesso simpatico dell'arteria carotide esterna e dei suoi rami. La sindrome di Horner può essere causata da lesioni dell'ipotalamo, del tronco cerebrale, del midollo spinale cervicale, delle strutture simpatiche del collo, del plesso dell'arteria carotide esterna e dei suoi rami. Tali lesioni possono essere causate da traumi a queste strutture del sistema nervoso centrale e del sistema nervoso periferico, da un processo patologico volumetrico, da malattie cerebrovascolari e talvolta dalla demielinizzazione nella sclerosi multipla. Un processo oncologico accompagnato dallo sviluppo della sindrome di Horner può essere il cancro del lobo superiore del polmone, che cresce nella pleura (cancro di Pancoast).
13.3.20. Innervazione della vescica e sue patologie
Di grande importanza pratica è l'identificazione delle disfunzioni della vescica, che insorgono in connessione con un disturbo della sua innervazione, che è fornita principalmente dal sistema nervoso autonomo (Fig. 13.4).
Fibre somatosensoriali afferenti provengono dai propriocettori della vescica, che rispondono al suo allungamento. Gli impulsi nervosi derivanti da questi recettori penetrano attraverso i nervi spinali S II - S IV

Riso. 13.4.Innervazione della vescica [secondo Müller].
1 - lobulo paracentrale; 2 - ipotalamo; 3 - midollo spinale lombare superiore; 4 - midollo spinale sacrale inferiore; 5 - vescica; 6 - nervo genitale; 7 - nervo ipogastrico; 8 - nervo pelvico; 9 - plesso della vescica; 10 - detrusore della vescica; 11 - sfintere interno della vescica; 12 - sfintere esterno della vescica.
nelle corde posteriori del midollo spinale, quindi entra nella formazione reticolare del tronco encefalico e oltre - nei lobuli paracentrali degli emisferi cerebrali, Inoltre, lungo il percorso, parte di questi impulsi passa dalla parte opposta.
Grazie all'informazione che passa attraverso le strutture periferiche, spinali e cerebrali indicate fino ai lobuli paracentrali, si realizza lo stiramento della vescica quando è piena e la presenza di ipertrofia incompleta.
L'incrocio di questi percorsi afferenti porta al fatto che con la localizzazione corticale del focus patologico, una violazione del controllo delle funzioni pelviche di solito si verifica solo quando sono colpiti entrambi i lobuli paracentrali (ad esempio, nel meningioma della falce).
Innervazione efferente della vescica è effettuato principalmente a causa dei lobuli paracentrali, della formazione reticolare del tronco encefalico e dei centri autonomi spinali: simpatico (neuroni delle corna laterali dei segmenti Th XI - L II) e parasimpatico, situati a livello dei segmenti del midollo spinale S II - S IV. La regolazione cosciente della minzione viene effettuata principalmente a causa degli impulsi nervosi provenienti dalla zona motoria della corteccia cerebrale e dalla formazione reticolare del tronco ai motoneuroni delle corna anteriori dei segmenti S III - S IV. È chiaro che per garantire la regolazione nervosa della vescica, è necessario preservare i percorsi che collegano tra loro queste strutture del cervello e del midollo spinale, nonché le formazioni del sistema nervoso periferico che forniscono innervazione alla vescica.
Le fibre pregangliari provenienti dal centro simpatico lombare degli organi pelvici (L 1 -L 2) passano nell'ambito dei nervi presacrali e ipogastrici, in transito attraverso le sezioni caudali dei tronchi paravertebrali simpatici e lungo i nervi splancnici lombari (nn. splanchnici lumbales) raggiungono i nodi del plesso mesenterico inferiore (plexus mesentericus inferior). Le fibre postgangliari provenienti da questi nodi partecipano alla formazione dei plessi nervosi della vescica e forniscono innervazione principalmente al suo sfintere interno. A causa della stimolazione simpatica della vescica, lo sfintere interno formato dalla muscolatura liscia si contrae; in questo caso, quando la vescica si riempie, il muscolo della sua parete si allunga, il muscolo che spinge fuori l'urina (m. vesciche detrusoriali). Tutto ciò garantisce la ritenzione urinaria, facilitata dalla simultanea contrazione dello sfintere striato esterno della vescica, che ha innervazione somatica. Suo effettuato dai nervi pudendi (nn. pudendi), costituiti da assoni di motoneuroni situati nei corni anteriori dei segmenti S III S IV del midollo spinale. Anche gli impulsi efferenti diretti ai muscoli del pavimento pelvico e i segnali afferenti contropropriocettivi provenienti da questi muscoli passano attraverso i nervi pudendi.
Innervazione parasimpatica degli organi pelvici effettuato da fibre pregangliari provenienti dal centro parasimpatico della vescica, situato nella parte sacrale del midollo spinale (S I -S III). Partecipano alla formazione del plesso pelvico e raggiungono i gangli intramurali (situati nella parete della vescica). La stimolazione parasimpatica provoca la contrazione della muscolatura liscia che costituisce il corpo della vescica (m. detrusor vesicae) e un concomitante rilassamento dei suoi sfinteri lisci, così come una maggiore motilità intestinale, che crea le condizioni per lo svuotamento della vescica. Contrazione involontaria, spontanea o provocata, del detrusore della vescica (iperattività detrusoriale) porta all'incontinenza urinaria. L'iperattività del detrusore può essere neurogena (ad esempio, nella sclerosi multipla) o idiopatica (in assenza di una causa identificata).
Ritenzione urinaria (ritenzione urinaria) più spesso si verifica a causa di un danno al midollo spinale al di sopra della posizione dei centri autonomici simpatici spinali (Th XI -L II), responsabili dell'innervazione della vescica.
La ritenzione urinaria è causata dalla dissinergia del detrusore e degli sfinteri vescicali (contrazione dello sfintere interno e rilasciamento del detrusore). COSÌ
accade, ad esempio, con danni traumatici al midollo spinale, tumori intravertebrali, sclerosi multipla. In questi casi, la vescica si riempie e il suo fondo può salire fino al livello dell'ombelico e oltre. La ritenzione urinaria è possibile anche a causa del danno all'arco riflesso parasimpatico, che si chiude nei segmenti sacrali del midollo spinale e fornisce innervazione al detrusore della vescica. La causa della paresi o della paralisi detrusoriale può essere una lesione a questo livello del midollo spinale o un disturbo nella funzione delle strutture del sistema nervoso periferico che compongono l'arco riflesso. In caso di ritenzione urinaria persistente, i pazienti solitamente necessitano di svuotare la vescica attraverso un catetere. Insieme alla ritenzione urinaria, di solito si verifica la ritenzione fecale neuropatica. (retencia alvi).
Un danno parziale al midollo spinale al di sopra del livello dei centri spinali autonomi responsabili dell'innervazione della vescica può portare all'interruzione del controllo volontario della minzione e al verificarsi dei cosiddetti bisogno imperativo di urinare, in cui il paziente, sentendo lo stimolo, non è in grado di trattenere l'urina. Un ruolo importante è probabilmente svolto da un disturbo nell'innervazione dello sfintere esterno della vescica, che normalmente può essere controllato in una certa misura con la forza di volontà. Tali manifestazioni di disfunzione vescicale sono possibili, in particolare con danno bilaterale alle strutture mediali delle corde laterali in pazienti con tumore intramidollare o sclerosi multipla.
Un processo patologico che colpisce il midollo spinale a livello della posizione dei centri autonomi simpatici della vescica (cellule delle corna laterali dei segmenti Th I -L II del midollo spinale) porta alla paralisi dello sfintere interno della vescica, mentre il tono del suo protrusore aumenta, in relazione a ciò si verifica un rilascio costante di urina in gocce - vera incontinenza urinaria (incontinentia urinae vera) Poiché viene prodotta dai reni, la vescica è praticamente vuota. La vera incontinenza urinaria può essere causata da ictus spinale, lesione del midollo spinale o tumore spinale a livello di questi segmenti lombari. La vera incontinenza urinaria può essere associata anche a danni alle strutture del sistema nervoso periferico coinvolte nell'innervazione della vescica, in particolare al diabete mellito o all'amiloidosi primaria.
Quando si verifica ritenzione di urina a causa di danni alle strutture del sistema nervoso centrale o periferico, si accumula nella vescica sovraccarica e può creare in essa una pressione così elevata che, sotto la sua influenza, gli sfinteri interni ed esterni della vescica, che sono in uno stato di contrazione spastica, sono allungati. A questo proposito, l'urina viene costantemente rilasciata attraverso l'uretra in gocce o periodicamente in piccole porzioni mentre la vescica rimane piena - incontinenza urinaria paradossa (incontinentia urinae paradoxa), che può essere stabilito identificando mediante esame visivo, nonché mediante palpazione e percussione del basso addome, la sporgenza del fondo della vescica sopra il pube (a volte fino all'ombelico).
Con un danno al centro spinale parasimpatico (segmenti del midollo spinale S I -S III) e alle corrispondenti radici della cauda equina, può svilupparsi debolezza e simultanea compromissione della sensibilità del muscolo che spinge l'urina (m. vesciche detrusoriali), questo provoca ritenzione urinaria.
Tuttavia, in questi casi, col tempo, è possibile ripristinare lo svuotamento riflesso della vescica, che inizia a funzionare in modalità “autonoma” (vescica autonoma).
Chiarire la natura della disfunzione vescicale può aiutare a determinare la diagnosi topica e nosologica della malattia di base. Per chiarire le caratteristiche dei disturbi della funzione vescicale, insieme ad un esame neurologico approfondito, se indicato, viene eseguita una radiografia delle vie urinarie superiori, della vescica e dell'uretra utilizzando soluzioni radiopache. I risultati degli esami urologici, in particolare la cistoscopia e la cistometria (determinazione della pressione nella vescica durante il riempimento con liquido o gas), possono aiutare a chiarire la diagnosi. In alcuni casi, l'elettromiografia dei muscoli striati periuretrali può essere informativa.
Dipartimenti del sistema nervoso centrale
Il sistema nervoso centrale ha molte funzioni. Raccoglie ed elabora informazioni sull'ambiente provenienti dal PNS, forma riflessi e altre reazioni comportamentali, pianifica (prepara) ed esegue movimenti volontari.
Inoltre, il sistema nervoso centrale fornisce le cosiddette funzioni cognitive superiori. I processi legati alla memoria, all’apprendimento e al pensiero avvengono nel sistema nervoso centrale. Il sistema nervoso centrale include midollo spinale (midollo spinale) E cervello (encefalo) (Figura 5-1). Il midollo spinale è diviso in sezioni successive (cervicale, toracica, lombare, sacrale e coccigea), ciascuna delle quali è costituita da segmenti.
Sulla base delle informazioni sui modelli di sviluppo embrionale, il cervello è diviso in cinque sezioni: mielencefalo (midollo), metencefalo (cervello) mesencefalo (mesencefalo) diencefalo (diencefalo) e telencefalo (telencefalo). Nel cervello adulto mielencefalo(midollo)
comprende il midollo allungato (midollo allungato, da midollo), metencefalo(romboencefalo) - ponte (pon Varolii) e cervelletto (cervelletto); mesencefalo(mesencefalo) - mesencefalo; diencefalo(diencefalo) - talamo (talamo) E ipotalamo (ipotalamo), telencefalo(fine del cervello) - gangli della base (nuclei basali) e corteccia cerebrale (corteccia cerebrale) (Fig. 5-1 B). A sua volta, la corteccia di ciascun emisfero è costituita da lobi, che hanno lo stesso nome delle corrispondenti ossa del cranio: frontale (lobo frontale), parietale ( l. parietale), temporale ( l. temporale) E occipitale ( l. occipitale) azioni. Emisferi collegato corpo calloso (corpo calloso) - un massiccio fascio di assoni che attraversa la linea mediana tra gli emisferi.
Sulla superficie del sistema nervoso centrale si trovano diversi strati di tessuto connettivo. Questo meningi: molli(Pia madre), aracnoide (aracnoidea madre) E difficile (dura madre). Proteggono il sistema nervoso centrale. Subaracnoideo (subaracnoideo) lo spazio tra le membrane molli e aracnoide è riempito liquido cerebrospinale (CSF)).
Riso. 5-1. La struttura del sistema nervoso centrale.
A - cervello e midollo spinale con nervi spinali. Notare le dimensioni relative dei componenti del sistema nervoso centrale. C1, Th1, L1 e S1 sono rispettivamente le prime vertebre delle regioni cervicale, toracica, lombare e sacrale. B - componenti principali del sistema nervoso centrale. Sono mostrati anche i quattro lobi principali della corteccia cerebrale: occipitale, parietale, frontale e temporale.
Divisioni del cervello
Le principali strutture del cervello sono mostrate in Fig. 5-2 A. Ci sono cavità nel tessuto cerebrale - ventricoli, riempito con liquido cerebrospinale (Fig. 5-2 B, C). Il liquido cerebrospinale ha un effetto ammortizzante e regola l'ambiente extracellulare attorno ai neuroni. Viene prodotto principalmente il liquido cerebrospinale plessi coroidei, che sono rivestiti con cellule ependimali specializzate. I plessi corioidei si trovano nei ventricoli laterali, terzo e quarto. Ventricoli laterali localizzati in ciascuno dei due emisferi cerebrali. Si connettono con terzo ventricolo Attraverso forame interventricolare (forame di Monroy). Il terzo ventricolo si trova sulla linea mediana tra le due metà del diencefalo. È collegato a quarto ventricolo Attraverso acquedotto del cervello (acquedotto di Silvio), penetrando nel mesencefalo. Il “fondo” del quarto ventricolo è formato dal ponte e dal midollo allungato, mentre il “tetto” è formato dal cervelletto. La continuazione del quarto ventricolo in direzione caudale è canale centrale midollo spinale, solitamente chiuso nell'adulto.
Il liquido cerebrospinale fluisce dai ventricoli del ponte spazio subaracnoideo (subaracnoideo). attraverso tre fori nel tetto del quarto ventricolo: apertura mediana(Buco Magendie) e due aperture laterali(Buchi di Lushka). Il liquido cerebrospinale che lascia il sistema ventricolare circola nello spazio subaracnoideo che circonda il cervello e il midollo spinale. Le estensioni di questo spazio vengono chiamate subaracnoideo (subaracnoideo)
carri armati. Uno di loro - cisterna lombare (lombare), da cui si ottengono campioni di liquido cerebrospinale mediante puntura lombare per l'analisi clinica. Una parte significativa del liquido cerebrospinale viene assorbita attraverso le valvole dotate villi aracnoidei nei seni venosi della dura madre.
Il volume totale del liquido cerebrospinale nei ventricoli del cervello è di circa 35 ml, mentre lo spazio subaracnoideo contiene circa 100 ml. Ogni minuto vengono prodotti circa 0,35 ml di liquido cerebrospinale. A questo ritmo, il ricambio del liquido cerebrospinale avviene circa quattro volte al giorno.
In una persona in posizione supina, la pressione del liquido cerebrospinale nello spazio subaracnoideo della colonna vertebrale raggiunge 120-180 mm di colonna d'acqua. Il tasso di produzione del liquido cerebrospinale è relativamente indipendente dalle pressioni ventricolare e subaracnoidea e dalla pressione sanguigna sistemica. Allo stesso tempo, la velocità di riassorbimento del liquido cerebrospinale è direttamente correlata alla pressione del liquido cerebrospinale.
Il liquido extracellulare nel sistema nervoso centrale comunica direttamente con il liquido cerebrospinale. Pertanto, la composizione del liquido cerebrospinale influenza la composizione dell’ambiente extracellulare attorno ai neuroni nel cervello e nel midollo spinale. I componenti principali del liquido cerebrospinale nella cisterna lombare sono elencati nella Tabella. 5-1. Per confronto, vengono fornite le concentrazioni delle sostanze corrispondenti nel sangue. Come mostrato in questa tabella, il contenuto di K+, glucosio e proteine nel liquido cerebrospinale è inferiore a quello del sangue, mentre il contenuto di Na+ e Cl - - è maggiore. Inoltre, nel liquido cerebrospinale non ci sono praticamente globuli rossi. Grazie all'aumento del contenuto di Na + e Cl -, l'isotonicità del liquido cerebrospinale e del sangue è garantita, nonostante ci siano relativamente poche proteine nel liquido cerebrospinale.
Tabella 5-1. Composizione del liquido cerebrospinale e del sangue

Riso. 5-2. Cervello.
A - sezione mediasagittale del cervello. Notare le posizioni relative della corteccia cerebrale, del cervelletto, del talamo e del tronco cerebrale, nonché delle varie commissure. B e C - sistema ventricolare cerebrale in situ - vista laterale (B) e vista frontale (C)

Organizzazione del midollo spinale
Midollo spinale si trova nel canale spinale e negli adulti è un cordone cilindrico lungo (45 cm negli uomini e 41-42 cm nelle donne), un po' appiattito dalla parte anteriore a quella posteriore, che in alto (cranialmente) passa direttamente nel midollo allungato, e all'estremità la parte inferiore (caudalmente) termina con una punta conica a livello della II vertebra lombare. La conoscenza di questo fatto è di importanza pratica (per non danneggiare il midollo spinale durante una puntura lombare allo scopo di prelevare liquido cerebrospinale o ai fini dell'anestesia spinale, è necessario inserire un ago di siringa tra i processi spinosi del III e IV vertebre lombari).
Il midollo spinale lungo la sua lunghezza presenta due ispessimenti corrispondenti alle radici nervose degli arti superiori e inferiori: quello superiore è chiamato ispessimento cervicale e quello inferiore è chiamato ispessimento lombare. Di questi ispessimenti, quello lombare è più esteso, ma quello cervicale è più differenziato, al quale si associa un'innervazione più complessa della mano come organo del travaglio.
Nei fori intervertebrali vicino alla giunzione di entrambe le radici, la radice dorsale ha un ispessimento: il ganglio spinale. (ganglio spinale), contenente cellule nervose false unipolari (neuroni afferenti) con un processo, che viene poi diviso in due rami. Uno di essi, quello centrale, entra come parte della radice dorsale nel midollo spinale, mentre l'altro, quello periferico, continua nel nervo spinale. Così,
Nei gangli spinali non ci sono sinapsi, poiché qui si trovano solo i corpi cellulari dei neuroni afferenti. Ciò distingue i nodi nominati dai nodi autonomi del SNP, poiché in quest'ultimo entrano in contatto i neuroni intercalari ed efferenti.
Il midollo spinale è costituito da materia grigia contenente cellule nervose e sostanza bianca costituita da fibre nervose mielinizzate.
La materia grigia forma due colonne verticali situate nella metà destra e sinistra del midollo spinale. Nel mezzo c'è uno stretto canale centrale contenente liquido cerebrospinale. Il canale centrale è un residuo della cavità del tubo neurale primario, quindi nella parte superiore comunica con il quarto ventricolo del cervello.
La materia grigia che circonda il canale centrale è chiamata substantia intermedia. In ciascuna colonna di materia grigia ci sono due colonne: anteriore e posteriore. Nelle sezioni trasversali, questi pilastri sembrano corna: anteriori, allargati e posteriori, appuntiti.
La materia grigia è costituita da cellule nervose raggruppate in nuclei, la cui posizione corrisponde generalmente alla struttura segmentale del midollo spinale e al suo arco riflesso primario a tre membri. Il primo neurone sensoriale di questo arco si trova nei gangli spinali, il suo processo periferico va come parte dei nervi agli organi e ai tessuti e si lega ai recettori lì, e quello centrale penetra nel midollo spinale come parte delle radici sensoriali posteriori.
Riso. 5-3. Midollo spinale.
A - tratti nervosi del midollo spinale; B - sezione trasversale del midollo spinale. Percorsi

Struttura del neurone
Unità funzionale del sistema nervoso - neurone. Un tipico neurone ha una superficie ricettiva nella forma corpo cellulare (soma) e diversi scatti - dendriti, su cui si trovano sinapsi, quelli. contatti interneuronali. L'assone di una cellula nervosa forma connessioni sinaptiche con altri neuroni o con cellule effettrici. Le reti di comunicazione del sistema nervoso sono costituite da circuiti neurali, formato da neuroni interconnessi sinapticamente.
Soma
Nel soma ci sono neuroni nucleo E nucleolo(Fig. 5-4), nonché un apparato biosintetico ben sviluppato che produce componenti di membrana, sintetizza enzimi e altri composti chimici necessari per le funzioni specializzate delle cellule nervose. L'apparato di biosintesi nei neuroni include Corpi di Nissl- cisterne appiattite strettamente adiacenti del reticolo endoplasmatico granulare, nonché ben definite Apparato del Golgi. Inoltre, il soma ne contiene numerosi mitocondri ed elementi citoscheletrici, inclusi neurofilamenti E microtubuli. Come risultato della degradazione incompleta dei componenti della membrana, si forma il pigmento lipofuscina, accumulandosi con l’età in un certo numero di neuroni. In alcuni gruppi di neuroni nel tronco cerebrale (ad esempio, nei neuroni della substantia nigra e del locus coeruleus), il pigmento melatonina è evidente.
Dendriti
I dendriti, prolungamenti del corpo cellulare, raggiungono in alcuni neuroni una lunghezza superiore a 1 mm, e rappresentano oltre il 90% della superficie del neurone. Nelle parti prossimali dei dendriti (più vicine al corpo cellulare)
contiene corpi di Nissl e parti dell'apparato di Golgi. Tuttavia, i componenti principali del citoplasma dei dendriti sono i microtubuli e i neurofilamenti. Era generalmente accettato che i dendriti non fossero elettricamente eccitabili. Tuttavia, è ormai noto che i dendriti di molti neuroni hanno una conduttività controllata dal voltaggio. Ciò è spesso dovuto alla presenza di canali del calcio che, quando attivati, generano potenziali d'azione del calcio.
Assone
L'area specializzata del corpo cellulare (solitamente il soma, ma talvolta il dendrite) da cui si estende l'assone è chiamata collinetta dell'assone. L'assone e la collinetta dell'assone differiscono dal soma e dai dendriti prossimali in quanto non contengono reticolo endoplasmatico granulare, ribosomi liberi o apparato di Golgi. L'assone contiene un reticolo endoplasmatico liscio e un citoscheletro pronunciato.
I neuroni possono essere classificati in base alla lunghezza dei loro assoni. U Neuroni del Golgi di tipo 1 gli assoni sono corti e terminano, come i dendriti, vicino al soma. Neuroni del Golgi di tipo 2 caratterizzato da assoni lunghi, talvolta più di 1 m.
I neuroni comunicano tra loro utilizzando potenziali d'azione, diffondendosi nei circuiti neurali lungo gli assoni. Di conseguenza, i potenziali d'azione viaggiano da un neurone all'altro trasmissione sinaptica. Durante il processo di trasferimento, raggiungendo terminale presinaptico Un potenziale d'azione di solito innesca il rilascio di una sostanza neurotrasmettitore che neanche eccita la cellula postsinaptica in modo che in esso avvenga una scarica di uno o più potenziali d'azione, o rallenta la sua attività. Gli assoni non solo trasmettono informazioni nei circuiti neurali, ma trasportano anche sostanze chimiche ai terminali sinaptici attraverso il trasporto assonale.
Riso. 5-4. Schema di un neurone “ideale” e dei suoi componenti principali.
La maggior parte degli input afferenti che arrivano lungo gli assoni di altre cellule terminano in sinapsi sui dendriti (D), ma alcuni terminano in sinapsi sul soma. Le terminazioni nervose eccitatorie sono spesso localizzate distalmente sui dendriti, mentre le terminazioni nervose inibitorie sono spesso localizzate sul soma.

Organelli neuronali
La Figura 5-5 mostra il soma dei neuroni. Il soma dei neuroni mostra il nucleo e il nucleolo, un apparato biosintetico che produce componenti di membrana, sintetizza enzimi e altri composti chimici necessari per le funzioni specializzate delle cellule nervose. Include corpi di Nissl: cisterne appiattite di tessuto granulare strettamente adiacenti l'una all'altra.
reticolo endoplasmatico e un apparato di Golgi ben definito. Il soma contiene mitocondri ed elementi citoscheletrici, inclusi neurofilamenti e microtubuli. Come risultato della degradazione incompleta dei componenti della membrana, si forma il pigmento lipofuscina, che si accumula con l'età in un numero di neuroni. In alcuni gruppi di neuroni nel tronco cerebrale (ad esempio, nei neuroni della substantia nigra e del locus coeruleus), il pigmento melatonina è evidente.
Riso. 5-5. Neurone.
A - organelli neuronali. Il diagramma mostra i tipici organelli neuronali come appaiono al microscopio ottico. La metà sinistra del diagramma riflette le strutture del neurone dopo la colorazione di Nissl: nucleo e nucleolo, corpi di Nissl nel citoplasma del soma e dendriti prossimali, nonché l'apparato di Golgi (non colorato). Notare l'assenza di corpi di Nissl nella collinetta dell'assone e nell'assone. Parte di un neurone dopo colorazione con sali di metalli pesanti: sono visibili le neurofibrille. Con opportuna colorazione con sali di metalli pesanti si può osservare l'apparato di Golgi (non mostrato in questo caso). Sulla superficie del neurone sono presenti diverse terminazioni sinaptiche (colorate con sali di metalli pesanti). B - Il diagramma corrisponde all'immagine al microscopio elettronico. Sono visibili il nucleo, il nucleolo, la cromatina e i pori nucleari. Nel citoplasma sono visibili i mitocondri, il reticolo endoplasmatico rugoso, l'apparato di Golgi, i neurofilamenti e i microtubuli. All'esterno della membrana plasmatica si trovano le terminazioni sinaptiche e i processi degli astrociti

Tipi di neuroni
I neuroni sono molto diversi. I neuroni di diverso tipo svolgono funzioni di comunicazione specifiche, che si riflettono nella loro struttura. COSÌ, neuroni dei gangli della radice dorsale (gangli della radice dorsale) ricevono informazioni non attraverso la trasmissione sinaptica, ma dalle terminazioni nervose sensoriali degli organi. I corpi cellulari di questi neuroni sono privi di dendriti (Fig. 5-6 A5) e non ricevono terminazioni sinaptiche. Dopo aver lasciato il corpo cellulare, l'assone di un tale neurone si divide in due rami, uno dei quali (processo periferico)
viene inviato come parte del nervo periferico al recettore sensoriale e dall'altro ramo (processo centrale) entra nel midollo spinale (come parte di radice dorsale) o nel tronco cerebrale (come parte di nervo cranico).
Altri tipi di neuroni come cellule piramidali corteccia cerebrale e Cellule di Purkinje La corteccia cerebellare è impegnata nell'elaborazione delle informazioni (Fig. 5-6 A1, A2). I loro dendriti sono ricoperti di spine dendritiche e sono caratterizzati da un'ampia superficie. Hanno un numero enorme di input sinaptici.
Riso. 5-6. Tipi di neuroni
A - neuroni di varie forme: 1 - neurone che ricorda una piramide. Neuroni di questo tipo, chiamati cellule piramidali, sono caratteristici della corteccia cerebrale. Notare i processi simili a spine che punteggiano la superficie dei dendriti; 2 - Cellule di Purkinje, dal nome del neuroanatomista ceco Jan Purkinje che per primo le descrisse. Si trovano nella corteccia cerebellare. La cellula ha il corpo a forma di pera; da un lato del soma c'è un abbondante plesso di dendriti, dall'altro un assone. I rami sottili dei dendriti sono ricoperti di spine (non mostrate nel diagramma); 3 - motoneurone simpatico postgangliare; 4 - motoneurone alfa del midollo spinale. Come il motoneurone simpatico postgangliare (3), è multipolare, con dendriti radiali; 5 - cellula sensoriale del ganglio spinale; non ha dendriti. Il suo processo è diviso in due rami: centrale e periferico. Poiché durante lo sviluppo embrionale l'assone si forma come risultato della fusione di due processi, questi neuroni non sono considerati unipolari, ma pseudounipolari. B - tipi di neuroni

Tipi di cellule non neuronali
Un altro gruppo di elementi cellulari del sistema nervoso è neuroglia(Fig. 5-7 A), o cellule di supporto. Nel sistema nervoso centrale umano, il numero di cellule neurogliali è un ordine di grandezza maggiore del numero di neuroni: rispettivamente 10 13 e 10 12. La neuroglia non partecipa direttamente ai processi di comunicazione a breve termine nel sistema nervoso, ma contribuisce all'implementazione di questa funzione da parte dei neuroni. Pertanto, le cellule neurogliali di un certo tipo si formano attorno a molti assoni guaina mielinica, aumentando significativamente la velocità dei potenziali d’azione. Ciò consente agli assoni di trasmettere rapidamente informazioni a cellule distanti.
Tipi di neuroglia
Le cellule gliali supportano l'attività dei neuroni (Fig. 5-7 B). Nel sistema nervoso centrale, le neuroglia sono classificate come astrociti E oligodendrociti, e nel PNS - Cellule di Schwann E cellule satellite. Inoltre, le cellule gliali centrali sono considerate cellule microglia e cellule ependima.
Astrociti(chiamati così per la loro forma a stella) regolano il microambiente attorno ai neuroni del sistema nervoso centrale, sebbene entrino in contatto solo con parte della superficie dei neuroni centrali (Fig. 5-7 A). Tuttavia, i loro processi sono circondati da gruppi di terminali sinaptici, che di conseguenza sono isolati dalle sinapsi vicine. Riprese speciali - "gambe" gli astrociti formano contatti con i capillari e con il tessuto connettivo sulla superficie del sistema nervoso centrale - con Pia madre(Fig. 5-7A). Le gambe limitano la libera diffusione delle sostanze nel sistema nervoso centrale. Gli astrociti possono assorbire attivamente K+ e sostanze neurotrasmettitrici, per poi metabolizzarle. Pertanto, gli astrociti svolgono un ruolo tampone, bloccando l’accesso diretto di ioni e neurotrasmettitori all’ambiente extracellulare attorno ai neuroni. Nel citoplasma degli astrociti sono presenti le cellule gliali
filamenti che svolgono una funzione di supporto meccanico nel tessuto del sistema nervoso centrale. In caso di danno, i processi degli astrociti contenenti filamenti gliali subiscono ipertrofia e formano una “cicatrice” gliale.
Altri elementi della neuroglia forniscono l'isolamento elettrico degli assoni neuronali. Molti assoni sono ricoperti di materiale isolante guaina mielinica.È un involucro multistrato avvolto elicoidalmente sulla membrana plasmatica degli assoni. Nel sistema nervoso centrale, la guaina mielinica è creata dalle membrane cellulari oligodendroglia(Fig. 5-7 B3). Nel SNP la guaina mielinica è formata da membrane Cellule di Schwann(Fig. 5-7 B2). Gli assoni del sistema nervoso centrale non mielinizzati (non mielinizzati) non hanno un rivestimento isolante.
La mielina aumenta la velocità dei potenziali d'azione perché le correnti ioniche durante un potenziale d'azione entrano ed escono solo in Intercettazioni di Ranvier(aree di interruzione tra cellule mielinizzanti adiacenti). Pertanto, il potenziale d'azione "salta" da un'intercettazione all'altra, la cosiddetta conduzione saltatoria.
Inoltre, la neuroglia contiene cellule satellitari, incapsulando i neuroni gangliari spinali e cranici, regolando il microambiente attorno a questi neuroni in modo simile a quello degli astrociti. Un altro tipo di cellula - microglia, o fagociti latenti. In caso di danno alle cellule del sistema nervoso centrale, le microglia aiutano a rimuovere i prodotti di degradazione cellulare. Questo processo coinvolge altre cellule neurogliali, nonché fagociti che penetrano nel sistema nervoso centrale dal flusso sanguigno. Il tessuto del sistema nervoso centrale è separato dal liquido cerebrospinale, che riempie i ventricoli del cervello, da un epitelio formato cellule ependimali(Fig. 5-7 A). L'ependima consente la diffusione di molte sostanze tra lo spazio extracellulare del cervello e il liquido cerebrospinale. Le cellule ependimali specializzate dei plessi corioidei nel sistema ventricolare secernono quantità significative
quota del QCS.
Riso. 5-7. Cellule non neuronali.
A - rappresentazione schematica degli elementi non neurali del sistema nervoso centrale. Sono raffigurati due astrociti, i cui processi terminano sul soma e sui dendriti del neurone, e contattano anche la pia madre e/o i capillari. Gli oligodendrociti formano la guaina mielinica degli assoni. Sono mostrate anche le cellule microgliali e le cellule ependimali. B - diversi tipi di cellule neurogliali nel sistema nervoso centrale: 1 - astrocito fibrillare; 2 - astrocito protoplasmatico. Si notino i peduncoli astrocitici a contatto con i capillari (vedi 5-7 A); 3 - oligodendrociti. Ciascuno dei suoi processi prevede la formazione di una o più guaine mieliniche internodali attorno agli assoni del sistema nervoso centrale; 4 - cellule microgliali; 5 - cellule ependimali

Schema di propagazione dell'informazione lungo un neurone
Nella zona della sinapsi, l'EPSP formato localmente si propaga passivamente elettrotonicamente attraverso la membrana postsinaptica della cellula. Questa distribuzione non segue la legge del tutto o niente. Se un gran numero di sinapsi eccitatorie vengono eccitate contemporaneamente o quasi contemporaneamente, si verifica il fenomeno somma, manifestato nella comparsa di EPSP di ampiezza significativamente maggiore, che possono depolarizzare la membrana dell'intera cellula postsinaptica. Se l'entità di questa depolarizzazione raggiunge un certo valore di soglia (10 mV o più) nell'area della membrana postsinaptica, allora i canali Na+ voltaggio-dipendenti si aprono alla velocità della luce sulla collinetta assonica della cellula nervosa e la cellula genera un potenziale d'azione condotto lungo il suo assone. Con un rilascio abbondante del trasmettitore, il potenziale postsinaptico può apparire già 0,5-0,6 ms dopo che il potenziale d'azione è arrivato nell'area presinaptica. Dall'inizio dell'EPSP alla formazione del potenziale d'azione passano circa 0,3 ms.
Stimolo soglia- lo stimolo più debole distinto in modo affidabile dal recettore sensoriale. Per fare ciò, lo stimolo deve evocare un potenziale recettore di ampiezza tale da essere sufficiente ad attivare almeno una fibra afferente primaria. Stimoli più deboli possono produrre un potenziale recettoriale sottosoglia, ma non ecciteranno i neuroni sensoriali centrali e quindi non saranno percepiti. Inoltre, la quantità
dipende dai neuroni afferenti primari eccitati necessari per la percezione sensoriale spaziale E sommatoria temporale nelle vie sensoriali (Fig. 5-8 B, D).
Interagendo con il recettore, le molecole di ACh aprono canali ionici non specifici nella membrana cellulare postsinaptica in modo che la loro capacità di condurre cationi monovalenti aumenti. Il funzionamento dei canali porta ad una corrente di base di ioni positivi verso l'interno, e quindi alla depolarizzazione della membrana postsinaptica, che in relazione alle sinapsi viene chiamata potenziale postsinaptico eccitatorio.
Le correnti ioniche coinvolte nella generazione di EPSP si comportano diversamente dalle correnti di sodio e potassio durante la generazione di un potenziale d'azione. Il motivo è che il meccanismo per generare EPSP coinvolge altri canali ionici con proprietà diverse (dipendenti dal ligando anziché dal voltaggio). Al potenziale d'azione vengono attivati i canali ionici voltaggio-dipendenti e con l'aumento della depolarizzazione si aprono i canali successivi, in modo che il processo di depolarizzazione si rafforzi. Allo stesso tempo, la conduttanza dei canali controllati dal trasmettitore (dipendenti dal ligando) dipende solo dal numero di molecole trasmettitrici associate alle molecole recettrici (a seguito delle quali i canali ionici controllati dal trasmettitore si aprono) e, quindi, dal numero di canali ionici aperti. L'ampiezza dell'EPSP varia da 100 μV fino a 10 mV in alcuni casi. A seconda del tipo di sinapsi, la durata totale dell'EPSP in alcune sinapsi varia da 5 a 100 ms.
Riso. 5-8. Le informazioni fluiscono dai dendriti al soma, all'assone, alla sinapsi.
La figura mostra i tipi di potenziali in diversi punti del neurone a seconda della somma spaziale e temporale

Riflesso- questa è una risposta a uno stimolo specifico, effettuato con la partecipazione obbligatoria del sistema nervoso. Viene chiamato il circuito neurale che fornisce un riflesso specifico arco riflesso.
Nella sua forma più semplice arco riflesso del sistema nervoso somatico(Fig. 5-9 A), di regola, è costituito da recettori sensoriali di una certa modalità (il primo collegamento dell'arco riflesso), le informazioni dalle quali entrano nel sistema nervoso centrale lungo l'assone di una cellula sensibile situata nella colonna vertebrale ganglio esterno al sistema nervoso centrale (il secondo arco riflesso di collegamento). Come parte della radice dorsale del midollo spinale, l'assone della cellula sensibile entra nel corno dorsale del midollo spinale dove forma una sinapsi sull'interneurone. L'assone dell'interneurone si dirige senza interruzione alle corna anteriori, dove forma una sinapsi sull'α-motoneurone (l'interneurone e l'α-motoneurone, in quanto strutture situate nel sistema nervoso centrale, costituiscono il terzo anello dell'arco riflesso). L'assone dell'α-motoneurone emerge dalle corna anteriori come parte della radice anteriore del midollo spinale (il quarto collegamento dell'arco riflesso) e si dirige nel muscolo scheletrico (il quinto collegamento dell'arco riflesso), formando il muscolo neuronale sinapsi su ciascuna fibra muscolare.
Lo schema più semplice arco riflesso del sistema nervoso simpatico autonomo
(Fig. 5-9 B), di solito è costituito da recettori sensoriali (il primo collegamento dell'arco riflesso), le informazioni dalle quali entrano nel sistema nervoso centrale lungo l'assone di una cellula sensibile situata nel ganglio spinale o in altro ganglio sensibile all'esterno del centro sistema nervoso (il secondo collegamento degli archi riflessi). L'assone della cellula sensoriale come parte della radice dorsale entra nel corno dorsale del midollo spinale, dove forma una sinapsi sull'interneurone. L'assone dell'interneurone va alle corna laterali, dove forma una sinapsi sul neurone simpatico pregangliare (nelle regioni toracica e lombare). (Interneurone e simpatico pregangliare
neurone è il terzo anello dell'arco riflesso). L'assone del neurone simpatico pregangliare lascia il midollo spinale come parte delle radici anteriori (il quarto collegamento dell'arco riflesso). Le altre tre varianti del percorso di questo tipo di neuroni sono riunite nel diagramma. Nel primo caso, l'assone del neurone simpatico pregangliare va al ganglio paravertebrale dove forma una sinapsi sul neurone, il cui assone va all'effettore (il quinto collegamento dell'arco riflesso), ad esempio, al liscio muscoli degli organi interni, alle cellule secretorie, ecc. Nel secondo caso, l'assone del neurone simpatico pregangliare va al ganglio prevertebrale, dove forma una sinapsi su un neurone, il cui assone va all'organo interno (il quinto collegamento dell'arco riflesso). Nel terzo caso, l'assone del neurone simpatico pregangliare entra nel midollo surrenale, dove forma una sinapsi su una cellula speciale che rilascia adrenalina nel sangue (tutto questo è il quarto collegamento dell'arco riflesso). In questo caso, l'adrenalina scorre attraverso il sangue verso tutte le strutture bersaglio che hanno recettori farmacologici per essa (il quinto collegamento dell'arco riflesso).
Nella sua forma più semplice arco riflesso del sistema nervoso autonomo parasimpatico(Fig. 5-9 B) è costituito da recettori sensoriali - il primo collegamento dell'arco riflesso (situato, ad esempio, nello stomaco), che inviano informazioni al sistema nervoso centrale lungo l'assone di una cellula sensibile situata nel ganglio situato lungo il nervo vago (secondo arco riflesso di collegamento). L'assone della cellula sensibile trasmette le informazioni direttamente al midollo allungato, dove si forma una sinapsi sul neurone, il cui assone (anche all'interno del midollo allungato) forma una sinapsi sul neurone pregangliare parasimpatico (il terzo anello dell'arco riflesso ). Da esso, l'assone, ad esempio come parte del nervo vago, ritorna allo stomaco e forma una sinapsi sulla cellula efferente (il quarto collegamento dell'arco riflesso), il cui assone si ramifica lungo il tessuto dello stomaco (il quinto collegamento dell'arco riflesso), formando terminazioni nervose.
Riso. 5-9. Schemi dei principali archi riflessi.
A - Arco riflesso del sistema nervoso somatico. B - Arco riflesso del sistema nervoso simpatico autonomo. B - Arco riflesso del sistema nervoso autonomo parasimpatico

Boccioli di gusto
Familiare a tutti noi sensazioni gustative sono in realtà miscele di quattro gusti elementari: salato, dolce, acido e amaro. Quattro sostanze sono particolarmente efficaci nel produrre le corrispondenti sensazioni gustative: cloruro di sodio (NaCl), saccarosio, acido cloridrico (HC1) e chinino.
Distribuzione spaziale e innervazione delle papille gustative
Le papille gustative sono contenute in diversi tipi di papille gustative sulla superficie della lingua, del palato, della faringe e della laringe (Fig. 5-10 A). Situato sulla parte anteriore e laterale della lingua a forma di fungo E a forma di foglia
papille, e sulla superficie della radice della lingua - scanalato. Quest'ultimo può comprendere diverse centinaia di papille gustative, il cui numero totale nell'uomo raggiunge diverse migliaia.
La sensibilità specifica al gusto non è la stessa nelle diverse aree della superficie della lingua (Fig. 5-10 B, C). I gusti dolci sono percepiti meglio dalla punta della lingua, salato e acido dalle zone laterali e amaro dalla base (radice) della lingua.
Le papille gustative sono innervate da tre nervi cranici, due dei quali sono mostrati in Fig. 5-10 G. Corda di tamburo(corda del timpano- ramo del nervo facciale) fornisce le papille gustative dei due terzi anteriori della lingua, nervo glossofaringeo- terzo posteriore (Fig. 5-10 D). Nervo vago innerva alcune papille gustative della laringe e dell'esofago superiore.
Riso. 5-10 Sensibilità chimica: gusto e sue basi.
A - papilla gustativa. Organizzazione delle papille gustative in tre tipi di papille. Viene mostrata una papilla gustativa con un'apertura gustativa all'apice e nervi che si estendono dal basso, oltre a due tipi di cellule chemorecettrici, cellule di supporto (supporto) e cellule del gusto. B - Sulla superficie della lingua sono presenti tre tipi di papille. B - distribuzione delle zone di quattro qualità gustative elementari sulla superficie della lingua. D - innervazione dei due terzi anteriori e del terzo posteriore della superficie della lingua da parte dei nervi facciale e glossofaringeo

Papilla gustativa
Le sensazioni gustative derivano dall'attivazione dei chemocettori nelle papille gustative (papille gustative). Ogni papilla gustativa(Calicilus gustatorius) contiene da 50 a 150 cellule sensoriali (chemorecettive, gustative) e comprende anche cellule di supporto (di supporto) e basali (Fig. 5-11 A). La parte basale della cellula sensoriale forma una sinapsi all'estremità dell'assone afferente primario. Esistono due tipi di cellule chemiorecettive contenenti diverse vescicole sinaptiche: con un centro denso di elettroni o vescicole rotonde trasparenti. La superficie apicale delle cellule è ricoperta di microvilli diretti verso il poro del gusto.
Molecole chemocettrici microvilli interagiscono con le molecole stimolanti che entrano nel tempo di gusto(apertura gustativa) dal liquido che lava le papille gustative. Questo fluido è in parte prodotto dalle ghiandole tra le papille gustative. Come risultato di uno spostamento della conduttività della membrana, nella cellula sensoriale sorge un potenziale recettore e viene rilasciato un neurotrasmettitore eccitatorio, sotto l'influenza del quale si sviluppa un potenziale generatore nella fibra afferente primaria e inizia una scarica di impulsi, trasmessa al centro sistema nervoso.
La codifica delle quattro qualità gustative primarie non si basa sulla completa selettività delle cellule sensoriali. Ogni cellula risponde agli stimoli di più di una qualità gustativa, ma, di regola, risponde più attivamente solo a una. La discriminazione del gusto dipende dall'input ordinato spazialmente da una popolazione di cellule sensoriali. L'intensità di uno stimolo è codificata dalle caratteristiche quantitative dell'attività che provoca (frequenza degli impulsi e numero di fibre nervose eccitate).
Nella fig. 5-11 mostra il meccanismo delle papille gustative, che si attiva per sostanze di gusti diversi.
I meccanismi cellulari della percezione del gusto si riducono a vari modi di depolarizzare la membrana cellulare e aprire ulteriormente i canali del calcio potenzialmente controllati. Il calcio in entrata rende possibile il rilascio del trasmettitore, che porta alla comparsa di un potenziale generatore all'estremità del nervo sensoriale. Ciascuno stimolo depolarizza la membrana in modi diversi. Lo stimolo salino interagisce con i canali epiteliali del sodio (ENaC), aprendoli al sodio. Uno stimolo acido può aprire autonomamente l'ENaC o, a causa di una diminuzione del pH, chiudere i canali del potassio, il che porterà anche alla depolarizzazione della membrana delle cellule del gusto. Il gusto dolce si verifica a causa dell'interazione di uno stimolo dolce con un recettore accoppiato a proteine G che lo rileva. La proteina G attivata stimola l'adenilato ciclasi, che aumenta i livelli di cAMP e attiva ulteriormente la proteina chinasi dipendente, che, a sua volta, fosforila i canali del potassio e li chiude. Tutto ciò porta anche alla depolarizzazione della membrana. Uno stimolo amaro può depolarizzare la membrana in tre modi: (1) chiudendo i canali del potassio, (2) interagendo con la proteina G (gastducina) per attivare la fosfodiesterasi (PDE), riducendo così i livelli di cAMP. Ciò (per ragioni non del tutto chiare) provoca la depolarizzazione della membrana. (3) Lo stimolo amaro si lega alla proteina G, che può attivare la fosfolipasi C (PLC), determinando un aumento del contenuto di inositolo 1,4,5 trifosfato (IP 3), che porta al rilascio di calcio dalle riserve .
Il glutammato si lega ai canali ionici non selettivi regolati dal glutammato e li apre. Ciò è accompagnato da depolarizzazione e apertura dei canali del calcio voltaggio-dipendenti.
(PIP 2) - fosfatidil inositolo 4,5 bifosfato (DAG) - diacilglicerolo
Riso. 5-11. Meccanismi cellulari della percezione del gusto

Vie centrali del gusto
I corpi cellulari che possiedono le fibre del gusto dei nervi cranici VII, IX e X sono localizzati rispettivamente nei gangli genicolato, petroso e nodulare (Fig. 5-12 B). I processi centrali delle loro fibre afferenti entrano nel midollo allungato, sono inclusi nel tratto solitario e terminano con sinapsi nel nucleo del tratto solitario (nucleo solitario)(Fig. 5-12 A). In un certo numero di animali, comprese alcune specie di roditori, i neuroni del gusto secondari nel nucleo del tratto solitario si proiettano rostralmente al tratto ipsilaterale nucleo parabrachiale.
A sua volta, il nucleo parabrachiale invia proiezioni alla parte parvocellulare (cellulare destra). nucleo ventrale posteromediale (VPM μ) (MK - parte parvocellulare del VPM) talamo (Fig. 5-12 B). Nelle scimmie, le proiezioni del nucleo del tratto solitario al nucleo μ del VSM sono dirette. Il nucleo μ della VZM è associato a due diverse aree del gusto della corteccia cerebrale. Uno di essi fa parte della rappresentazione facciale (SI), l'altro si trova nell'insula (insula- isolotto) (Fig. 5-12 D). La via centrale del gusto è insolita in quanto le sue fibre non viaggiano verso l'altro lato del cervello (a differenza delle vie somatosensoriali, visive e uditive).
Riso. 5-12. Vie che conducono la sensibilità del gusto.
A - terminazione delle fibre afferenti al gusto nel nucleo del tratto solitario e vie ascendenti al nucleo parabrachiale, al talamo ventrobasale e alla corteccia cerebrale. B - distribuzione periferica delle fibre afferenti al gusto. B e D: aree del gusto del talamo e della corteccia cerebrale delle scimmie

Odore
Nei primati e nell'uomo (microsmati) sensibilità olfattiva molto meno sviluppati che nella maggior parte degli animali (macromati). La capacità dei cani di riconoscere un odore attraverso l'olfatto è davvero leggendaria, così come la capacità degli insetti di attrarre individui del sesso opposto con l'aiuto di feromoni. Per quanto riguarda gli esseri umani, l'olfatto gioca un ruolo nella sfera emotiva; gli odori promuovono efficacemente il recupero delle informazioni dalla memoria.
Recettori olfattivi
Il chemiorecettore olfattivo (cellula sensoriale) è un neurone bipolare (Fig. 5-13 B). La sua superficie apicale porta ciglia immobili che rispondono alle sostanze odorose disciolte nello strato di muco che le ricopre. Un assone non mielinizzato si estende dal bordo più profondo della cellula. Gli assoni si uniscono in fasci olfattivi (fila olfattiva), penetrare nel cranio attraverso i fori della lamina cribriforme (lamina cribrosa) osso etmoidale (os etmoidi). Le fibre nervose olfattive terminano nel bulbo olfattivo e le strutture olfattive centrali si trovano alla base del cranio appena sotto il lobo frontale. Le cellule dei recettori olfattivi fanno parte della mucosa della zona olfattiva specializzata del rinofaringe, la cui superficie totale su entrambi i lati è di circa 10 cm 2 (Fig. 5-13 A). Una persona ha circa 10 7 recettori olfattivi. Come le papille gustative, i recettori olfattivi hanno una vita breve (circa 60 giorni) e vengono continuamente sostituiti.
Molecole di sostanze odorose entrano nella zona olfattiva attraverso le narici durante l'inalazione o dalla bocca durante il pasto. I movimenti dell'annusare aumentano l'apporto di queste sostanze, che si combinano temporaneamente con la proteina legante olfattiva del muco secreta dalle ghiandole della mucosa nasale.
Ci sono più sensazioni olfattive primarie che gustative. Esistono odori di almeno sei classi: floreale, etereo(frutta), muschiato, canforato, putrido E caustico. Esempi delle loro fonti naturali includono rispettivamente rosa, pera, muschio, eucalipto, uova marce e aceto. La mucosa olfattiva contiene ancora recettori per il nervo trigemino. Quando si testa clinicamente il senso dell'olfatto, si dovrebbe evitare la stimolazione del dolore o della temperatura di questi recettori somatosensoriali.
Diverse molecole di una sostanza odorosa provocano un potenziale recettore depolarizzante nella cellula sensoriale, innescando una scarica di impulsi nella fibra nervosa afferente. Tuttavia, una risposta comportamentale richiede l’attivazione di un certo numero di recettori olfattivi. Il potenziale del recettore sembra derivare da un aumento della conduttanza del Na+. Allo stesso tempo, la proteina G viene attivata. Di conseguenza, nella trasformazione olfattiva (trasduzione) è coinvolta una cascata di secondi messaggeri.
La codifica olfattiva ha molto in comune con la codifica gustativa. Ciascun chemiorecettore olfattivo risponde a più di una classe di odori. La codifica di una specifica qualità dell'odore è fornita dalle risposte di molti recettori olfattivi e l'intensità della sensazione è determinata dalle caratteristiche quantitative dell'attività impulsiva.
Riso. 5-13. Sensibilità chimica: l'olfatto e le sue basi.
A&B - diagramma della posizione della zona olfattiva della mucosa nel rinofaringe. In alto c'è la lamina cribriforme e sopra c'è il bulbo olfattivo. La mucosa olfattiva si estende anche ai lati del rinofaringe. C e D - chemocettori olfattivi e cellule di supporto. G - epitelio olfattivo. D - diagramma dei processi nei recettori olfattivi

Vie olfattive centrali
La via olfattiva si attiva innanzitutto nel bulbo olfattivo, che appartiene alla corteccia cerebrale. Questa struttura contiene tre tipi di cellule: cellule mitraliche, cellule a ciuffo E interneuroni (cellule granulari, cellule periglomerulari)(Figura 5-14). I dendriti lunghi e ramificati delle cellule mitraliche e a ciuffo formano i componenti postsinaptici dei glomeruli olfattivi (glomeruli). Le fibre afferenti olfattive (provenienti dalla mucosa olfattiva al bulbo olfattivo) si ramificano vicino ai glomeruli olfattivi e terminano in sinapsi sui dendriti delle cellule mitraliche e a ciuffo. In questo caso, sui dendriti delle cellule mitraliche si verifica una significativa convergenza degli assoni olfattivi: sul dendrite di ciascuna cellula mitrale si trovano fino a 1000 sinapsi di fibre afferenti. Le cellule granulari (cellule granulari) e le cellule periglomerulari sono interneuroni inibitori. Formano sinapsi dendrodendritiche reciproche con le cellule mitraliche. Quando le cellule mitraliche vengono attivate, si verifica la depolarizzazione degli interneuroni a contatto con esse, a seguito della quale un neurotrasmettitore inibitorio viene rilasciato nelle loro sinapsi sulle cellule mitraliche. Il bulbo olfattivo riceve input non solo attraverso i nervi olfattivi ipsilaterali, ma anche attraverso il tratto olfattivo controlaterale, che decorre nella commissura anteriore (commissura).
Gli assoni delle cellule mitraliche e del ciuffo lasciano il bulbo olfattivo ed entrano nel tratto olfattivo (Fig. 5-14). A partire da quest'area le connessioni olfattive diventano molto complesse. Il tratto olfattivo lo attraversa nucleo olfattivo anteriore. I neuroni di questo nucleo ricevono connessioni sinaptiche dai neuroni dell'olfatto
bulbi e proiettano attraverso la commissura anteriore al bulbo olfattivo controlaterale. Avvicinandosi alla sostanza perforata anteriore alla base del cervello, il tratto olfattivo si divide nelle strisce olfattive laterali e mediali. Gli assoni della stria olfattiva laterale terminano alle sinapsi dell'area olfattiva primaria, compresa la corteccia prepiriforme (prepiriforme) e, negli animali, il lobo piriforme (piriforme). La striscia olfattiva mediale fornisce proiezioni all'amigdala e alla corteccia basale del prosencefalo.
Va notato che la via olfattiva è l'unico sistema sensoriale senza commutazione sinaptica obbligatoria nel talamo. Probabilmente, l'assenza di tale interruttore riflette l'antichità filogenetica e la relativa primitività del sistema olfattivo. Tuttavia, le informazioni olfattive continuano ad entrare nel nucleo posteromediale del talamo e da lì vengono inviate alla corteccia prefrontale e orbitofrontale.
Gli esami neurologici standard di solito non testano il senso dell’olfatto. Tuttavia, la percezione degli odori può essere testata chiedendo al soggetto di annusare e identificare una sostanza odorosa. Una narice viene esaminata contemporaneamente, l'altra deve essere chiusa. In questo caso, non è possibile utilizzare stimoli così forti come l'ammoniaca, poiché attivano anche le terminazioni del nervo trigemino. Senso dell'olfatto compromesso (anosmia) osservato quando la base del cranio è danneggiata o uno o entrambi i bulbi olfattivi sono compressi da un tumore (ad esempio, con meningioma della fossa olfattiva). Un'aura di odore sgradevole, spesso odore di gomma bruciata, si verifica durante le crisi epilettiche generate nella zona dell'uncus.
Riso. 5-14. Diagramma di una sezione sagittale attraverso il bulbo olfattivo, che mostra le terminazioni delle cellule chemocettrici olfattive sui glomeruli olfattivi e sui neuroni del bulbo olfattivo.
Gli assoni delle cellule mitraliche e del ciuffo escono come parte del tratto olfattivo (a destra)

Struttura dell'occhio
La parete dell'occhio è costituita da tre strati concentrici (conchiglie) (Fig. 5-15 A). Lo strato di supporto esterno, o membrana fibrosa, comprende un trasparente cornea con il suo epitelio, congiuntiva e opaco sclera Lo strato intermedio, o coroide, contiene l'iride (iride) e la coroide stessa. (coroide). IN iris sono presenti fibre muscolari lisce radiali e circolari, che formano il dilatatore e lo sfintere della pupilla (Fig. 5-15 B). Coroide(coroide) è riccamente fornita di vasi sanguigni che nutrono gli strati esterni della retina e contiene anche pigmento. Lo strato neurale interno della parete dell'occhio, o retina, contiene bastoncelli e coni e riveste l'intera superficie interna dell'occhio, ad eccezione del "punto cieco" - disco ottico(Fig. 5-15 A). Gli assoni delle cellule gangliari della retina convergono sul disco, formando il nervo ottico. L'acuità visiva più alta si trova nella parte centrale della retina, la cosiddetta macula(macula lutea). La parte centrale della macula è depressa nella forma fovea(fovea centrale)- aree di messa a fuoco delle immagini visive. La parte interna della retina è nutrita dai rami dei suoi vasi centrali (arterie e vene), che entrano insieme al nervo ottico, poi si ramificano nella zona del disco e divergono lungo la superficie interna della retina (Fig. 5-15 B), senza toccare la macula.
Oltre alla retina, ci sono altre formazioni nell'occhio: lente- una lente che focalizza la luce sulla retina; strato di pigmento, limitare la diffusione della luce; umore acqueo E corpo vitreo. L'umor acqueo è il fluido che costituisce l'ambiente delle camere anteriore e posteriore dell'occhio e l'umor vitreo riempie lo spazio interno dell'occhio dietro il cristallino. Entrambe le sostanze aiutano a mantenere la forma dell'occhio. L'umor acqueo viene secreto dall'epitelio ciliato della camera posteriore, quindi circola attraverso la pupilla nella camera anteriore e da lì
passa Canale di Schlemm nel flusso sanguigno venoso (Fig. 5-15 B). La pressione intraoculare dipende dalla pressione dell'umor acqueo (normalmente è inferiore a 22 mm Hg), che non deve superare i 22 mm Hg. Il vitreo è un gel costituito da fluido extracellulare con collagene e acido ialuronico; a differenza dell'umor acqueo, viene sostituito molto lentamente.
Se l'assorbimento dell'umore acqueo è compromesso, la pressione intraoculare aumenta e si sviluppa il glaucoma. Quando la pressione intraoculare aumenta, l’afflusso di sangue alla retina diventa difficile e l’occhio può diventare cieco.
Numerose funzioni oculari dipendono dall'attività muscolare. I muscoli oculari estrinseci, attaccati all'esterno dell'occhio, dirigono i movimenti dei bulbi oculari verso il bersaglio visivo. Questi muscoli sono innervati oculomotore(nervo oculomotorio),blocco(N. trocleare) E deviante(N. abducente)nervi. Ci sono anche muscoli oculari interni. Grazie al muscolo che dilata la pupilla (dilatatore della pupilla), e il muscolo che restringe la pupilla (sfintere pupillare) L'iride agisce come un diaframma e regola il diametro della pupilla in modo simile all'apertura di una fotocamera, che controlla la quantità di luce che entra. Il dilatatore pupillare è attivato dal sistema nervoso simpatico e lo sfintere è attivato dal sistema nervoso parasimpatico (tramite il sistema nervoso oculomotore).
La forma del cristallino è determinata anche dal lavoro dei muscoli. Il cristallino è sospeso e tenuto in posizione dietro l'iride da fibre ciliare(ciliare o cinnova) cintura, attaccato alla capsula pupillare e al corpo ciliare. La lente è circondata da fibre muscolo ciliare, agendo come uno sfintere. Quando queste fibre sono rilassate, la tensione delle fibre della zonula allunga il cristallino, appiattendolo. Contraendosi, il muscolo ciliare contrasta la tensione delle fibre della cintura, che consente alla lente elastica di assumere una forma più convessa. Il muscolo ciliare è attivato dal sistema nervoso parasimpatico (tramite il sistema nervoso oculomotore).
Riso. 5-15. Visione.
A - diagramma di una sezione orizzontale dell'occhio destro. B - la struttura della parte anteriore dell'occhio nella regione del limbo (la giunzione tra cornea e sclera), il corpo ciliare e il cristallino. B - superficie posteriore (inferiore) dell'occhio umano; vista attraverso un oftalmoscopio. I rami delle arterie e delle vene centrali emergono dall'area della testa del nervo ottico. Non lontano dal disco ottico, sul lato temporale, si trova la fossa centrale (CF). Notare la distribuzione degli assoni delle cellule gangliari (linee sottili) convergenti nel disco ottico.
Ulteriori disegni forniscono dettagli sulla struttura dell'occhio e sui meccanismi di funzionamento delle sue strutture (spiegazioni nei disegni)


Riso. 5-15.2.

Riso. 5-15.3.

Riso. 5-15.4.

Riso. 5-15.5.
Sistema ottico dell'occhio
La luce entra nell'occhio attraverso la cornea e attraversa fluidi e strutture trasparenti disposti successivamente: la cornea, l'umor acqueo, il cristallino e l'umor vitreo. La loro totalità è chiamata dispositivo diottrico. In condizioni normali ciò accade rifrazione(rifrazione) dei raggi luminosi provenienti da un bersaglio visivo da parte della cornea e del cristallino in modo che i raggi siano focalizzati sulla retina. Il potere rifrattivo della cornea (il principale elemento rifrattivo dell'occhio) è pari a 43 diottrie * [“D”, diottria, è un'unità di potere rifrattivo (ottico) pari al reciproco della lunghezza focale della lente (lente ), espresso in metri]. La convessità della lente può cambiare e il suo potere di rifrazione varia tra 13 e 26 D. Grazie a ciò, la lente offre alloggio al bulbo oculare per oggetti situati a distanza vicina o lontana. Quando, ad esempio, i raggi luminosi provenienti da un oggetto distante entrano in un occhio normale (con un muscolo ciliare rilassato), il bersaglio viene messo a fuoco sulla retina. Se l'occhio è diretto verso un oggetto vicino, i raggi luminosi vengono prima focalizzati dietro la retina (cioè l'immagine sulla retina diventa sfocata) finché non avviene l'accomodamento. Il muscolo ciliare si contrae, indebolendo la tensione delle fibre della zonula, la curvatura del cristallino aumenta e, di conseguenza, l'immagine viene focalizzata sulla retina.
La cornea e il cristallino insieme formano una lente convessa. I raggi di luce provenienti da un oggetto passano attraverso il punto nodale del cristallino e formano un'immagine invertita sulla retina, come in una macchina fotografica. La retina elabora una sequenza continua di immagini e invia anche messaggi al cervello sui movimenti degli oggetti visivi, segnali minacciosi, cambiamenti periodici di luce e oscurità e altri dati visivi sull'ambiente esterno.
Sebbene l’asse ottico dell’occhio umano passi per il punto nodale del cristallino e per il punto della retina compreso tra la fovea e la testa del nervo ottico, il sistema oculomotore orienta il bulbo oculare verso una regione dell’oggetto chiamata punto di fissazione. Da questo punto un fascio di luce attraversa il punto nodale e si concentra nella fovea centrale. Pertanto, il raggio passa lungo l'asse visivo. I raggi provenienti da altre parti dell'oggetto vengono focalizzati nell'area della retina attorno alla fovea centrale (Fig. 5-16 A).
La messa a fuoco dei raggi sulla retina dipende non solo dal cristallino, ma anche dall'iride. L'iride svolge il ruolo di apertura della fotocamera e regola non solo la quantità di luce che entra nell'occhio, ma, soprattutto, la profondità del campo visivo e l'aberrazione sferica dell'obiettivo. Al diminuire del diametro della pupilla, aumenta la profondità del campo visivo e i raggi luminosi vengono diretti attraverso la parte centrale della pupilla, dove l'aberrazione sferica è minima. Le modifiche al diametro della pupilla avvengono automaticamente, ad es. di riflesso, quando si regola (accomodamento) l'occhio per esaminare oggetti vicini. Pertanto, durante la lettura o altre attività oculari che comportano la discriminazione di piccoli oggetti, la qualità dell'immagine viene migliorata dal sistema ottico dell'occhio. Un altro fattore che influisce sulla qualità dell'immagine è la diffusione della luce. Viene minimizzato limitando il fascio luminoso, nonché il suo assorbimento da parte del pigmento della coroide e dello strato pigmentato della retina. Sotto questo aspetto, l'occhio ricorda ancora una volta una macchina fotografica. Lì, la diffusione della luce viene impedita anche limitando il fascio di raggi e il suo assorbimento mediante vernice nera che ricopre la superficie interna della camera.
La messa a fuoco dell'immagine viene interrotta se la dimensione dell'occhio non corrisponde al potere di rifrazione della diottria. A miopia(miopia) le immagini di oggetti distanti vengono messe a fuoco davanti alla retina, senza raggiungerla (Fig. 5-16 B). Il difetto viene corretto utilizzando lenti concave. E viceversa, quando ipermetropia(ipermetropia) - le immagini di oggetti distanti sono focalizzate dietro la retina. Per risolvere il problema sono necessarie lenti convesse (Fig. 5-16 B). È vero, l'immagine può essere temporaneamente messa a fuoco a causa dell'accomodamento, ma questo fa stancare i muscoli ciliari e gli occhi. A astigmatismo c'è un'asimmetria tra i raggi di curvatura delle superfici della cornea o del cristallino (e talvolta della retina) su piani diversi. Per la correzione vengono utilizzate lenti con raggi di curvatura appositamente selezionati.
L'elasticità della lente diminuisce gradualmente con l'età. Di conseguenza, l'efficienza della sua accomodazione diminuisce quando si osservano oggetti vicini. (presbiopia). In giovane età, il potere di rifrazione della lente può variare in un ampio intervallo, fino a 14 D. All'età di 40 anni, questo intervallo si dimezza e dopo 50 anni scende a 2 D e inferiore. La presbiopia si corregge con lenti convesse.
Riso. 5-16. Sistema ottico dell'occhio.
A - somiglianza tra i sistemi ottici dell'occhio e della macchina fotografica. B - accomodazione e suoi disturbi: 1 - emmetropia - accomodazione normale dell'occhio. I raggi di luce provenienti da un oggetto visivo distante vengono focalizzati sulla retina (diagramma superiore) e la focalizzazione dei raggi provenienti da un oggetto vicino avviene come risultato dell'accomodamento (diagramma inferiore); 2 - miopia; l'immagine di un oggetto visivo distante viene messa a fuoco davanti alla retina; per la correzione sono necessarie lenti concave; 3 - ipermetropia; l'immagine è focalizzata dietro la retina (diagramma in alto), richiedendo lenti convesse per la correzione (diagramma in basso)

Organo dell'udito
Il sistema uditivo periferico, l’orecchio, si divide in orecchio esterno, medio ed interno
(Fig. 5-17 A). Orecchio esterno
L'orecchio esterno è costituito dal padiglione auricolare, dal canale uditivo esterno e dal canale uditivo. Le ghiandole ceruminose delle pareti del canale uditivo secernono cerume- sostanza protettiva cerosa. Il padiglione auricolare (almeno negli animali) dirige il suono nel condotto uditivo. Il suono viene trasmesso attraverso il canale uditivo al timpano. Nell'uomo, il canale uditivo ha una frequenza di risonanza di circa 3500 Hz e limita la frequenza dei suoni che raggiungono il timpano.
Orecchio medio
L'orecchio esterno è separato dall'orecchio medio timpano(Fig. 5-17B). L'orecchio medio è pieno d'aria. Una catena di ossicini collega il timpano alla finestra ovale, che si apre nell'orecchio interno. Non lontano dalla finestra ovale c'è una finestra rotonda, che collega anche l'orecchio medio con l'orecchio interno (Fig. 5-17 B). Entrambi i fori sono coperti da una membrana. La catena degli ossicini uditivi comprende martello(martello),incudine(incudine) E staffa(staffa). La base della staffa a forma di piatto si adatta perfettamente alla finestra ovale. Dietro la finestra ovale c'è un liquido pieno vestibolo(vestibolo)- Parte lumache(coclea) orecchio interno. Il vestibolo è solidale con una struttura tubolare - vestibolo della scala(scala vestiboli- scala vestibolare). Le vibrazioni del timpano causate dalle onde di pressione sonora si trasmettono lungo la catena degli ossicini e spingono la staffa nella finestra ovale (Fig. 5-17 B). I movimenti della placca della staffa sono accompagnati da fluttuazioni di liquidi nel vestibolo della scala. Le onde di pressione si propagano attraverso il liquido e vengono trasmesse membrana principale (basilare). lumache a
scala timpanica(scala timpani)(vedi sotto), facendo inarcare la membrana della finestra rotonda verso l'orecchio medio.
Il timpano e la catena degli ossicini uditivi eseguono l'adattamento dell'impedenza. Il fatto è che l'orecchio deve distinguere le onde sonore che si propagano nell'aria, mentre il meccanismo di conversione nervosa del suono dipende dai movimenti della colonna di fluido nella coclea. Pertanto è necessaria una transizione dalle vibrazioni dell'aria alle vibrazioni del liquido. L'impedenza acustica dell'acqua è molto più alta di quella dell'aria, quindi senza uno speciale dispositivo di adattamento dell'impedenza, la maggior parte del suono che entra nell'orecchio verrebbe riflesso. L'adattamento dell'impedenza nell'orecchio dipende da:
rapporto tra le superfici della membrana timpanica e della finestra ovale;
vantaggio meccanico del design della leva sotto forma di una catena di ossa articolate in modo mobile.
L'efficacia del meccanismo di adattamento dell'impedenza corrisponde ad un miglioramento dell'udibilità di 10-20 dB.
L'orecchio medio svolge anche altre funzioni. Contiene due muscoli: muscolo tensore del timpano(m. tensore del timpano- innervato dal nervo trigemino), e muscolo stapedio
(m. stapedio- innervato dal nervo facciale). Il primo è attaccato al martello, il secondo alla staffa. Contraendosi riducono il movimento degli ossicini uditivi e riducono la sensibilità dell'apparato acustico. Ciò aiuta a proteggere l'udito dai suoni dannosi, ma solo se il corpo li prevede. Un'esplosione improvvisa può danneggiare l'apparato acustico, poiché la contrazione riflessa dei muscoli dell'orecchio medio viene ritardata. La cavità dell'orecchio medio è collegata alla faringe attraverso Tromba d'Eustachio. Grazie a questo passaggio la pressione nell'orecchio esterno e medio viene equalizzata. Se il liquido si accumula nell’orecchio medio a causa di un’infiammazione, il lume della tuba di Eustachio potrebbe chiudersi. La differenza di pressione che ne risulta tra l'orecchio esterno e quello medio provoca dolore a causa della tensione del timpano, che può persino rompersi. Le differenze di pressione possono verificarsi in aereo e durante le immersioni.
Riso. 5-17. Udito.
A - schema generale dell'orecchio esterno, medio ed interno. B - schema del timpano e della catena degli ossicini uditivi. B - il diagramma spiega come, quando la placca ovale della staffa viene spostata, il fluido si muove nella coclea e la finestra rotonda si piega

Orecchio interno
L'orecchio interno comprende i labirinti ossei e membranosi. Costituiscono la coclea e l'apparato vestibolare.
La coclea è un tubo attorcigliato a forma di spirale. Negli esseri umani, la spirale ha 2 giri e mezzo; il tubo inizia con una base larga e termina con un apice ristretto. La coclea è formata dall'estremità rostrale dei labirinti ossei e membranosi. Nell'uomo l'apice della coclea si trova sul piano laterale (Fig. 5-18 A).
Labirinto osseo (labirinto osseo) La lumaca comprende diverse camere. Lo spazio vicino alla finestra ovale è chiamato vestibolo (Fig. 5-18 B). Il vestibolo passa nella scala vestibolo, un tubo a spirale che prosegue fino all'apice della coclea. Lì il vestibolo della scala si collega attraverso l'apertura della coclea (elicotrema) con una scala a tamburo; questo è un altro tubo a spirale che corre indietro lungo la coclea e termina nella finestra rotonda (Fig. 5-18 B). Viene chiamata l'asta ossea centrale attorno alla quale sono attorcigliate le scale a spirale asta della coclea(modiolo coclea).
Riso. 5-18. La struttura della lumaca.
A - posizione relativa della coclea e dell'apparato vestibolare dell'orecchio medio ed esterno umano. B - rapporto tra gli spazi della coclea

Organo di Corti
Labirinto membranoso (labirinto membranaceo) vengono anche chiamate lumache scale intermedie(scala media) O condotto cocleare(dotto cocleare).È un tubo membranoso, appiattito, a spirale, lungo 35 mm, situato tra la scala vestibolare e la scala timpanica. Una parete della scala media è formata dalla membrana basilare, l'altra... Membrana Reissner, terzo - stria vascolare(stria vascolare)(Fig. 5-19 A).
La coclea è piena di liquido. Nella scala vestibolo e nella scala timpani c'è perilinfa, simile nella composizione al liquido cerebrospinale. La scala centrale contiene endolinfa, che è significativamente diverso dal liquido cerebrospinale. Questo fluido è ricco di K+ (circa 145 mM) e basso di Na+ (circa 2 mM), quindi è simile all'ambiente intracellulare. Poiché l'endolinfa ha una carica positiva (circa +80 mV), le cellule ciliate all'interno della coclea hanno un elevato gradiente di potenziale transmembrana (circa 140 mV). L'endolinfa viene secreta dalla stria vascolare e il drenaggio avviene attraverso il dotto endolinfatico nei seni venosi della dura madre.
Si chiama l'apparato nervoso per la conversione del suono "organo di Corti"(Fig. 5-19B). Si trova nella parte inferiore del condotto cocleare sulla membrana basilare ed è costituito da diversi componenti: tre file di cellule ciliate esterne, una fila di cellule ciliate interne, una membrana tettoria gelatinosa e diversi tipi di cellule di supporto. L'organo umano del Corti contiene 15.000 cellule ciliate esterne e 3.500 interne. La struttura portante dell'organo del Corti è costituita da cellule colonnari e dalla lamina reticolare (membrana reticolare). Dalle punte delle cellule ciliate sporgono fasci di stereociglia - ciglia, immerse nella membrana tettoria.
L'organo del Corti è innervato dalle fibre nervose della parte cocleare dell'ottavo nervo cranico. Queste fibre (ci sono 32.000 assoni afferenti uditivi nell'uomo) appartengono alle cellule sensoriali del ganglio spirale, contenuto nella diafisi centrale dell'osso. Le fibre afferenti entrano nell'organo del Corti e terminano alla base delle cellule ciliate (Fig. 5-19 B). Le fibre che forniscono le cellule ciliate esterne entrano attraverso il tunnel del Corti, un'apertura sotto le cellule colonnari.
Riso. 5-19. Lumaca.
A - diagramma di una sezione trasversale attraverso la coclea dall'angolo mostrato nel riquadro di Fig. 5-20 B. B - struttura dell'organo del Corti

Conversione (trasduzione) del suono
L'organo di Corti trasforma il suono nel modo seguente. Raggiungendo il timpano, le onde sonore provocano le sue vibrazioni, che vengono trasmesse al fluido che riempie la scala vestibolare e la scala timpanica (Fig. 5-20 A). L'energia idraulica porta allo spostamento della membrana basilare e con essa dell'organo del Corti (Fig. 5-20 B). La forza di taglio sviluppata come risultato dello spostamento della membrana basilare rispetto alla membrana tettoria provoca la flessione delle stereociglia delle cellule ciliate. Quando le stereociglia si piegano verso quella più lunga, la cellula ciliata si depolarizza; quando si piegano nella direzione opposta, si iperpolarizza.
Tali cambiamenti nel potenziale di membrana delle cellule ciliate sono causati da cambiamenti nella conduttività cationica della membrana al loro apice. Il gradiente potenziale che determina l'ingresso degli ioni nella cellula ciliata è la somma del potenziale di riposo della cellula e della carica positiva dell'endolinfa. Come notato sopra, la differenza di potenziale transmembrana totale è di circa 140 mV. Lo spostamento nella conduttività della membrana della parte superiore delle cellule ciliate è accompagnato da una significativa corrente ionica, che crea il potenziale recettore di queste cellule. Un indicatore della corrente ionica è quello extracellulare registrato potenziale microfonico della coclea- un processo oscillatorio, la cui frequenza corrisponde alle caratteristiche dello stimolo acustico. Questo potenziale è la somma dei potenziali recettoriali di un certo numero di cellule ciliate.
Come i fotorecettori retinici, le cellule ciliate rilasciano un neurotrasmettitore eccitatorio (glutammato o aspartato) dopo la depolarizzazione. Sotto l'influenza del neurotrasmettitore, nelle terminazioni delle fibre afferenti cocleari si forma un potenziale generatore, sulle quali le cellule ciliate formano sinapsi. Quindi, la trasformazione del suono termina con le vibrazioni della basilare
le membrane portano a scariche periodiche di impulsi nelle fibre afferenti del nervo uditivo. L'attività elettrica di molte fibre afferenti può essere registrata a livello extracellulare come potenziale d'azione composto.
Si è scoperto che solo un piccolo numero di afferenze cocleari risponde al suono di una certa frequenza. L'insorgenza della risposta dipende dalla posizione delle terminazioni nervose afferenti lungo l'organo del Corti, poiché a parità di frequenza del suono l'ampiezza dello spostamento della membrana basilare non è la stessa nelle diverse parti di essa. Ciò è in parte dovuto alle differenze nella larghezza della membrana e nella tensione lungo l'organo del Corti. In precedenza, si riteneva che la differenza nella frequenza di risonanza in diverse parti della membrana basilare fosse spiegata dalle differenze nella larghezza e nella tensione di queste aree. Ad esempio, alla base della coclea la larghezza della membrana basilare è di 100 μm e all'apice è di 500 μm. Inoltre, alla base della coclea la tensione della membrana è maggiore che all'apice. Pertanto, la zona della membrana vicino alla base dovrebbe vibrare ad una frequenza più alta rispetto alla zona vicino alla sommità, come le corde corte di uno strumento musicale. Tuttavia, gli esperimenti hanno dimostrato che la membrana basilare vibra come una singola unità e le onde viaggianti la seguono. Con i toni ad alta frequenza, l'ampiezza delle vibrazioni ondulatorie della membrana basilare è massima più vicino alla base della coclea e con i toni a bassa frequenza è all'apice. In effetti, la membrana basilare funge da analizzatore di frequenza; lo stimolo è distribuito lungo l'organo del Corti in modo tale che cellule ciliate di diversa localizzazione rispondano a suoni di frequenze diverse. Questa conclusione costituisce la base teorie del luogo. Inoltre, le cellule ciliate situate lungo l'organo del Corti sono sintonizzate su diverse frequenze del suono a causa delle loro proprietà biofisiche e delle caratteristiche delle stereociglia. Grazie a questi fattori si ottiene una cosiddetta mappa tonotopica della membrana basilare e dell'organo del Corti.
Riso. 5-20. Organo di Corti

Sezione periferica del sistema vestibolare
Il sistema vestibolare percepisce le accelerazioni angolari e lineari della testa. I segnali provenienti da questo sistema attivano movimenti della testa e degli occhi che forniscono un’immagine visiva stabile sulla retina, nonché la correzione della postura del corpo per mantenere l’equilibrio.
Struttura del labirinto vestibolare
Come la coclea, l'apparato vestibolare è un labirinto membranoso situato nel labirinto osseo (Fig. 5-21 A). Su ciascun lato della testa l'apparato vestibolare è formato da tre canali semicircolari [orizzontale, verticale anteriore (superiore) E posteriore verticale] e due organi otolitici. Tutte queste strutture sono immerse nella perilinfa e piene di endolinfa. L'organo otolitico è costituito da utricolo(utricolo- sacco ellittico, otricolo) e sacculo(sacculo- sacchetto sferico). Un'estremità di ciascun canale semicircolare viene espansa nella forma ampolle. Tutti i canali semicircolari entrano nell'utricolo. L'utricolo e il sacculo comunicano tra loro attraverso condotto di collegamento(ductus reuniens). Si comincia da lui condotto endolinfatico(dotto endolinfatico), termina con un sacco endolinfatico che forma una connessione con la coclea. Attraverso questa connessione, l'endolinfa secreta dalla stria vascolare della coclea entra nell'apparato vestibolare.
Ciascuno dei canali semicircolari su un lato della testa si trova sullo stesso piano del canale corrispondente sull'altro lato. Grazie a ciò, le aree corrispondenti dell'epitelio sensoriale di due canali accoppiati percepiscono i movimenti della testa su qualsiasi piano. La Figura 5-21 B mostra l'orientamento dei canali semicircolari su entrambi i lati della testa; si noti che la coclea si trova rostralmente all'apparato vestibolare e che l'apice della coclea si trova lateralmente. I due canali orizzontali su entrambi i lati della testa formano una coppia, così come i due canali anteriori verticali e i due canali posteriori verticali. I canali orizzontali hanno una caratteristica interessante: loro
sono sul piano orizzontale quando la testa è inclinata di 30°. L'utricolo è orientato quasi orizzontalmente e il sacculo è orientato verticalmente.
L'ampolla di ciascun canale semicircolare contiene l'epitelio sensoriale nella forma del cosiddetto pettine ampollare(crista ampollare) con cellule ciliate vestibolari (uno schema del taglio attraverso la cresta ampollare è mostrato in Fig. 5-21 B). Sono innervati dalle fibre afferenti primarie del nervo vestibolare, che fa parte dell'VIII nervo cranico. Ciascuna cellula ciliata dell'apparato vestibolare, come cellule simili della coclea, porta un fascio di stereocilia (cilia) al suo apice. Tuttavia, a differenza delle cellule cocleari, le cellule ciliate vestibolari ne hanno ancora una kinocilium. Tutte le ciglia delle cellule ampollari sono immerse in una struttura gelatinosa - cupola, che si trova attraverso l'ampolla, bloccandone completamente il lume. Con l'accelerazione angolare (rotazionale) della testa, la cupola devia; Le ciglia delle cellule ciliate si piegano di conseguenza. La cupola ha lo stesso peso specifico (densità) dell'endolinfa, quindi non è influenzata dall'accelerazione lineare creata dalla gravità (accelerazione gravitazionale). La Figura 5-21 D, E mostra la posizione della cupola prima di girare la testa (D) e durante il giro (E).
L'epitelio sensoriale degli organi otolitici è punto del sacco ellittico(macula utricolica) E punto del sacco sferico(macula sacculi)(Fig. 5-21 E). Ogni macula (macchia) è rivestita da cellule ciliate vestibolari. Le loro stereocilia e chinociglio, così come le ciglia delle cellule ciliate dell'ampolla, sono immerse in una massa gelatinosa. La differenza tra la massa gelatinosa degli organi otolitici è che contiene numerosi otoliti (minuscole inclusioni "pietrose") - cristalli di carbonato di calcio (calcite). Viene chiamata la massa gelatinosa insieme ai suoi otoliti membrana dell'otolite. A causa della presenza di cristalli di calcite, il peso specifico (densità) della membrana otolitica è circa due volte superiore a quello dell'endolinfa, quindi la membrana otolitica viene facilmente spostata sotto l'influenza dell'accelerazione lineare creata dalla gravità. L'accelerazione angolare della testa non porta a un tale effetto, poiché la membrana otolitica quasi non sporge nel lume del labirinto membranoso.
Riso. 5-21. Sistema vestibolare.
A - struttura dell'apparato vestibolare. B - vista dall'alto della base del cranio. L'orientamento delle strutture dell'orecchio interno è evidente. Prestare attenzione alle coppie di canali semicircolari controlaterali situati sullo stesso piano (due canali orizzontali, superiore - anteriore e inferiore - posteriore). B - schema dell'incisione attraverso il pettine ampollare. La stereocilia e il chinociglio di ciascuna cellula ciliata sono incorporati nella cupola. Posizione della cupola prima di girare la testa (D) e durante la rotazione (E). E - struttura degli organi otolitici

Innervazione dell'epitelio sensoriale dell'apparato vestibolare
Sono localizzati i corpi cellulari delle fibre afferenti primarie del nervo vestibolare Gangli delle scarpe. Come i neuroni gangliari a spirale, queste sono cellule bipolari; i loro corpi e assoni sono mielinizzati. Il nervo vestibolare invia un ramo separato a ciascuna macula dell'epitelio sensoriale (Fig. 5-22 A). Il nervo vestibolare viaggia insieme ai nervi cocleare e facciale nel canale uditivo interno (meato acustico interno) teschi
Cellule ciliate vestibolari divisi in due tipologie (Fig. 5-22 B). Le cellule di tipo I hanno la forma di una fiasca e formano connessioni sinaptiche con le terminazioni a calice delle afferenze primarie.
affitti del nervo vestibolare. Le cellule di tipo II sono cilindriche, i loro contatti sinaptici sono sulle stesse afferenze primarie. Le sinapsi delle fibre efferenti vestibolari si trovano alle terminazioni delle afferenze primarie delle cellule di tipo I. Con le cellule di tipo II, le fibre efferenti vestibolari formano contatti sinaptici diretti. Questa organizzazione è simile a quella discussa sopra quando si descrivono i contatti delle fibre afferenti ed efferenti del nervo cocleare con le cellule ciliate interne ed esterne dell'organo del Corti. La presenza di terminazioni nervose efferenti sulle cellule di tipo II può spiegare l'irregolarità delle scariche nelle afferenze di queste cellule.
Riso. 5-22.
A - innervazione del labirinto membranoso. B - cellule ciliate vestibolari di tipo I e II. Riquadro a destra: vista dall'alto di stereocilia e chinocilia. Notare dove si trovano i contatti delle fibre afferenti ed efferenti

Trasformazione (trasduzione) dei segnali vestibolari
Come le cellule ciliate cocleari, la membrana delle cellule ciliate vestibolari è funzionalmente polarizzata. Quando le stereociglia si piegano verso il ciglio più lungo (cinocilio), la conduttanza cationica della membrana apicale della cellula aumenta e le cellule ciliate vestibolari si depolarizzano (Figura 5-23 B). Al contrario, quando le stereocilia si inclinano nella direzione opposta, si verifica l’iperpolarizzazione della cellula. Un neurotrasmettitore eccitatorio (glutammato o aspartato) viene rilasciato tonicamente (costantemente) dalla cellula ciliata, in modo che la fibra afferente su cui questa cellula forma una sinapsi genera un'attività impulsiva spontaneamente, in assenza di segnali. Quando la cellula si depolarizza, aumenta il rilascio del neurotrasmettitore e aumenta la frequenza di scarica nella fibra afferente. Nel caso dell'iperpolarizzazione, invece, viene rilasciata una quantità minore di neurotrasmettitore e la frequenza di scarica diminuisce fino a quando l'impulso si arresta completamente.
Canali semicircolari
Come già accennato, quando la testa gira, le cellule ciliate dell'ampolla ricevono informazioni sensoriali, alle quali vengono inviate
cervello. Il meccanismo di questo fenomeno è che le accelerazioni angolari (giri della testa) sono accompagnate dalla flessione delle ciglia sulle cellule ciliate della cresta ampollare e, di conseguenza, uno spostamento del potenziale di membrana e un cambiamento nella quantità di neurotrasmettitore rilasciato. Durante le accelerazioni angolari, l'endolinfa, a causa della sua inerzia, si sposta rispetto alla parete del labirinto membranoso e preme sulla cupola. La forza di taglio fa piegare le ciglia. Tutte le ciglia delle cellule di ciascuna cresta ampollare sono orientate nella stessa direzione. Nel canale semicircolare orizzontale le ciglia sono rivolte verso l'utricolo; nelle ampolle degli altri due canali semicircolari le ciglia sono rivolte in direzione opposta all'utricolo.
I cambiamenti nella scarica delle afferenze del nervo vestibolare sotto l'influenza dell'accelerazione angolare possono essere discussi usando l'esempio del canale semicircolare orizzontale. Le chinocilia di tutte le cellule ciliate sono solitamente rivolte verso l'utricolo. Di conseguenza, quando le ciglia si piegano verso l'utricolo, la frequenza della scarica afferente aumenta, mentre quando si allontanano dall'utricolo diminuisce. Quando giri la testa a sinistra, l'endolinfa nei canali semicircolari orizzontali si sposta a destra. Di conseguenza, le ciglia delle cellule ciliate nel canale sinistro si piegano verso l'utricolo e nel canale destro si allontanano dall'utricolo. Di conseguenza, la frequenza di scarica nelle afferenze del canale orizzontale sinistro aumenta e nelle afferenze di destra diminuisce.
Riso. 5-23. Trasformazioni meccaniche nelle cellule ciliate.
A - Cellula ciliata;
B - Deformazione meccanica positiva; B - Deformazione meccanica negativa; G - Sensibilità meccanica della cellula ciliata;
D - polarizzazione funzionale delle cellule ciliate vestibolari. Quando le stereocilia si piegano verso il chinocilio, la cellula ciliata viene depolarizzata e si verifica l'eccitazione nella fibra afferente. Quando le stereociglia si allontanano dal chinocilio, la cellula ciliata si iperpolarizza e la scarica afferente si indebolisce o si arresta

Diversi importanti riflessi spinali vengono attivati dai recettori dell'allungamento muscolare: i fusi muscolari e l'apparato tendineo del Golgi. Questo riflesso di stiramento muscolare (riflesso miotatico) E riflesso miotatico inverso, necessario per mantenere la postura.
Un altro riflesso significativo è il riflesso di flessione, causato da segnali provenienti da vari recettori sensoriali nella pelle, nei muscoli, nelle articolazioni e negli organi interni. Le fibre afferenti che causano questo riflesso vengono spesso chiamate afferenze del riflesso di flessione.
La struttura e le funzioni del fuso muscolare
La struttura e la funzione dei fusi muscolari sono molto complesse. Sono presenti nella maggior parte dei muscoli scheletrici, ma sono particolarmente abbondanti nei muscoli che richiedono una regolazione precisa del movimento (ad esempio, nei piccoli muscoli della mano). Per quanto riguarda i muscoli di grandi dimensioni, i fusi muscolari sono più abbondanti nei muscoli contenenti molte fibre fasiche lente (fibre di tipo I; fibre a contrazione lenta).
Il fuso è costituito da un fascio di fibre muscolari modificate innervate sia da assoni sensoriali che motori (Fig. 5-24 A). Il diametro del fuso muscolare è di circa 100 cm, la lunghezza arriva fino a 10 mm. La parte innervata del fuso muscolare è racchiusa in una capsula di tessuto connettivo. Il cosiddetto spazio linfatico della capsula è pieno di liquido. Il fuso muscolare si trova liberamente tra le fibre muscolari normali. La sua estremità distale è attaccata a endomisio- rete di tessuto connettivo all'interno del muscolo. I fusi muscolari si trovano paralleli alle normali fibre muscolari striate.
Il fuso muscolare contiene fibre muscolari modificate chiamate fibre muscolari intrafusali, a differenza del solito - fibre muscolari extrafusali. Le fibre intrafusali sono molto più sottili delle fibre extrafusali e sono troppo deboli per partecipare alla contrazione muscolare. Esistono due tipi di fibre muscolari intrafusali: con sacca nucleare e con catena nucleare (Fig. 5-24 B). I loro nomi sono legati all'organizzazione dei nuclei cellulari. Fibre con una borsa nucleare più grandi delle fibre
catena nucleare, e i loro nuclei sono strettamente imballati nella parte centrale della fibra come un sacchetto di arance. IN fibre della catena nucleare tutti i nuclei si trovano in una riga.
I fusi muscolari ricevono un’innervazione complessa. L'innervazione sensoriale è costituita da un gruppo Ia assone afferente e diversi afferenze del II gruppo(Fig. 5-24B). Le afferenze del gruppo Ia appartengono alla classe degli assoni sensoriali di diametro maggiore con una velocità di conduzione da 72 a 120 m/s; Gli assoni del gruppo II hanno un diametro intermedio e conducono impulsi a velocità comprese tra 36 e 72 m/s. Si forma l'assone afferente del gruppo Ia finale primario avvolgendosi a spirale attorno a ciascuna fibra intrafusale. Le terminazioni primarie sono presenti sulle fibre intrafusali di entrambi i tipi, il che è importante per l'attività di questi recettori. Forma delle afferenze del II gruppo finali secondari su fibre con una catena nucleare.
L'innervazione motoria dei fusi muscolari è fornita da due tipi di assoni γ-efferenti (Fig. 5-24 B). Dinamicoγ -efferenti terminare su ciascuna fibra con un sacchetto nucleare, staticoγ -efferenti- su fibre con catena nucleare. Gli assoni γ-efferenti sono più sottili degli α-efferenti delle fibre muscolari extrafusali, quindi conducono l'eccitazione a una velocità inferiore.
Il fuso muscolare risponde all'allungamento muscolare. La Figura 5-24 B mostra il cambiamento nell'attività afferente degli assoni mentre il fuso muscolare passa da uno stato accorciato durante la contrazione delle fibre extrafusali ad uno stato allungato durante l'allungamento muscolare. La contrazione delle fibre muscolari extrafusali provoca un accorciamento del fuso muscolare poiché si trova parallelo alle fibre extrafusali (vedi sopra).
L'attività delle afferenze dei fusi muscolari dipende dallo stiramento meccanico delle terminazioni afferenti sulle fibre intrafusali. Quando le fibre extrafusali si contraggono, la fibra muscolare si accorcia, la distanza tra le spire della terminazione nervosa afferente diminuisce e la frequenza di scarica nell'assone afferente diminuisce. Al contrario, quando l'intero muscolo viene allungato, anche il fuso muscolare si allunga (perché le sue estremità sono attaccate alla rete di tessuto connettivo all'interno del muscolo) e l'allungamento dell'estremità afferente aumenta la frequenza della scarica dell'impulso.
Riso. 5-24. Recettori sensoriali responsabili della causa dei riflessi spinali.
A - diagramma del fuso muscolare. B - fibre intrafusali con una sacca nucleare e una catena nucleare; la loro innervazione sensoriale e motoria. B - cambiamenti nella frequenza della scarica dell'impulso dell'assone afferente del fuso muscolare durante l'accorciamento del muscolo (durante la sua contrazione) (a) e durante l'allungamento del muscolo (durante il suo allungamento) (b). B1 - durante la contrazione muscolare, il carico sul fuso muscolare diminuisce, poiché si trova parallelo alle normali fibre muscolari. B2 - quando un muscolo viene allungato, il fuso muscolare si allunga. R - sistema di registrazione

Recettori di allungamento muscolare
Un modo noto per influenzare le afferenze sull'attività riflessa è attraverso la loro interazione con le fibre intrafusali con la borsa nucleare e le fibre con la catena nucleare. Come accennato in precedenza, esistono due tipi di motoneuroni γ: dinamici e statici. Gli assoni γ motori dinamici terminano su fibre intrafusali con una sacca nucleare e quelli statici terminano su fibre con una catena nucleare. Quando viene attivato un γ-motoneurone dinamico, la risposta dinamica delle afferenze del gruppo Ia aumenta (Fig. 5-25 A4), e quando viene attivato un γ-motoneurone statico, aumentano le risposte statiche delle afferenze di entrambi i gruppi Ia e II ( Fig. 5-25 A3), e allo stesso tempo può diminuire la risposta dinamica. Diverse vie discendenti hanno un effetto preferenziale sui motoneuroni gamma dinamici o statici, modificando così la natura dell'attività riflessa del midollo spinale.
Apparato tendineo del Golgi
Esiste un altro tipo di recettore dello stiramento nei muscoli scheletrici: Apparato tendineo del Golgi(Fig. 5-25 B). Il recettore, con un diametro di circa 100 μm e una lunghezza di circa 1 mm, è formato dalle terminazioni delle afferenze del gruppo Ib, assoni spessi con la stessa velocità di conduzione degli impulsi di quelle delle afferenze del gruppo Ia. Queste terminazioni avvolgono fasci di filamenti di collagene nel tendine muscolare (o inclusioni tendinee all'interno del muscolo). L'estremità sensibile dell'apparato tendineo è organizzata rispetto al muscolo in modo sequenziale, a differenza dei fusi muscolari che si trovano paralleli alle fibre extrafusali.
Grazie alla sua disposizione sequenziale, l'apparato tendineo del Golgi viene attivato sia dalla contrazione che dallo stiramento del muscolo (Fig. 5-25 B). Tuttavia, la contrazione muscolare è uno stimolo più efficace dello stretching, poiché lo stimolo per l'apparato tendineo è la forza sviluppata dal tendine in cui è situato il recettore. Pertanto, l'apparato tendineo del Golgi è un sensore di forza, a differenza del fuso muscolare, che fornisce segnali sulla lunghezza del muscolo e sulla velocità del suo cambiamento.
Riso. 5-25. Recettori di allungamento muscolare.
A - influenza dei motoneuroni gamma statici e dinamici sulle risposte delle terminazioni primarie durante l'allungamento muscolare. A1 - decorso temporale dell'allungamento muscolare. A2 - scarica dell'assone del gruppo Ia in assenza di attività del γ-motoneurone. A3 - risposta durante la stimolazione di un assone γ-efferente statico. A4 - risposta durante la stimolazione dell'assone dinamico γ-efferente. B - diagramma della posizione dell'apparato tendineo del Golgi. B - attivazione dell'apparato tendineo del Golgi durante l'allungamento muscolare (a sinistra) o la contrazione muscolare (a destra)

Funzione dei fusi muscolari
La frequenza di scarica nelle afferenze del gruppo Ia e del gruppo II è proporzionale alla lunghezza del fuso muscolare; ciò è evidente sia durante lo stretching lineare (Fig. 5-26 A, a sinistra) sia quando il muscolo si rilassa dopo lo stretching (Fig. 5-26 A, a destra). Questa reazione si chiama risposta statica afferenze dei fusi muscolari. Tuttavia, le terminazioni afferenti primarie e secondarie rispondono allo stiramento in modo diverso. Le terminazioni primarie sono sensibili sia al grado di allungamento che alla sua velocità, mentre le terminazioni secondarie rispondono principalmente all'entità dello stiramento (Fig. 5-26 A). Queste differenze determinano la natura dell'attività dei due tipi di finali. La frequenza di scarica dell'estremità primaria raggiunge il massimo durante l'allungamento muscolare e quando il muscolo allungato si rilassa, la scarica si interrompe. Questo tipo di reazione si chiama risposta dinamica assoni afferenti del gruppo Ia. Le risposte al centro della figura (Figura 5-26 A) sono esempi di risposte dinamiche della desinenza primaria. La percussione di un muscolo (o del suo tendine) o l'allungamento sinusoidale sono più efficaci nel provocare una scarica nella terminazione afferente primaria che in quella secondaria.
A giudicare dalla natura delle risposte, le terminazioni afferenti primarie segnalano sia la lunghezza del muscolo che la velocità del suo cambiamento, mentre le terminazioni secondarie trasmettono informazioni solo sulla lunghezza del muscolo. Queste differenze nel comportamento delle terminazioni primarie e secondarie dipendono principalmente dalla differenza nelle proprietà meccaniche delle fibre intrafusali con sacco nucleare e con catena nucleare. Come affermato sopra, le terminazioni primarie e secondarie si trovano su entrambi i tipi di fibre, mentre le terminazioni secondarie si trovano prevalentemente sulle fibre a catena nucleare. La parte centrale (equatoriale) della fibra con la sacca nucleare è priva di proteine contrattili a causa dell'accumulo di nuclei cellulari, quindi questa parte della fibra si allunga facilmente. Tuttavia, subito dopo lo stiramento, la parte centrale della fibra con il sacco nucleare tende a ritornare alla sua lunghezza originale, sebbene le parti terminali della fibra si allunghino. Il fenomeno che
chiamato "scivolare" a causa delle proprietà viscoelastiche di questa fibra intrafusale. Di conseguenza, si osserva un'esplosione di attività dalla terminazione primaria, seguita da un indebolimento dell'attività ad un nuovo livello statico di frequenza dell'impulso.
A differenza delle fibre della borsa, le fibre della catena nucleata variano in lunghezza più strettamente con i cambiamenti nella lunghezza delle fibre muscolari extrafusali perché la porzione centrale delle fibre della borsa contiene proteine contrattili. Di conseguenza, la fibra della catena nucleare ha caratteristiche viscoelastiche più uniformi, non è soggetta a scivolamento e le sue terminazioni afferenti secondarie generano solo risposte statiche.
Finora abbiamo considerato il comportamento dei fusi muscolari solo in assenza di attività dei motoneuroni γ. Allo stesso tempo, l'innervazione efferente dei fusi muscolari è estremamente significativa, poiché determina la sensibilità dei fusi muscolari allo stiramento. Ad esempio, nella Fig. 5-26 B1 mostra l'attività dei fusi muscolari afferenti durante l'allungamento costante. Come già accennato, con la contrazione delle fibre extrafusali (Fig. 5-26 B2), i fusi muscolari cessano di essere caricati e lo scarico delle loro afferenze si interrompe. Tuttavia, l’effetto dello scarico del fuso muscolare è contrastato dall’effetto della stimolazione del motoneurone γ. Questa stimolazione provoca un accorciamento del fuso muscolare insieme alle fibre extrafusali (Fig. 5-26 B3). Più precisamente, solo due estremità del fuso muscolare risultano accorciate; la sua parte media (equatoriale), dove si trovano i nuclei cellulari, non si contrae per la mancanza di proteine contrattili. Di conseguenza, la parte centrale del fuso si allunga in modo che le terminazioni afferenti siano allungate ed eccitate. Questo meccanismo è molto importante per la normale attività dei fusi muscolari, poiché a seguito dei comandi motori discendenti dal cervello, di regola, si verifica l'attivazione simultanea dei motoneuroni α e γ e, di conseguenza, una contrazione coniugata di extrafusale e intrafusale fibre muscolari.
Riso. 5-26. I fusi muscolari e il loro lavoro.
A - risposte delle terminazioni primarie e secondarie a vari tipi di cambiamenti nella lunghezza del muscolo; sono state dimostrate differenze tra le risposte dinamiche e quelle statiche. Le curve superiori mostrano lo schema dei cambiamenti nella lunghezza del muscolo. La riga centrale e quella inferiore delle registrazioni sono scariche di impulsi delle terminazioni nervose primarie e secondarie. B - l'attivazione dell'assone γ-efferente contrasta l'effetto di scarico dei fusi muscolari. B1 - scarica dell'impulso del fuso muscolare afferente durante lo stiramento costante del fuso. B2 - La scarica afferente cessa durante la contrazione delle fibre muscolari extrafusali, poiché il carico viene rimosso dal fuso. B3 - l'attivazione del γ-motoneurone provoca l'accorciamento del fuso muscolare, contrastando l'effetto dello scarico

Riflesso miotatico o riflesso di stiramento
Il riflesso di stiramento gioca un ruolo chiave nel mantenimento della postura. Inoltre, i suoi cambiamenti sono coinvolti nell'attuazione dei comandi motori del cervello. I disturbi patologici di questo riflesso sono segni di malattie neurologiche. Il riflesso si manifesta in due forme: riflesso fasico da stiramento,è attivato dalle terminazioni primarie dei fusi muscolari e riflesso tonico da stiramento dipende sia dal finale primario che da quello secondario.
Riflesso di stiramento fasico
L'arco riflesso corrispondente è mostrato in Fig. 5-27. L'assone afferente del gruppo Ia dal fuso muscolare del retto femorale entra nel midollo spinale e si ramifica. I suoi rami entrano nella materia grigia del midollo spinale. Alcuni di essi terminano direttamente (monosinapticamente) sui motoneuroni α, inviando gli assoni motori al retto femorale (e ai suoi sinergisti, come il vasto intermedio), che estende la gamba all'altezza del ginocchio. Gli assoni del gruppo Ia forniscono l'eccitazione monosinaptica del motoneurone α. Con un livello sufficiente di eccitazione, il motoneurone genera una scarica che provoca la contrazione muscolare.
Altri rami dell'assone del gruppo Ia formano terminazioni sugli interneuroni inibitori del gruppo Ia (tale interneurone è mostrato in nero nella Figura 5.27). Questi interneuroni inibitori terminano sui motoneuroni α che innervano i muscoli che si collegano ai muscoli posteriori della coscia (compreso il muscolo semitendinoso), i muscoli flessori antagonisti del ginocchio. Quando gli interneuroni inibitori Ia sono eccitati, l’attività dei motoneuroni dei muscoli antagonisti viene soppressa. Pertanto, la scarica (attività stimolante) delle afferenze del gruppo Ia dai fusi muscolari del muscolo retto femorale provoca una rapida contrazione dello stesso muscolo e
rilassamento coniugato dei muscoli collegati ai muscoli posteriori della coscia.
L'arco riflesso è organizzato in modo tale da garantire l'attivazione di un certo gruppo di motoneuroni α e la simultanea inibizione di un gruppo di neuroni antagonisti. È chiamato innervazione reciproca.È caratteristico di molti riflessi, ma non è l'unico possibile nei sistemi di regolazione del movimento. In alcuni casi, i comandi motori provocano una contrazione coniugata di agenti sinergici e antagonisti. Ad esempio, quando stringi la mano a pugno, i muscoli estensori e flessori della mano si contraggono, fissando la posizione della mano.
La scarica dell'impulso delle afferenze del gruppo Ia si osserva quando il medico applica un leggero colpo al tendine di un muscolo, solitamente il quadricipite femorale, con un martello neurologico. La reazione normale è una contrazione muscolare a breve termine.
Riflesso tonico da stiramento
Questo tipo di riflesso viene attivato dalla flessione passiva dell'articolazione. L'arco riflesso è lo stesso del riflesso fasico da stiramento (Fig. 5-27), con la differenza che sono coinvolte le afferenze di entrambi i gruppi - Ia e II. Molti assoni del gruppo II formano connessioni eccitatorie monosinaptiche con i motoneuroni α. Di conseguenza, i riflessi da stiramento tonico sono in gran parte monosinaptici, proprio come i riflessi da stiramento fasici. I riflessi tonici da stiramento contribuiscono al tono muscolare.
γ -Motoneuroni e riflessi di stiramento
I motoneuroni γ regolano la sensibilità dei riflessi da stiramento. Le afferenze dei fusi muscolari non influenzano direttamente i γ-motoneuroni, che vengono attivati polisinapticamente solo dalle afferenze del riflesso di flessione a livello spinale, nonché dai comandi discendenti dal cervello.
Riso. 5-27. Riflesso miotatico.
L'arco del riflesso da stiramento. L'interneurone (mostrato in nero) appartiene agli interneuroni inibitori del gruppo Ia

Riflesso miotatico inverso
L'attivazione dell'apparato tendineo del Golgi è accompagnata da una risposta riflessa, che a prima vista è l'opposto del riflesso da stiramento (in realtà questa reazione è complementare al riflesso da stiramento). La reazione viene chiamata riflesso miotatico inverso; l'arco riflesso corrispondente è mostrato in Fig. 5-28. I recettori sensoriali per questo riflesso sono l'apparato tendineo del Golgi nel muscolo retto femorale. Gli assoni afferenti entrano nel midollo spinale, si ramificano e formano terminazioni sinaptiche sugli interneuroni. La via che parte dall'apparato tendineo del Golgi non ha una connessione monosinaptica con gli α-motoneuroni, ma comprende interneuroni inibitori che sopprimono l'attività degli α-motoneuroni del muscolo retto femorale e interneuroni eccitatori che causano l'attività degli α-motoneuroni dei muscoli antagonisti . Pertanto, nella sua organizzazione, il riflesso miotatico inverso è l'opposto del riflesso di stiramento, da cui deriva il nome. Tuttavia, in realtà, il riflesso miotatico inverso è funzionalmente complementare al riflesso da stiramento. L'apparato tendineo del Golgi funge da sensore della forza sviluppata dal tendine a cui è collegato. Quando si mantiene stabile
postura (ad esempio una persona sta sull'attenti), il muscolo retto femorale inizia ad affaticarsi, la forza applicata al tendine rotuleo diminuisce e, di conseguenza, diminuisce l'attività dei corrispondenti recettori del tendine del Golgi. Poiché questi recettori di solito sopprimono l'attività dei motoneuroni α del muscolo retto femorale, l'indebolimento delle scariche impulsive da essi porta ad una maggiore eccitabilità dei motoneuroni α e aumenta la forza sviluppata dal muscolo. Di conseguenza, si verifica un cambiamento coordinato nelle reazioni riflesse con la partecipazione sia dei fusi muscolari che degli assoni afferenti dell'apparato tendineo del Golgi, la contrazione del muscolo retto aumenta e la postura viene mantenuta.
Quando i riflessi sono iperattivati, si può osservare un riflesso “a coltello a serramanico”. Quando un’articolazione si flette passivamente, inizialmente la resistenza alla flessione aumenta. Tuttavia, man mano che la flessione continua, la resistenza diminuisce improvvisamente e l’articolazione si sposta bruscamente nella sua posizione finale. La ragione di ciò è l'inibizione dei riflessi. In precedenza, il riflesso del coltello a serramanico veniva spiegato con l'attivazione dei recettori tendinei del Golgi, poiché si pensava che avessero una soglia elevata di risposta all'allungamento muscolare. Tuttavia, il riflesso è ora associato all'attivazione di altri recettori muscolari ad alta soglia situati nella fascia muscolare.
Riso. 5-28. Riflesso miotatico inverso.
Arco del riflesso miotatico inverso. Sono coinvolti sia gli interneuroni eccitatori che quelli inibitori

Riflessi di flessione
Il collegamento afferente dei riflessi di flessione inizia da diversi tipi di recettori. Durante i riflessi di flessione, le scariche afferenti portano al fatto che, in primo luogo, gli interneuroni eccitatori causano l'attivazione degli α-motoneuroni che forniscono i muscoli flessori dell'arto ipsilaterale e, in secondo luogo, i neuroni inibitori non consentono l'attivazione dei muscoli estensori antagonisti degli α-motoneuroni ( Figura 5-29). Di conseguenza, uno o più giunti si piegano. Inoltre, gli interneuroni commissurali causano un'attività funzionalmente opposta dei motoneuroni sul lato controlaterale del midollo spinale, in modo che si verifichi l'estensione muscolare: il riflesso estensore crociato. Questo effetto controlaterale aiuta a mantenere l'equilibrio del corpo.
Esistono diversi tipi di riflessi di flessione, sebbene la natura delle contrazioni muscolari corrispondenti sia simile. Una fase importante della locomozione è la fase di flessione, che può essere considerata un riflesso di flessione. È fornito principalmente dalla rete neurale del midollo spinale
cervello ha chiamato generatore locomotore
ciclo. Tuttavia, sotto l'influenza degli input afferenti, il ciclo locomotore può adattarsi a cambiamenti momentanei nell'appoggio degli arti.
Il riflesso di flessione più potente è riflesso di ritiro della flessione. Prevale sugli altri riflessi, compresi quelli locomotori, apparentemente perché previene ulteriori danni all'arto. Questo riflesso può essere osservato quando un cane che cammina preme la zampa ferita. La parte afferente del riflesso è formata dai nocicettori.
In questo riflesso, un forte stimolo doloroso fa ritirare l'arto. La Figura 5-29 mostra la rete neurale per un riflesso di flessione specifico per l'articolazione del ginocchio. Tuttavia, in realtà, durante il riflesso di flessione si verifica una significativa divergenza di segnali dalle afferenze primarie e dalle vie interneuronali, per cui tutte le principali articolazioni dell'arto (anca, ginocchio, caviglia) possono essere coinvolte nel riflesso di ritiro. Le caratteristiche del riflesso di ritiro della flessione in ciascun caso specifico dipendono dalla natura e dalla posizione dello stimolo.
Riso. 5-29. Riflesso di flessione

Divisione simpatica del sistema nervoso autonomo
I corpi cellulari dei neuroni simpatici pregangliari sono concentrati nella materia grigia intermedia e laterale (colonna intermediolaterale) segmenti toracici e lombari del midollo spinale (Fig. 5-30). Alcuni neuroni si trovano nei segmenti C8. Insieme alla localizzazione nella colonna intermediolaterale, è stata trovata la localizzazione dei neuroni simpatici pregangliari anche nel funicolo laterale, nella regione intermedia e nella placca X (dorsale al canale centrale).
La maggior parte dei neuroni simpatici pregangliari hanno assoni mielinizzati sottili - B- fibra. Tuttavia, alcuni assoni sono fibre C non mielinizzate. Gli assoni pregangliari lasciano il midollo spinale come parte della radice anteriore ed entrano nel ganglio paravertebrale a livello dello stesso segmento attraverso i rami comunicanti bianchi. I rami di collegamento bianchi sono presenti solo ai livelli T1-L2. Gli assoni pregangliari terminano nelle sinapsi di questo ganglio o, dopo averlo attraversato, entrano nel tronco simpatico (catena simpatica) dei gangli paravertebrali o del nervo splancnico.
Come parte della catena simpatica, gli assoni pregangliari sono diretti rostralmente o caudalmente al ganglio prevertebrale più vicino o distante e lì formano sinapsi. Dopo aver lasciato il ganglio, gli assoni postgangliari viaggiano verso il nervo spinale, solitamente attraverso il ramo comunicante grigio, presente in ciascuna delle 31 paia di nervi spinali. Come parte dei nervi periferici, gli assoni postgangliari entrano negli effettori della pelle (muscoli piloerettori, vasi sanguigni, ghiandole sudoripare), muscoli e articolazioni. Tipicamente, gli assoni postgangliari non sono mielinizzati (CON-fibre), anche se ci sono delle eccezioni. Le differenze tra i rami di collegamento bianchi e grigi dipendono dal contenuto relativo
contengono assoni mielinizzati e non mielinizzati.
Come parte del nervo splancnico, gli assoni pregangliari spesso vanno al ganglio prevertebrale, dove formano sinapsi, oppure possono passare attraverso il ganglio, terminando in un ganglio più distale. Alcuni assoni pregangliari che corrono come parte del nervo splancnico terminano direttamente sulle cellule della midollare del surrene.
La catena simpatica si estende dal livello cervicale a quello coccigeo del midollo spinale. Funziona come un sistema di distribuzione, consentendo ai neuroni pregangliari situati solo nei segmenti toracico e lombare superiore di attivare i neuroni postgangliari che riforniscono tutti i segmenti del corpo. Tuttavia, ci sono meno gangli paravertebrali rispetto ai segmenti spinali, poiché alcuni gangli si fondono durante l'ontogenesi. Ad esempio, il ganglio simpatico cervicale superiore è composto dai gangli simpatici fusi C1-C4, il ganglio simpatico cervicale medio è composto dai gangli C5-C6 e il ganglio simpatico cervicale inferiore è composto dai gangli C7-C8. Il ganglio stellato è formato dalla fusione del ganglio simpatico cervicale inferiore con il ganglio T1. Il ganglio cervicale superiore fornisce innervazione postgangliare alla testa e al collo, mentre i gangli cervicali centrali e stellati forniscono innervazione postgangliare al cuore, ai polmoni e ai bronchi.
Tipicamente, gli assoni dei neuroni simpatici pregangliari si distribuiscono ai gangli ipsilaterali e quindi regolano le funzioni autonome sullo stesso lato del corpo. Un'importante eccezione è l'innervazione simpatica bilaterale dell'intestino e degli organi pelvici. Come i nervi motori dei muscoli scheletrici, gli assoni dei neuroni simpatici pregangliari appartenenti a organi specifici innervano diversi segmenti. Pertanto, i neuroni simpatici pregangliari, che forniscono funzioni simpatiche alle aree della testa e del collo, si trovano nei segmenti C8-T5, e quelli relativi alle ghiandole surrenali sono in T4-T12.
Riso. 5-30. Sistema nervoso simpatico autonomo.
A - principi fondamentali. Arco riflesso vedere fig. 5-9 B

Divisione parasimpatica del sistema nervoso autonomo
I neuroni parasimpatici pregangliari si trovano nel tronco cerebrale in diversi nuclei dei nervi cranici - nell'oculomotore Nucleo di Westphal-Edinger(III nervo cranico), superiore(VII nervo cranico) e inferiore(IX nervo cranico) nuclei salivari, E nucleo dorsale del nervo vago(nucleo dorsale dei nervi vagi) E dual core(nucleo ambiguo) X nervo cranico. Inoltre, tali neuroni sono presenti nella regione intermedia dei segmenti sacrali S3-S4 del midollo spinale. I neuroni parasimpatici postgangliari si trovano nei gangli dei nervi cranici: nel ganglio ciliare (ganglio ciliare), ricevere input pregangliari dal nucleo Westphal-Edinger; nel ganglio pterigopalatino (ganglio pterigopalatino) e nodo sottomandibolare (ganglio sottomandibolare) con input dal nucleo salivare superiore (nucleo salivatorio superiore); nel nodo dell'orecchio (ganglio otico) con input dal nucleo salivare inferiore (nucleo salivatorio inferiore). Il ganglio ciliare innerva il muscolo sfintere della pupilla e i muscoli ciliari dell'occhio. Gli assoni vanno dal ganglio pterigopalatino alle ghiandole lacrimali, nonché alle ghiandole della faringe nasale e orale. I neuroni del ganglio sottomandibolare proiettano alle ghiandole salivari sottomandibolari e sublinguali e alle ghiandole della cavità orale. Il ganglio auricolare fornisce la ghiandola salivare parotide e le ghiandole orali
(Fig. 5-31 A).
Altri neuroni parasimpatici postgangliari si trovano vicino agli organi interni del torace, delle cavità addominali e pelviche o nelle pareti di questi organi. Possono essere prese in considerazione anche alcune cellule del plesso enterico
come neuroni parasimpatici postgangliari. Ricevono input dal vago o dai nervi pelvici. Il nervo vago innerva il cuore, i polmoni, i bronchi, il fegato, il pancreas e l'intero tratto gastrointestinale dall'esofago alla flessura splenica del colon. Il resto del colon, del retto, della vescica e dei genitali è rifornito dagli assoni dei neuroni parasimpatici pregangliari sacrali; questi assoni sono distribuiti attraverso i nervi pelvici ai neuroni postgangliari dei gangli pelvici.
I neuroni parasimpatici pregangliari, che danno proiezioni agli organi interni della cavità toracica e parte della cavità addominale, sono localizzati nel nucleo motore dorsale del nervo vago e nel doppio nucleo. Il nucleo motore dorsale funziona principalmente funzione secretomotoria(attiva le ghiandole), mentre il doppio nucleo - funzione visceromotoria(regola l'attività del muscolo cardiaco). Il nucleo motore dorsale fornisce gli organi viscerali del collo (faringe, laringe), la cavità toracica (trachea, bronchi, polmoni, cuore, esofago) e la cavità addominale (una parte significativa del tratto gastrointestinale, fegato, pancreas). La stimolazione elettrica del nucleo motore dorsale provoca la secrezione acida nello stomaco e la secrezione di insulina e glucagone nel pancreas. Sebbene le proiezioni al cuore siano tracciate anatomicamente, le loro funzioni non sono chiare. Nel doppio nucleo si distinguono due gruppi di neuroni:
Gruppo dorsale, attiva i muscoli striati del palato molle, faringe, laringe ed esofago;
Il gruppo ventrolaterale innerva il cuore, rallentandone il ritmo.
Riso. 5-31. Sistema nervoso autonomo parasimpatico.
A - principi fondamentali

Sistema nervoso autonomo
Sistema nervoso autonomo può essere considerato come parte del sistema motorio (efferente). Solo che al posto dei muscoli scheletrici, gli effettori del sistema nervoso autonomo sono i muscoli lisci, il miocardio e le ghiandole. Poiché il sistema nervoso autonomo fornisce il controllo efferente degli organi viscerali, nella letteratura straniera viene spesso chiamato sistema nervoso viscerale o autonomo.
Un aspetto importante dell'attività del sistema nervoso autonomo è l'aiuto nel mantenere la costanza dell'ambiente interno del corpo (omeostasi). Quando dagli organi viscerali si ricevono segnali sulla necessità di regolare l'ambiente interno, il sistema nervoso centrale e il suo sito effettore autonomo inviano i comandi appropriati. Ad esempio, quando si verifica un improvviso aumento della pressione sanguigna sistemica, i barocettori vengono attivati, inducendo il sistema nervoso autonomo ad avviare processi compensatori e a ripristinare la normale pressione sanguigna.
Il sistema nervoso autonomo è anche coinvolto in adeguate reazioni coordinate agli stimoli esterni. Quindi è utile regolare la dimensione della pupilla in base all'illuminazione. Un caso estremo di regolazione autonomica è la risposta di lotta o fuga, che si verifica quando il sistema nervoso simpatico viene attivato da uno stimolo minaccioso. Ciò comporta una serie di reazioni: rilascio di ormoni dalle ghiandole surrenali, aumento della frequenza cardiaca e della pressione sanguigna, dilatazione dei bronchi, inibizione della motilità e della secrezione intestinale, aumento del metabolismo del glucosio, pupille dilatate, piloerezione, costrizione dei vasi sanguigni cutanei e viscerali. , dilatazione dei vasi muscolari scheletrici. Va notato che la risposta “lotta o fuga” non può essere considerata ordinaria; va oltre la normale attività del sistema nervoso simpatico durante la normale esistenza del corpo.
Nei nervi periferici, insieme alle fibre efferenti autonome, seguono le fibre afferenti dei recettori sensoriali degli organi viscerali. I segnali provenienti da molti di questi recettori attivano i riflessi, ma l'attivazione di alcuni recettori provoca
sensazioni: dolore, fame, sete, nausea, sensazione di riempimento degli organi interni. La sensibilità viscerale può includere anche la sensibilità chimica.
Il sistema nervoso autonomo è solitamente suddiviso in comprensivo E parasimpatico.
Unità funzionale del sistema nervoso simpatico e parasimpatico- una via efferente a due neuroni costituita da un neurone pregangliare con un corpo cellulare nel sistema nervoso centrale e un neurone postgangliare con un corpo cellulare nel ganglio autonomo. Il sistema nervoso enterico comprende neuroni e fibre nervose dei plessi mioenterico e sottomucoso nella parete del tratto gastrointestinale.
I neuroni pregangliari simpatici si trovano nei segmenti toracico e lombare superiore del midollo spinale, quindi il sistema nervoso simpatico viene talvolta definito divisione toracolombare del sistema nervoso autonomo. Il sistema nervoso parasimpatico è strutturato in modo diverso: i suoi neuroni pregangliari si trovano nel tronco encefalico e nel midollo spinale sacrale, per questo a volte viene chiamato regione craniosacrale. I neuroni postgangliari simpatici si trovano solitamente nei gangli paravertebrali o prevertebrali a una distanza dall'organo bersaglio. Per quanto riguarda i neuroni parasimpatici postgangliari, si trovano nei gangli parasimpatici vicino all'organo esecutivo o direttamente nella sua parete.
L'influenza regolatoria dei sistemi nervoso simpatico e parasimpatico in molti organismi è spesso descritta come reciprocamente antagonista, ma questo non è del tutto vero. Sarebbe più corretto considerare queste due sezioni del sistema di regolazione autonoma delle funzioni viscerali come agenti in modo coordinato: a volte reciprocamente, a volte sinergicamente. Inoltre, non tutte le strutture viscerali ricevono innervazione da entrambi i sistemi. Pertanto, i muscoli lisci e le ghiandole cutanee, così come la maggior parte dei vasi sanguigni, sono innervati solo dal sistema simpatico; Pochi vasi sono forniti dai nervi parasimpatici. Il sistema parasimpatico non innerva i vasi della pelle e dei muscoli scheletrici, ma fornisce solo le strutture della testa, del torace e della cavità addominale, nonché del bacino.
Riso. 5-32. Sistema nervoso autonomo (autonomo) (Tabella 5-2)
Tabella 5-2.Reazioni degli organi effettori ai segnali provenienti dai nervi autonomi *

Fine del tavolo. 5-2.

1 Un trattino significa che l'innervazione funzionale dell'organo non è stata rilevata.
2 segni “+” (da uno a tre) indicano quanto sia importante l'attività dei nervi adrenergici e colinergici nella regolazione di organi e funzioni specifici.
3 Sul posto predomina l’espansione dovuta all’autoregolazione metabolica.
4 Il ruolo fisiologico della vasodilatazione colinergica in questi organi è controverso.
5 Nell'intervallo delle concentrazioni fisiologiche dell'adrenalina circolante nel sangue, la reazione di espansione mediata dai recettori β predomina nei vasi dei muscoli scheletrici e del fegato, mentre la reazione di costrizione mediata dai recettori α predomina nei vasi di altri organi addominali . Inoltre, i vasi dei reni e del mesentere contengono specifici recettori della dopamina che mediano la dilatazione, che però non svolge un ruolo importante in molte reazioni fisiologiche.
6 Il sistema simpatico colinergico provoca vasodilatazione nel muscolo scheletrico, ma questo effetto non è coinvolto nella maggior parte delle risposte fisiologiche.
7 Si presume che i nervi adrenergici forniscano recettori β inibitori nella muscolatura liscia
e recettori α inibitori sui neuroni gangliari colinergici (eccitatori) parasimpatici del plesso di Auerbach.
8 A seconda della fase del ciclo mestruale, della concentrazione di estrogeni e progesterone nel sangue e di altri fattori.
9 Ghiandole sudoripare dei palmi delle mani e di alcune altre aree del corpo (“sudorazione adrenergica”).
10 I tipi di recettori che mediano le risposte metaboliche specifiche variano in modo significativo tra le specie animali.
Domanda 20. Unità strutturali del sistema nervoso
Funzioni e struttura del sistema nervoso.
Arco riflesso.
Nervi.
Nodi nervosi.
1. Funzioni del sistema nervoso - Lei:
Effettua l'unificazione delle parti del corpo in un unico insieme (integrazione); V fornisce la regolamentazione di vari processi, il coordinamento
funzioni di vari organi e tessuti e interazione del corpo con l'ambiente esterno;
Percepisce una varietà di informazioni provenienti dall'ambiente esterno e dagli organi interni, le elabora e genera segnali che forniscono risposte adeguate agli stimoli attuali.
Anatomicamente il sistema nervososuddiviso:
SU Sistema nervoso centrale - cervello e midollo spinale;
V PNS- gangli nervosi periferici, nervi e terminazioni nervose.
Fisiologicamente,a seconda della natura dell'innervazione di organi e tessuti:
SU sistema nervoso somatico (animale), che regola innanzitutto le funzioni del movimento volontario;
sistema nervoso autonomo (vegetativo), che regola l’attività degli organi interni e delle ghiandole. Influenzando l'attività metabolica in vari organi e tessuti in conformità con le mutevoli condizioni del loro funzionamento e dell'ambiente esterno, svolge una funzione adattivo-trofica.
Sistema nervoso autonomoè suddiviso in dipartimenti che interagiscono tra loro, che differiscono nella localizzazione dei centri nel cervello e nei nodi periferici, nonché nella natura dell'effetto sugli organi interni:
Comprensivo;
Parasimpatico.
Il sistema nervoso somatico e autonomo comprende collegamenti situati nel sistema nervoso centrale e nel PNS.
Il tessuto funzionalmente principale degli organi del sistema nervoso è tessuto nervoso, Compreso neuroni E glia.
Vengono solitamente chiamati gruppi di neuroni nel sistema nervoso centrale nuclei, e nel PNS - nodi (gangli).
Vengono chiamati fasci di fibre nervose nel sistema nervoso centrale tratti, nel PNS si formano nervi.
Centri nervosi- accumuli di cellule nervose nel sistema nervoso centrale e nel sistema nervoso centrale, in cui avviene la trasmissione sinaptica tra di loro. Hanno una struttura complessa, ricchezza e varietà di connessioni interne ed esterne e sono specializzati nello svolgimento di determinate funzioni.
Dalla natura dell'organizzazione morfofunzionalesi distinguono i centri nervosi:
tipo nucleare, in cui i neuroni si trovano senza ordine visibile (gangli autonomi, nuclei del midollo spinale e del cervello);
tipo di schermo, in cui neuroni che svolgono funzioni simili sono raccolti sotto forma di strati separati, simili a schermi su cui vengono proiettati gli impulsi nervosi (corteccia cerebellare, corteccia cerebrale, retina). Esistono numerose connessioni associative all'interno e tra gli strati.
Nei centri nervosi si verificano processi di convergenza e divergenza dell'eccitazione nervosa e funzionano i meccanismi di feedback.
Convergenza- convergenza di diverse vie di impulsi nervosi verso un numero minore di cellule nervose. I neuroni possono avere terminazioni cellulari di diverso tipo, il che garantisce la convergenza di influenze provenienti da varie fonti.
Divergenza- formazione di connessioni di un neurone con un gran numero di altri, l'attività di cui influenza, fornendo la ridistribuzione degli impulsi con irradiazione dell'eccitazione.
Forniscono meccanismi di feedback la capacità dei neuroni di regolare l'entità dei segnali da loro ricevuti grazie alle connessioni dei loro collaterali assonici con le cellule intercalari. Questi ultimi hanno un effetto (solitamente inibitorio) sia sui neuroni che sui terminali delle fibre ad essi convergenti.
2. Arco riflesso È unità funzionale del sistema nervoso e rappresenta catene di neuroni, che forniscono reazioni degli organi funzionanti (organi bersaglio) in risposta all'irritazione dei recettori. Negli archi riflessi si formano neuroni collegati tra loro tramite sinapsi 3 collegamento
- recettore (afferente);
- effettore;
- associativo (intercalare) situato tra di loro; nella versione più semplice l'arco può essere assente.
I vari collegamenti dell'arco sono soggetti agli influssi regolatori dei neuroni associati dei centri sovrastanti, per cui gli archi riflessi hanno una struttura complessa. Gli archi riflessi nelle parti somatiche (animali) e autonome (vegetative) del sistema nervoso hanno una serie di caratteristiche.
Arco riflesso somatico (animale):
collegamento del recettore formato da afferente neuroni pseudounipolari, corpo che si trovano nei gangli spinali. Dendriti queste cellule formano sensibili terminazioni nervose nella pelleo muscoli scheletrici, UN assoni entrare nel midollo spinale come parte delle radici dorsali e sono diretti ai corni posteriori della sua materia grigia, formandosi sinapsi sui corpi e sui dendriti degli interneuroni. Alcuni ramoscelli (collaterali) gli assoni dei neuroni pseudounipolari passano direttamente (senza formare connessioni nelle corna dorsali). nelle corna anteriori, dove finiscono sui motoneuroni (formandosi con essi archi riflessi a due neuroni);
legame associativo(che potrebbe non essere) rappresentato, dendriti e corpo che si trovano nelle corna posteriori midollo spinale e assoni vengono inviati nelle corna anteriori, trasmettendo impulsi sui corpi e dendriti neuroni effettori;
collegamento effettore educato motoneuroni multipolari, corpo e i cui dendriti giacciono nelle corna anteriori, UN assoni uscire dal midollo spinale come parte delle radici anteriori, stanno andando al ganglio spinale e inoltre come parte del nervo misto - al muscolo scheletrico, sulle cui fibre si trovano i loro rami formano sinapsi neuromuscolari (placche motorie o motorie).).
Arco riflesso autonomo (vegetativo).
collegamento del recettore, come nell'arco riflesso somatico, è formato da afferenti Neuroni pseudounipolari, corpi che si trovano nei gangli spinali Tuttavia dendriti queste cellule formano terminazioni nervose sensoriali nei tessuti degli organi interni, dei vasi sanguigni e delle ghiandole. Il loro a xoni entrano nel midollo spinale come parte delle radici dorsali e, aggirando le corna dorsali, sono diretti nelle corna laterali materia grigia, formando sinapsi sui corpi e sui dendriti degli interneuroni;
legame associativo presentata interneuroni multipolari, dendriti e corpi che si trovano in corna laterali midollo spinale e assoni(fibre pregangliari) lasciano il midollo spinale come parte delle radici anteriori, intestazione in uno dei gangli autonomi, dove finiscono sui dendriti e corpi di neuroni effettori;
collegamento effettore formato da neuroni multipolari, corpo che mentono all'interno dei gangli autonomi, UN assoni(fibre postgangliari) come parte dei tronchi nervosi e i loro rami sono diretti alle cellule degli organi funzionanti: muscoli lisci, ghiandole, cuore.
3. Nervi (tronchi nervosi) collegano i centri nervosi del cervello e del midollo spinale con i recettori e gli organi funzionanti. Sono formati da fasci di fibre nervose unite componenti del tessuto connettivo (conchiglie):
endonevrio;
Perinevrio;
Epinevrio.
La maggior parte dei nervi lo sono misto, cioè, includono fibre nervose afferenti ed efferenti. Fasci di fibre nervose contengono fino a diverse migliaia di fibre mielinizzate e non mielinizzate, il rapporto tra le quali varia nei diversi nervi; funzionalmente sono correlati all'animale E sistema nervoso autonomo.
Endonevrio- sottili strati di tessuto connettivo fibroso lasso che circondano le singole fibre nervose e le legano in un unico fascio. Contiene poche cellule e fibre (principalmente reticolari), piccoli vasi sanguigni.
Perinevrio- una guaina che copre ciascun fascio di fibre nervose dall'esterno e estende i setti più in profondità nel fascio. Il perinevrio è formato da 2-10 fogli concentrici di cellule appiattite collegate da giunzioni strette e giunzioni comunicanti. Il citoplasma delle cellule, soprattutto gli strati esterni, contiene numerose vescicole pinocitotiche. Tra gli strati di cellule in spazi a fessura pieni di liquido si trovano i componenti della membrana basale e le fibre di collagene orientate longitudinalmente. Nella parte terminale del nervo, il perinevrio è formato da un solo strato di cellule piatte, che termina bruscamente distalmente e ha l'aspetto di una cuffia aperta.
Epinevrio- la guaina esterna del nervo, che collega tra loro fasci di fibre nervose (il cui numero dipende dal diametro del nervo e varia da una a diverse dozzine). È costituito da tessuto connettivo fibroso denso contenente cellule adipose, vasi sanguigni e linfatici.
- Nodi nervosi (gangli) - accumulo di neuroni al di fuori del sistema nervoso centrale.
Tipi di gangli nervosi:
Sensibile (sensoriale),
Autonomo (vegetativo).
Gangli nervosi sensoriali (sensoriali). contengono neuroni afferenti pseudounipolari o bipolari (nei gangli spirale e vestibolari) e si trovano lungo le radici dorsali del midollo spinale (nodi spinali o spinali) e dei nervi cranici (5, 7, 8, 9, 10 paia).
Ganglio spinale (spinale). ha una forma fusiforme ed è ricoperto da una capsula di tessuto connettivo fibroso denso. Lungo la sua periferia ci sono densi gruppi di corpi di neuroni pseudounipolari, e la parte centrale è occupata dai loro processi e sottili strati di endonevrio situati tra loro, che portano vasi.
Neuroni pseudounipolari caratterizzato da un corpo sferico e un nucleo di colore chiaro con nucleolo ben visibile. Esistono cellule grandi e piccole, che probabilmente differiscono per il tipo di impulsi che conducono. Il citoplasma dei neuroni contiene numerosi mitocondri, cisterne del reticolo endoplasmatico granulare, elementi del complesso del Golgi e lisosomi. Ogni neurone è circondato da uno strato di cellule oligodendrogliali appiattite adiacenti (gliociti del mantello o cellule satellite) con piccoli nuclei rotondi; all'esterno della membrana gliale è presente una sottile membrana di tessuto connettivo. Un processo si estende dal corpo del neurone pseudounipolare, dividendosi a forma di T in rami afferenti (dendritici) ed efferenti (assonali), che sono ricoperti da guaine mieliniche. Il ramo afferente termina alla periferia con i recettori, il ramo efferente, come parte della radice dorsale, entra nel midollo spinale. Poiché la commutazione di un impulso nervoso da un neurone all'altro non avviene all'interno dei gangli spinali, essi non sono centri nervosi. I neuroni dei gangli spinali contengono neurotrasmettitori come acetilcolina, acido glutammico, sostanza P, somatostatina, colecistochinina, gastrina e peptide vasointestinale.
Gangli nervosi autonomi (autonomi). può essere localizzato lungo la colonna vertebrale (gangli paravertebrali), o davanti a lui (gangli prevertebrali), così come nella parete degli organi: cuore, bronchi, tratto digestivo, vescica, ecc. (gangli intramurali) o vicino alla loro superficie. A volte hanno l'aspetto di piccoli accumuli (da alcune cellule a diverse decine di cellule) di neuroni situati lungo il decorso di alcuni nervi o situati intramurali (microgangli). Le fibre pregangliari (mielina), contenenti processi di cellule i cui corpi si trovano nel sistema nervoso centrale, si avvicinano ai nodi vegetativi. Queste fibre sono altamente ramificate e formano numerose terminazioni sinaptiche sulle cellule dei gangli vegetativi. Per questo motivo, un gran numero di terminali di fibre pregangliari convergono su ciascun neurone gangliare. A causa della presenza della trasmissione sinaptica, i nodi vegetativi sono classificati come centri nervosi di tipo nucleare.
Gangli nervosi autonomiIn base alle caratteristiche funzionali e alla localizzazione si dividono in:
Al simpatico;
Parasimpatico.
Gangli nervosi simpatici(para- e prevertebrale) ricevono fibre pregangliari da cellule situate nei nuclei autonomi dei segmenti toracico e lombare del midollo spinale. Il neurotrasmettitore delle fibre pregangliari è l’acetilcolina, mentre quello delle fibre postgangliari è norepinefrina (per ad eccezione delle ghiandole sudoripare e di alcuni vasi sanguigni che hanno innervazione simpatica colinergica). Oltre a questi neurotrasmettitori, nei linfonodi vengono rilevate encefaline, sostanza P, somatostatina e colecistochinina.
Gangli nervosi parasimpatici(intramurali, situati vicino a organi o nodi della testa) ricevono fibre pregangliari da cellule situate nei nuclei vegetativi del midollo allungato e del mesencefalo, nonché del midollo spinale sacrale. Queste fibre lasciano il sistema nervoso centrale come parte della 3a, 7a, 9a, 10a coppia di nervi cranici e delle radici anteriori dei segmenti sacrali del midollo spinale. Il neurotrasmettitore delle fibre pre e postgangliari è l'acetilcolina. Oltre a ciò, il ruolo di mediatori in questi gangli è svolto dalla serotonina, dall'ATP e possibilmente da alcuni peptidi.
La maggior parte degli organi interni hanno una doppia innervazione autonomica, cioè ricevono fibre postgangliari da cellule situate sia nei nodi simpatici che in quelli parasimpatici. Le reazioni mediate dalle cellule dei nodi simpatico e parasimpatico spesso hanno la direzione opposta, ad esempio: aumenta la stimolazione simpatica e la stimolazione parasimpatica inibisce l'attività cardiaca.
La struttura generale dei gangli nervosi simpatici e parasimpatici è simile. Nodo vegetativo ricoperto da una capsula di tessuto connettivo e contiene corpi diffusi o localizzati in gruppi di neuroni multipolari, i loro processi sotto forma di fibre non mielinizzate o, meno comunemente, mielinizzate ed endoneuria. I corpi cellulari dei neuroni hanno una forma irregolare, contengono un nucleo situato in posizione eccentrica e sono circondati (di solito non completamente) da membrane di cellule satelliti gliali (gliociti del mantello). Sono comuni i neuroni multinucleati e poliploidi.
Nodi intramurali e i percorsi associati, a causa della loro elevata autonomia, complessità organizzativa e caratteristiche dello scambio di mediatori, sono identificati da alcuni autori come una divisione metasimpatica indipendente del SNA. In particolare, il numero totale di neuroni nei nodi intramurali dell'intestino è maggiore che nel midollo spinale e, in termini di complessità della loro interazione nella regolazione della peristalsi e della secrezione, sono paragonati a un minicomputer.
Nei nodi intramurali sono descritti 3 tipi di neuroni:
neuroni efferenti assonali lunghi (cellule Dogel di tipo I) dominare numericamente. Si tratta di neuroni efferenti di grandi o medie dimensioni con dendriti corti e un lungo assone che va verso l'esterno verso l'organo funzionante, sulle cellule del quale forma terminazioni motorie o secretorie;
Neuroni afferenti equiprocessi (cellule Dogel di tipo II) contengono lunghi dendriti e un assone che si estende oltre i confini di un dato ganglio in quelli vicini e forma sinapsi sulle cellule di tipo I e III. Queste cellule, apparentemente, sono incluse come collegamento recettoriale negli archi riflessi locali, che si chiudono senza che l'impulso nervoso entri nel sistema nervoso centrale. La presenza di tali archi è confermata dalla conservazione dei neuroni afferenti, associativi ed efferenti funzionalmente attivi negli organi trapiantati (ad esempio il cuore);
cellule associative (cellule Dogel tipo III) - interneuroni locali che collegano con i loro processi diverse cellule di tipo I e II, morfologicamente simili alle cellule Dogel di tipo II. I dendriti di queste cellule non si estendono oltre il nodo e gli assoni vengono inviati ad altri nodi, formando sinapsi sulle cellule di tipo I.
Organizzazione del midollo spinale
\. Midollo spinalesi trova nel canale spinale e ha l'aspetto di un midollo arrotondato, espanso nelle regioni cervicale e lombare e penetrato dal canale centrale.
È costituito da 2 metà simmetriche, separate anteriormente dalla fessura mediana, posteriormente dal solco mediano, ed è caratterizzato da una struttura segmentale; ciascun segmento è associato a una coppia di radici anteriori (ventrali) e a una coppia di radici posteriori (dorsali).
Nel midollo spinaledistinguere:
· Materia grigia, situato nella sua parte centrale;
· materia bianca sdraiato alla periferia.
materia grigia in sezione trasversale sembra una farfalla e include:
Raddoppia davanti(ventrale);
posteriore(dorsale);
laterale corna (laterali) (in realtà colonne continue che corrono lungo il midollo spinale).
Ognuno di noi almeno una volta nella vita ha pronunciato la frase "Ho un riflesso", ma pochi hanno capito di cosa stavano parlando esattamente. Quasi tutta la nostra vita si basa sui riflessi. Durante l’infanzia ci aiutano a sopravvivere e in età adulta ci aiutano a lavorare in modo efficace e a rimanere in salute. Sottomettendoci ai riflessi, respiriamo, camminiamo, mangiamo e molto altro ancora.
Riflesso
Un riflesso è la risposta del corpo a uno stimolo, effettuato dall'inizio o dalla cessazione di qualsiasi attività: movimento muscolare, secrezione delle ghiandole, cambiamenti del tono vascolare. Ciò consente di adattarsi rapidamente ai cambiamenti nell'ambiente esterno. L’importanza dei riflessi nella vita di una persona è così grande che anche la loro parziale esclusione (rimozione durante un intervento chirurgico, trauma, ictus, epilessia) porta alla disabilità permanente.
Lo studio è stato condotto da I.P. Pavlov e I.M. Sechenov. Hanno lasciato molte informazioni per le future generazioni di medici. In precedenza, la psichiatria e la neurologia non erano separate, ma dopo il loro lavoro i neurologi hanno iniziato a praticare separatamente, ad accumulare esperienza e ad analizzarla.
Tipi di riflessi
A livello globale, i riflessi sono divisi in condizionati e incondizionati. I primi sorgono in una persona nel processo della vita e sono associati, per la maggior parte, a ciò che fa. Alcune delle abilità acquisite scompaiono nel tempo e il loro posto viene preso da nuove, più necessarie nelle condizioni date. Questi includono andare in bicicletta, ballare, suonare strumenti musicali, creare oggetti, guidare e molto altro. Tali riflessi sono talvolta chiamati “stereotipo dinamico”.
I riflessi inconsci sono inerenti a tutte le persone allo stesso modo e sono presenti a noi dal momento della nascita. Persistono per tutta la vita, poiché sono loro che sostengono la nostra esistenza. Le persone non pensano al fatto che hanno bisogno di respirare, di contrarre il muscolo cardiaco, di tenere il corpo nello spazio in una certa posizione, di battere le palpebre, di starnutire, ecc. Ciò avviene automaticamente perché la natura si è presa cura di noi.
Classificazione dei riflessi
Esistono diverse classificazioni di riflessi che riflettono le loro funzioni o indicano il livello di percezione. Alcuni di essi possono essere citati.
In base al loro significato biologico, i riflessi si distinguono:
- cibo;
- protettivo;
- sessuale;
- indicativo;
- riflessi che determinano la posizione del corpo (posetonici);
- riflessi per il movimento.
In base alla localizzazione dei recettori che percepiscono lo stimolo possiamo distinguere:
- esterocettori situati sulla pelle e sulle mucose;
- interorecettori situati negli organi interni e nei vasi sanguigni;
- propriocettori che percepiscono l'irritazione di muscoli, articolazioni e tendini.
Conoscendo le tre classificazioni presentate, puoi caratterizzare qualsiasi riflesso: acquisito o connato, quale funzione svolge e come provocarlo.
Livelli dell'arco riflesso

È importante che i neurologi conoscano il livello al quale il riflesso si chiude. Ciò aiuta a determinare con maggiore precisione l'area interessata e a prevedere danni alla salute. Ci sono i riflessi spinali che si trovano nell'organismo. Sono responsabili della meccanica del corpo, della contrazione muscolare e del funzionamento degli organi pelvici. Salendo a un livello più alto: nel midollo allungato si trovano i centri bulbari che regolano le ghiandole salivari, alcuni muscoli facciali, la funzione della respirazione e il battito cardiaco. Il danno a questo dipartimento è quasi sempre fatale.
I riflessi mesencefalici sono chiusi nel mesencefalo. Questi sono principalmente archi riflessi dei nervi cranici. Esistono anche riflessi diencefalici, il cui neurone finale si trova nel diencefalo. E i riflessi corticali, che sono controllati dalla corteccia cerebrale. In genere si tratta di abilità apprese.
Va tenuto presente che la struttura dell'arco riflesso con la partecipazione dei centri di coordinamento più alti del sistema nervoso comprende sempre livelli inferiori. Cioè, il tratto corticospinale passerà attraverso il midollo intermedio, medio, e il midollo spinale.
La fisiologia del sistema nervoso è progettata in modo tale che ogni riflesso sia duplicato da diversi archi. Ciò consente di mantenere le funzioni del corpo anche in caso di infortuni e malattie.
Arco riflesso

L'arco riflesso è una via di trasmissione dall'organo percettivo (recettore) all'esecutore. L'arco nervoso riflesso è costituito da neuroni e dai loro processi che formano una catena. Questo concetto fu introdotto in medicina da M. Hall a metà del XIX secolo, ma col tempo si trasformò in un “anello riflesso”. È stato deciso che questo termine riflette più pienamente i processi che si verificano nel sistema nervoso.
In fisiologia si distinguono archi monosinaptici, così come archi a due e tre neuroni; a volte ci sono riflessi polisinaptici, cioè inclusi più di tre neuroni. L'arco più semplice è formato da due neuroni: uno sensoriale e uno motorio. L'impulso passa lungo il lungo processo del neurone che, a sua volta, lo trasmette al muscolo. Tali riflessi sono generalmente incondizionati.
Divisioni dell'arco riflesso

La struttura dell'arco riflesso comprende cinque sezioni.
Il primo è un recettore che percepisce le informazioni. Può localizzarsi sia sulla superficie del corpo (pelle, mucose) che nelle sue profondità (retina, tendini, muscoli). Morfologicamente, il recettore può apparire come un lungo processo di un neurone o un gruppo di cellule.
La seconda sezione è sensibile, che trasmette l'eccitazione ulteriormente lungo l'arco. I corpi di questi neuroni si trovano all'esterno, nei gangli spinali. La loro funzione è simile a quella di uno scambio sui binari della ferrovia. Cioè, questi neuroni distribuiscono le informazioni che arrivano loro a diversi livelli del sistema nervoso centrale.
La terza sezione è il luogo in cui la fibra sensoriale passa alla fibra motoria. Per la maggior parte dei riflessi si trova nel midollo spinale, ma alcuni archi complessi passano direttamente attraverso il cervello, ad esempio i riflessi protettivi, di orientamento e alimentari.
La quarta sezione è rappresentata dalla fibra motoria, che trasmette l'impulso nervoso dal midollo spinale al motoneurone effettore.
L'ultima, la quinta sezione è un organo che svolge l'attività riflessa. Tipicamente si tratta di un muscolo o di una ghiandola, come la pupilla, il cuore, le gonadi o le ghiandole salivari.
Proprietà fisiologiche dei centri nervosi

La fisiologia del sistema nervoso è variabile ai suoi diversi livelli. Quanto più tardi si forma il dipartimento, tanto più complessi sono il suo lavoro e la regolazione ormonale. Ci sono sei proprietà inerenti a tutti i centri nervosi, indipendentemente dalla loro topografia:
Condurre l'eccitazione solo dal recettore al neurone effettore. Fisiologicamente ciò è dovuto al fatto che le sinapsi (le giunzioni dei neuroni) agiscono solo in una direzione e non possono modificarla.
Il ritardo nella conduzione dell'eccitazione nervosa è anche associato alla presenza di un gran numero di neuroni nell'arco e, di conseguenza, di sinapsi. Per sintetizzare un trasmettitore (stimolo chimico), rilasciarlo nella fessura sinaptica e avviare così l'eccitazione, ci vuole più tempo che se l'impulso si propagasse semplicemente lungo la fibra nervosa.
Somma delle eccitazioni. Ciò accade se lo stimolo è debole, ma ripetuto costantemente e ritmicamente. In questo caso, il trasmettitore si accumula nella membrana sinaptica fino a quando non ne rimane una quantità significativa, e solo allora trasmette l'impulso. L'esempio più semplice di questo fenomeno è l'atto di starnutire.
Trasformazione del ritmo delle eccitazioni. La struttura dell'arco riflesso, così come le caratteristiche del sistema nervoso, sono tali che anche a un ritmo lento dello stimolo risponde con impulsi frequenti - da cinquanta a duecento volte al secondo. Pertanto, i muscoli del corpo umano si contraggono tetanicamente, cioè in modo intermittente.
Effetto collaterale riflesso. I neuroni dell'arco riflesso rimangono in uno stato eccitato per qualche tempo dopo la cessazione dello stimolo. Ci sono due teorie su questo argomento. La prima afferma che le cellule nervose trasmettono l'eccitazione per una frazione di secondo più lunga dell'azione dello stimolo, prolungando così il riflesso. Il secondo si basa su un anello riflesso, che si chiude tra due neuroni intermedi. Trasmettono l'eccitazione finché uno di loro non riesce a generare un impulso, oppure finché non arriva un segnale inibitorio dall'esterno.
L'annegamento dei centri nervosi si verifica con un'irritazione prolungata dei recettori. Ciò si manifesta prima come una diminuzione e poi come una completa mancanza di sensibilità.
Arco riflesso autonomo
In base al tipo di sistema nervoso che implementa l'eccitazione e conduce gli impulsi nervosi, si distinguono gli archi nervosi somatici e autonomi. La particolarità è che il riflesso ai muscoli scheletrici non viene interrotto e quello autonomo passa necessariamente attraverso il ganglio. Tutti i nodi nervosi possono essere divisi in tre gruppi:
- I gangli vertebrali (vertebrali) sono legati al sistema nervoso simpatico. Si trovano su entrambi i lati della colonna vertebrale, formando pilastri.
- I nodi prevertebrali si trovano a una certa distanza sia dalla colonna vertebrale che dagli organi. Questi includono il ganglio ciliare, i nodi simpatici cervicali, il plesso solare e i nodi mesenterici.
- I nodi intraorganici, come puoi immaginare, si trovano negli organi interni: il muscolo cardiaco, i bronchi, il tubo intestinale, le ghiandole endocrine.
Queste differenze tra il sistema somatico e quello vegetativo affondano nella filogenesi e sono associate alla velocità di diffusione dei riflessi e alla loro necessità vitale.
Attuazione del riflesso

Dall'esterno, il recettore dell'arco riflesso riceve irritazione, che provoca eccitazione e la comparsa di un impulso nervoso. Questo processo si basa su un cambiamento nella concentrazione degli ioni calcio e sodio, che si trovano su entrambi i lati della membrana cellulare. Un cambiamento nel numero di anioni e cationi provoca uno spostamento del potenziale elettrico e la comparsa di una scarica.
Dal recettore, l'eccitazione, muovendosi centripetamente, entra nel collegamento afferente dell'arco riflesso: il nodo spinale. Il suo processo entra nel midollo spinale fino ai nuclei sensoriali e quindi passa ai motoneuroni. Questo è l'anello centrale del riflesso. I processi dei nuclei motori emergono dal midollo spinale insieme ad altre radici e sono diretti al corrispondente organo esecutivo. Nello spessore dei muscoli le fibre terminano con una placca motoria.
La velocità di trasmissione dell'impulso dipende dal tipo di fibra nervosa e può variare da 0,5 a 100 metri al secondo. L'eccitazione non si diffonde ai nervi vicini a causa della presenza di membrane che isolano i processi l'uno dall'altro.
Il valore dell'inibizione del riflesso
Poiché una fibra nervosa può mantenere l'eccitazione per lungo tempo, l'inibizione è un importante meccanismo di adattamento del corpo. Grazie ad esso, le cellule nervose non subiscono costante sovraeccitazione e affaticamento. L'afferenza inversa, grazie alla quale si realizza l'inibizione, è coinvolta nella formazione dei riflessi condizionati e solleva il sistema nervoso centrale dalla necessità di analizzare compiti secondari. Ciò garantisce la coordinazione dei riflessi, come i movimenti.
L'afferenza inversa impedisce inoltre la diffusione degli impulsi nervosi ad altre strutture del sistema nervoso, mantenendone la funzionalità.
Coordinazione del sistema nervoso

In una persona sana tutti gli organi agiscono in armonia e di concerto. Sono soggetti ad un sistema di coordinamento unificato. La struttura dell'arco riflesso è un caso speciale che conferma un'unica regola. Come in qualsiasi altro sistema, anche negli esseri umani esistono una serie di principi o modelli in base ai quali funziona:
- convergenza (gli impulsi provenienti da diverse aree possono arrivare a un'area del sistema nervoso centrale);
- irradiazione (un'irritazione prolungata e forte provoca l'eccitazione delle aree vicine);
- alcuni riflessi da parte di altri);
- percorso finale comune (basato sulla discrepanza tra il numero di neuroni afferenti e quelli efferenti);
- feedback (autoregolazione del sistema in base al numero di impulsi ricevuti e generati);
- dominante (la presenza di un focus principale di eccitazione che si sovrappone agli altri).