Follow-up ambulatoriale dei pazienti dopo danno renale acuto. Danno renale acuto: stadi della patogenesi e metodi di terapia. Azioni quando non esiste una minaccia immediata per la vita del paziente
Creatinina sierica* - creatinina sierica, CF**- filtrazione glomerulare(vedi appendice 1, 2).
Gli studi condotti sui bambini poco dopo hanno mostrato quasi lo stesso valore dei criteri selezionati per l’AKI infanzia(Tavolo 2).
Tavolo 2
Criteri RIFLE modificati per i bambini (ADQI, 2007)
Nel considerare il problema di determinare e stratificare la gravità dell’AKI, gli esperti dell’ADQI si sono basati su una serie di principi:
· I cambiamenti nella funzionalità renale devono essere misurati a partire da un certo livello basale;
· Deve essere considerata la possibilità di un deterioramento acuto della funzionalità renale in pazienti con disfunzione renale cronica preesistente (“AKI associato a CKD”);
I criteri per la diagnosi e la valutazione della gravità dell’AKI dovrebbero essere facilmente applicabili in diversi casi centri clinici;
· È necessario determinare la sensibilità e la specificità di questi criteri.
Pertanto, per determinare l'AKI, sono stati selezionati 2 criteri: creatinina sierica e diuresi. Va tenuto presente che nel 50% degli AKI può essere non oligurico, cioè Cr.syv. in questi casi, questo è l’unico criterio per l’AKI. Il valore diagnostico del RIFLE è stato confermato in >200.000 casi.
Un'altra Internazionale gruppo di lavoro per lo studio dell'AKI - AKIN ha proposto una classificazione molto simile a RIFLE (Tabella 3).
Tabella 3
Classificazione dell'AKI (AKIN)
Le differenze tra queste due classificazioni sono che RIFLE valuta l'aumento dei livelli di creatinina entro 7 giorni e AKIN - entro 48 ore. Anche in quest’ultimo, come si vede dalla Tabella 3, vengono evidenziate le prime 3 fasi anziché 5.
Durante la preparazione di questo sussidio didattico nel marzo 2012, “Pratico Linee guida cliniche su APP" sotto gli auspici di KDIGO, dove fornito seguente definizione OPP, tenendo conto delle proposte di entrambi questi gruppi.
Tabella 4
Fasi dell'AKI (KDIGO, 2012)
Viene proposta una nuova definizione di AKI non solo per il nefrologo e l'intensivista, ma anche per i medici che non riscontrano AKI tutti i giorni. Ciò determinerà la familiarità di questi medici con i criteri per l’AKI lati positivi nuova classificazione. Non sostituisce altre classificazioni di AKI. I criteri per l'AKI avvisano il medico di un possibile AKI e aiutano a diagnosticarlo in modo tempestivo, inclusa la sua variante non oligurica. Si propone di prendere in considerazione la possibilità di un rapido sviluppo (meno di 48 ore) di diminuzione della funzionalità renale e, come linea guida, incremento assoluto creatinina durante questo periodo di ≥ 26,5 µmol/l. Lo sviluppo dell'AKI può verificarsi entro 1-7 giorni e il livello di creatinina può aumentare di 1,5 volte o più. Dalla classificazione consegue che la disfunzione renale, esistente anche da più di un mese, può essere considerata “acuta”. La classificazione RIFLE ci consente di determinare la linea temporale tra AKI e CKD. L'AKI è presente da meno di 3 mesi.
· Se il paziente soffre di insufficienza renale cronica, il suo trattamento deve essere effettuato in conformità con Raccomandazioni pratiche KDOQI per la gestione della malattia renale cronica.
· Se un paziente non soffre di insufficienza renale cronica, è necessario tenere presente che il paziente ha un rischio maggiore di sviluppare insufficienza renale cronica e deve essere gestito in conformità con le linee guida pratiche KDOQI.
I pazienti a rischio di sviluppare AKI devono essere attentamente monitorati per la pressione arteriosa. e il volume delle urine. La loro gestione dipende da fattori predisponenti. Prima di tutto, i pazienti dovrebbero essere esaminati per identificare cause reversibili AKI, che eliminerà immediatamente questi fattori (ad esempio postrenale).
CAUSE E CLASSIFICAZIONE DEL DANNO RENALE ACUTO
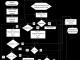
Secondo il principale meccanismo di sviluppo, l'AKI è diviso in 3 gruppi: prerenale, renale e postrenale. Molte ragioni possono portare al loro sviluppo (Fig. 1).
Immagine 1. Classificazione delle principali cause di AKI (Tomilina N.A., Podkorytnaya L.P., 2009).
Cause prerenali
Le cause prerenali rappresentano la maggior parte dei casi di AKI. Costituiscono la parte predominante (50-60%) dell’AKI. Spettro delle cause di AKI in paesi sviluppatiè cambiato negli ultimi decenni a causa dell'introduzione di nuovi metodi diagnostici e attività terapeutiche(il cosiddetto AKI “acquisito in ospedale”). La percentuale di casi di AKI grave che necessitano di terapia dialitica è aumentata negli ultimi 30 anni. L'AKI prerenale può verificarsi in pazienti con ipovolemia (diminuzione del volume sanguigno circolante) o normoipervolemia (riempimento insufficiente delle arterie) (Fig. 2).
Figura 2. Cause di prerenal acuto danno ai reni(Tomilina N.A., Podkorytnaya L.P., 2009).
Diminuzione vera BCC o ipovolemia si sviluppa a seguito di sanguinamento, vomito, diarrea, ustioni, aumento della diuresi dopo diuretici, diuresi osmotica (glicosuria), nonché condizioni con ridistribuzione dei volumi di liquidi corporei (sequestro fluido extracellulare o perdita del “terzo spazio”), che si verificano con peritonite, pancreatite, sindrome nefrosica e altri casi che si verificano con ipoalbuminemia grave, sindrome da risposta infiammatoria sistemica.
Una bambina di 1,5 anni nella scuola materna ospedale per malattie infettive, la diuresi è diminuita a completa assenza. L'insorgenza della malattia, secondo la madre, è avvenuta 3 giorni fa dall'esordio del diarrea fino a 15-20 volte al giorno, colore giallo-verde, vomito 7-8 volte al giorno con cibo e liquidi. All'esame, la ragazza è cosciente, letargica, gli occhi infossati, la pelle secca, il turgore della pelle è nettamente ridotto. Il tempo di ripristino capillare del flusso sanguigno è superiore a 4 secondi. Peso corporeo 9,8 kg, altezza 88 cm (pesato un mese fa, il peso era 12,9 kg). Fenomeni catarrali NO, linfonodi periferici non ingrandito. Nei polmoni respirare è difficile, nessun respiro sibilante. I suoni cardiaci sono ovattati, tachicardia, frequenza cardiaca 150/min, pressione arteriosa 65/30 mmHg. L'addome non è ingrandito, doloroso alla palpazione nella zona dell'ombelico, il fegato e la milza non sono ingranditi. Non c'è urina, la diuresi si è fermata. Emocromo: HB 140 g/l, eritrociti 5,4*10 12 /l, ematocrito 52%, leucociti 12,5*10 9 /l, piastrine 715*10 9 /l. Analisi biochimica sangue: creatinina 150 µmol/l, urea 15 mmol/l, potassio 2,3 mmol/l, sodio 148 mmol/l. Nelle urine (10 ml ricevuti attraverso il catetere uretrale): sodio 10 mmol/l, urea 42 mmol/l, creatinina 1500 µmol/l. FE Na<0,7%, FE Ur 28%(см. приложения 5, 6 и таблицу 6).
Discussione
Il bambino è gravemente disidratato con perdita di peso >3 kg al giorno poco tempo(più del 20% del peso corporeo). La disidratazione, non corretta fin dalle prime ore, è diventata la causa dello sviluppo del danno renale acuto prerenale. La genesi prerenale dell'AKI è confermata da ematocrito elevato, trombocitosi nell'emocromo, alto contenuto creatinina e basso contenuto di sodio nelle urine, ridotta frazione di sodio escreto nelle urine FeNa<1% на фоне нормального уровня натрия в крови, сниженной фракцией экскретируемой мочевины (< 35%) и характерным соотношением мочевина/креатинин в крови.
Secondo la classificazione RIFLE per i bambini (Tabella 2), una diminuzione del GFR inferiore a 30 ml/min (o una diminuzione superiore al 75% rispetto al basale) indica un AKI di stadio 3 (F). Secondo KDIGO, 2012: aumento della creatinina >3 volte il livello basale stimato per quell'età o livello di GFR<35 мл/мин говорит о стадии F «недостаточность» (таблица 4). Второй критерий – нарушение диуреза - анурия, хотя ее длительность не совсем известна, также говорит о 3 стадии. Таким образом, оба критерия (СКФ и диурез), также уровниFЕ Na и FE Ur соответствуют диагнозу: ОПП, преренальная, стадия 3 (F).
La terapia dovrebbe mirare ad eliminare rapidamente la disidratazione: per via orale o attraverso un sondino nasogastrico - reidrone, somministrazione parenterale di cristalloidi, nutrizione enterale. La prognosi con reidratazione tempestiva ed eliminazione della causa prerenale è favorevole. È pericoloso lo sviluppo di grave exicosi e ipovolemia con transizione alla forma renale dell'AKI, che può richiedere una terapia sostitutiva renale (vedere il capitolo "Trattamento").
Riempimento insufficiente delle arterie - questa è una condizione in cui il volume del sangue è normale o addirittura aumentato, ma quando i fattori circolatori non sono in grado di mantenere un'adeguata perfusione dei reni. Questa variante di AKI prerenale si sviluppa secondariamente in pazienti con cardiopatia con ridotta gittata cardiaca.
Esempio clinico n. 2
Un uomo di 70 anni con ipertensione arteriosa e aterosclerosi vascolare è stato ricoverato in ospedale lamentando mancanza di respiro, difficoltà di respirazione in posizione supina e attacchi notturni di mancanza di respiro spontaneo negli ultimi 10 giorni. Nell'ultima settimana ho preso 5 kg di peso e mi sono comparsi dei gonfiori alle caviglie. Prende digossina 0,25 mcg al giorno e furosemide 80 mg una volta. Fisicamente – rantoli umidi bilaterali nei polmoni. Esami del sangue di laboratorio: sodio 133 mmol/l, creatinina 150 µmol/l, azoto ureico 13 mmol/l. È stato prescritto riposo a letto, indapamide 5 mg/giorno, la dose di furosemide è stata aumentata a 120 mg*2 volte/giorno. Nei successivi 3 giorni il paziente ha perso peso 8 kg, pressione arteriosa 90/50 mmHg, ma durante questo periodo l'urea nel sangue è aumentata a 21,6 mmol/l, la creatinina a 208 μmol/l.
Discussione
Il paziente presenta sintomi di insufficienza cardiaca ventricolare sia sinistra che destra. A causa dell’insufficienza cardiaca cronica (CHF), si è verificata una diminuzione dell’afflusso di sangue ai tessuti. La gittata cardiaca è mantenuta da un elevato riempimento ventricolare, che porta a edema polmonare ed edema periferico. L'aumento dell'urea e della creatinina è moderato. Il grado di aumento dell'urea è maggiore che della creatinina, il che è una conseguenza dell'ipoperfusione renale, ad es. L’AKI è di origine prerenale. Il trattamento con diuretici porta ad una diminuzione della pressione e al riempimento dei ventricoli del cuore e alla rimozione parziale del liquido edematoso. Ma si verifica un'ulteriore diminuzione della perfusione tissutale, che si riflette nel successivo aumento dell'urea e della creatinina sierica e del rapporto urea/creatinina.
Il paziente presenta AKI, prerenale, dovuto a insufficienza cardiaca, stadio 1 con passaggio allo stadio 2.
La vasodilatazione periferica durante sepsi, insufficienza epatica, shock anafilattico e dovuta all'azione di farmaci antipertensivi e anestetici può anche portare ad azotemia prerenale. Una forma specifica di AKI prerenale, la sindrome epatorenale (HRS), si sviluppa in pazienti con grave insufficienza epatica. Ci sono 2 tipi. HRS di tipo 1, il più grave, si sviluppa rapidamente e senza trapianto di fegato, la mortalità entro 3 mesi è del 90% (R. Schreyer, 2009). La HRS di tipo 2 si sviluppa in pazienti con ascite refrattaria e progredisce lentamente.
Nei disturbi emodinamici intrarenali che si sviluppano a seguito di vari farmaci, l'AKI prerenale si verifica a causa di due effetti: costrizione delle arteriole afferenti (effetto preglomerulare) o dilatazione delle arteriole efferenti (effetto postglomerulare) (Fig. 2).
Nell’AKI prerenale, la ridotta velocità di filtrazione glomerulare non è accompagnata da danno strutturale o cellulare ai reni. L’AKI prerenale è reversibile quando le condizioni che hanno portato all’ipoperfusione renale si risolvono.
UDC 616-089-06
G.N. Chingaeva,MA Zhumabekova, G.B. Mamuova, M.B. Orazimbetova, A.B. Bakyt, A.B. Bakaeva
Università medica nazionale kazaka intitolata a S.D. Asfendiyarova,
modulo di nefrologia, Almaty
Questo articolo presenta un nuovo concetto di insufficienza renale acuta: danno renale acuto, sviluppato e introdotto nella pratica nel 2004. Viene presentato un sistema per stratificare la sua gravità (FUCILE-criteri), criteri per diagnosticare e valutare la gravità di questa condizione, la sua modifica (SIMILE-criteri) per la diagnosi precoce della disfunzione renale e la prevenzione dello sviluppo di insufficienza renale. Sono stati sviluppati i primi biomarcatori per la diagnosi di danno renale acuto.
Parole chiave: danno renale acuto,FUCILE-criteri, modificazioni, biomarcatori
L’insufficienza renale acuta (IRA) è uno dei problemi più urgenti e significativi della moderna nefrologia e dell’assistenza sanitaria in generale. Fino a poco tempo fa, la definizione e i criteri diagnostici dell'insufficienza renale acuta erano arbitrari; non esistevano criteri diagnostici uniformi, il che rendeva difficile la diagnosi tempestiva, tenendo conto della sua prevalenza e dell'efficacia del trattamento. L'ARF è un problema multidisciplinare, poiché le sue cause sono molteplici e si verificano nella pratica di qualsiasi medico. L’incidenza dell’AKI varia tra la popolazione generale e la popolazione ospedalizzata e critica.
Attualmente, gli approcci alla definizione del termine stesso scaricatore di sovratensione sono radicalmente cambiati. Ciò è stato preceduto da numerosi studi avviati nel 2000 da una Consensus Conference sotto gli auspici dell'American Society of Nephrology e della Society of Intensive Care Specialists. L'obiettivo era unificare la terminologia e sviluppare raccomandazioni per la diagnosi tempestiva e il trattamento dell'insufficienza renale acuta. Nel 2004, il gruppo di lavoro ADQI (Acute Dialysis Quality Initiative) ha analizzato 199 diversi criteri per definire l’AKI e 90 per iniziare la terapia sostitutiva renale.
Definizione di danno renale acuto
Nel 2004, l’ADQI ha proposto il concetto di “danno renale acuto” (AKI), che ha sostituito il termine “insufficienza renale acuta” e una classificazione chiamata RIFLE secondo le prime lettere di ciascuna delle fasi sequenziali dell’AKI: Rischio (Rischio), Danno (lesione), fallimento (fallimento), perdita, malattia renale allo stadio terminale (Tabella 1). RIFLE rappresenta il primo passo nello sviluppo di un approccio sistematico alla gestione dei pazienti con AKI basato sulla medicina basata sull’evidenza.
Tabella 1 - Classificazione dell'AKI per classi RIFLE (2004)
| Classi | Criteri per la diuresi | |
| Rischio | Scr* di 1,5 volte oppure ↓ CF** del 25% | <0,5 мл/кг/час ≥6 часов |
| Danno | Scr 2 volte oppure ↓ CF del 50% | <0,5 мл/кг/час ≥12 часов |
| Fallimento | Scr 3 volte oppure ↓ CF del 75% oppure Scr≥354 µmol/l con incremento di almeno 44,2 µmol/l | <0,3 мл/кг/час ≥24 часов или анурия ≥12 часов |
| Perdita della funzionalità renale | Insufficienza renale acuta persistente; perdita completa della funzionalità renale >4 settimane | |
| ESRD>3 mesi | ||
| Scr*-creatinina sierica, CF**-filtrazione glomerulare | ||
RIFLE comprende non solo la valutazione di 3 livelli di disfunzione renale (R, I, F), ma anche 2 punti finali del decorso dell'AKI: L ed E. Pertanto, la differenza nei processi adattativi tra pazienti con disfunzione renale reversibile e irreversibile viene sottolineato, con il possibile passaggio all’insufficienza renale cronica. Studi condotti sui bambini poco dopo hanno mostrato quasi lo stesso valore dei criteri selezionati per l’AKI durante l’infanzia (Tabella 2).
Tabella 2 - Criteri RIFLE modificati per i bambini (2007)
| Classi | Criteri di filtrazione glomerulare | Criteri per la diuresi |
| Rischio | Riduzione della FC del 25% | <0,5 мл/кг/час x 8 часов |
| Danno | Riduzione della FC del 50% | <0,5 мл/кг/час x 16 часов |
| Fallimento | Diminuzione dell'EF del 75% o ↓GFR<30 мл/мин/1,73м 2 | <0,3 мл/кг/час x 24 часов или анурия в течение 12 часов |
| Perdita della funzionalità renale | Insufficienza renale acuta persistente; perdita completa della funzionalità renale >4 settimane | |
| Insufficienza renale allo stadio terminale | ESRD>3 mesi | |
Nel considerare il problema di determinare e stratificare la gravità dell’AKI, gli esperti dell’ADQI si sono basati su una serie di principi:
- I cambiamenti nella funzionalità renale devono essere referenziati a partire da uno specifico livello basale;
- La possibilità di un deterioramento acuto della funzionalità renale deve essere presa in considerazione nei pazienti con disfunzione renale cronica preesistente (“AKI associato a CKD”);
- I criteri per la diagnosi e la valutazione della gravità dell’AKI dovrebbero essere facilmente applicabili in tutti i siti clinici;
- La sensibilità e la specificità di questi criteri devono essere determinate.
Pertanto, per determinare l'AKI nei criteri RIFLE, sono stati selezionati 2 criteri: i parametri clinici più comunemente utilizzati per valutare la funzionalità renale. È necessario tenere presente che nel 50% degli AKI può essere non oligurico, cioè Scr in questi casi è l'unico criterio per l'AKI. Il valore diagnostico del RIFLE è stato confermato in >200.000 casi.
Nel 2007, il gruppo di lavoro internazionale AKIN (Acute Kidney Injury Network) ha proposto criteri RIFLE migliorati per aumentarne la sensibilità, anche per piccole deviazioni della concentrazione di creatinina nel sangue nella prima fase (rischio/stadio 1). Questo passo è stato giustificato dai dati secondo i quali anche piccole deviazioni nel valore assoluto della concentrazione di creatinina hanno avuto un impatto sul numero di complicanze e sulla mortalità. È stato inoltre suggerito che qualsiasi paziente sottoposto a terapia sostitutiva renale debba essere classificato allo stadio 3 (Tabella 3).
Tabella 3 - Stadi dell'AKI secondo AKIN
|
Criteri basati su Scr |
Criteri basati sul volume delle urine | |
| Scr ≥ 26 µmol/l, o dal 150 al 200% (1,5-2 volte) del basale | <0,5 мл/кг/час в течение более чем 6 часов | |
| Scr più del 200%, ma meno del 300% (più di 2, ma meno di 3 volte) della base | <0,5 мл/кг/час в течение более чем 12 часов | |
| Scr superiore al 300% (più di 3 volte) del basale o Cr ≥ 350 µmol/l con un rapido aumento superiore a 44 µmol/l | <0,3 мл/кг/час в течение 24 ч или анурия в течение 12 ч |
Le differenze tra queste due classificazioni sono che RIFLE valuta l'aumento dei livelli di creatinina entro 7 giorni e AKIN - entro 48 ore. Anche in quest’ultimo, come si vede dalla Tabella 3, si distinguono 3 stadi anziché 5. I gradi RIFLE L ed E derivano da questa classificazione e sono considerati esiti dell'AKI. Allo stesso tempo, la categoria R nel sistema RIFLE coincide essenzialmente con quelle della diagnosi di stadio 1 AKI nel sistema AKIN, e le classi I e F secondo RIFLE corrispondono agli stadi 2 e 3 secondo AKIN.
Secondo gli esperti di AKIN, la diagnosi di AKI può essere stabilita quando si verifica una rapida (entro 48 ore) diminuzione della funzionalità renale, che attualmente viene definita come un aumento dei valori assoluti di Scr di 26,5 μmol/L o più; un aumento relativo della concentrazione di creatinina pari o superiore al 50% (1,5 volte il livello iniziale) o una diminuzione del volume delle urine (oliguria documentata con produzione di urina inferiore a 0,5 ml/kg di peso corporeo/ora per 6 ore).
Gli esperti AKIN hanno inoltre proposto un sistema per stratificare la gravità dell’AKI, che è una modifica del sistema RIFLE (Tabella 4).
Tabella 4 – Sistema modificato per la diagnosi e la stratificazione della gravità dell'AKI
| Palcoscenico | Criteri basati su Scr |
Criteri basati sul GFR* |
Criteri basati sul volume delle urine |
| Nessuna variazione della Scr, in presenza di altri marcatori di danno renale |
Nessuna variazione del GFR o riduzione del GFR con valore Scr normale |
Nessun cambiamento |
|
| Un aumento della Scr maggiore o uguale a 26,4 µmol/l, o dal 150 al 200% (1,5-2 volte) del basale |
Riduzione del GFR di oltre il 25% |
Meno di 0,5 ml/kg/h >6 ore |
|
| Un aumento di Scr superiore al 200%, ma inferiore al 300% (più di 2, ma meno di 3 volte) dalla base. |
Diminuzione del GFR superiore al 50% ma inferiore al 75% |
Meno di 0,5 ml/kg/ora >12 ore |
|
| Un aumento della Scr superiore al 300% (più di 3 volte) rispetto al basale o una Scr ≥ 350 µmol/l con un rapido aumento superiore a 44 µmol/l |
Riduzione del GFR di oltre il 75% |
Meno di 0,3 ml/kg/h per 24 ore o anuria per 12 ore |
Nota: *utilizzato per l'AKI dovuto a malattie renali parenchimali primarie. Per stimare la GFR si dovrebbe utilizzare la clearance della creatinina, ma non metodi “calcolati” (MDRD, Cocroft-Cault, ecc.)
Pertanto, l’AKI è “una diminuzione improvvisa (entro 48 ore) e persistente della filtrazione glomerulare o del volume delle urine, o di entrambi”. In questo caso, una disfunzione renale che persiste anche per più di un mese può essere considerata “acuta”. L'AKI è presente da meno di 3 mesi. In genere, lo sviluppo dell'AKI avviene entro 1-7 giorni. Il criterio per la “sostenibilità” della disfunzione è la sua registrazione per 24 ore o più. Si propone inoltre di intendere l'AKI come un danno acuto (ore, settimane), potenzialmente reversibile al parenchima renale di varie eziologie e patogenesi con o senza diminuzione della funzione escretoria dei reni. Dall’analisi degli aspetti positivi e svantaggi della classificazione RIFLE emerge quanto segue:
A favore contro
In relazione a quanto sopra, diventa chiaro che la classificazione RIFLE dovrebbe certamente essere utilizzata, ma anche altre classificazioni non hanno perso il loro significato. Viene proposta una nuova definizione di AKI non solo per il nefrologo e il rianimatore, ma anche per i medici che riscontrano AKI non quotidianamente. Gli aspetti positivi della nuova classificazione dipenderanno da quanto questi medici conosceranno i criteri per l’AKI. Non sostituisce altre classificazioni di AKI. I criteri per l'AKI avvisano il medico di un possibile AKI e aiutano a diagnosticarlo in modo tempestivo, inclusa la sua variante non oligurica. Dalla classificazione consegue che la disfunzione renale, esistente anche da più di un mese, può essere considerata “acuta”. La classificazione RIFLE ci consente di determinare la linea temporale tra AKI e malattia renale cronica (CKD). L'AKI è presente da meno di 3 mesi.
Dalle linee guida pratiche KDIGO (2012): “I pazienti con AKI dovrebbero essere seguiti per 3 mesi per valutare il grado di recupero della funzionalità renale, la recidiva di AKI o il peggioramento della CKD preesistente.
- Se un paziente ha una malattia renale cronica, il suo trattamento deve essere conforme alle linee guida pratiche KDOQI per la gestione della malattia renale cronica.
- Se un paziente non soffre di insufficienza renale cronica, è necessario tenere presente che il paziente ha un rischio maggiore di sviluppare insufficienza renale cronica e deve essere gestito in conformità con le linee guida pratiche KDOQI.
I pazienti a rischio di sviluppare AKI devono essere attentamente monitorati per la Scr e la produzione di urina. Si raccomanda di dividere i pazienti in gruppi in base al grado di rischio di sviluppare AKI. La loro gestione dipende da fattori predisponenti. I pazienti dovrebbero essere valutati innanzitutto per identificare le cause reversibili dell'AKI in modo che questi fattori (p. es., postrenali) possano essere affrontati tempestivamente.
Gli esiti AKI sono considerati separatamente (Tabella 5).
Tabella 5 – Esiti dell'AKI
Diagnostica. I livelli di creatinina vengono solitamente misurati per determinare la funzionalità renale. Ma tieni presente che i livelli di creatinina possono rimanere normali per diverse ore dopo un danno renale acuto. Per valutare accuratamente la gravità della malattia, è necessario effettuare misurazioni continue della creatinina nell'arco di 1-3 giorni. Ciò limita l'uso del metodo.
È possibile che in futuro la cistatina C possa rappresentare un'alternativa più realistica alla creatinina sierica o alla clearance della creatinina.La cistatina C è una proteina non glicosilata, appartiene alla famiglia degli inibitori della cisteina proteinasi ed è identica alla post-gammaglobulina. ; identificato per la prima volta in pazienti con insufficienza renale come proteina nel liquido cerebrospinale e nelle urine. La cistatina C, sebbene classificata anche come biomarcatore di danno renale acuto, non è un marcatore diretto di danno parenchimale, ma riflette i cambiamenti nella velocità di filtrazione glomerulare. La cistatina C è attualmente riconosciuta dalla comunità medica globale come il marcatore endogeno più accurato della velocità di filtrazione glomerulare. La cistatina C è significativamente superiore alla creatinina nelle sue caratteristiche diagnostiche e praticamente non dipende dalla massa muscolare o dall'età del bambino. Tuttavia, da un punto di vista clinico, il ruolo della cistatina nel danno renale acuto e cronico non è attualmente determinato. Inoltre, l’introduzione diffusa di questo parametro nella pratica potrebbe essere ostacolata dall’elevato costo dei sistemi di test utilizzati per misurarlo.
Negli ultimi anni sono emerse pubblicazioni sulla necessità di formule empiriche più accurate per stimare il GFR nei bambini rispetto alla formula di Schwartz proposta negli anni ’70, che sovrastima il GFR. Un gruppo di scienziati statunitensi guidati da George J. Schwartz nel 2009 ha proposto una nuova formula empirica per il calcolo della GFR nei bambini (1-16 anni), che tiene conto dei livelli di cistatina C, creatinina e urea nel siero del sangue:
GFR= 39,1 x 0,516 x 0,294 x 0,169 x 1,099 maschio x 0,188
dove: GFR - velocità di filtrazione glomerulare (ml/min/1,73 m)
altezza - altezza (m)
Scr—creatinina sierica (mg/dL)
cistatina C—cistatina C sierica (mg/l)
BUN: azoto ureico nel sangue (mg/dL)
maschio: utilizzare un moltiplicatore di 1.099 per i figli maschi
Si stanno sviluppando marcatori precoci di AKI ischemico, equivalenti, ad esempio, a un marcatore come la determinazione delle troponine nell'ischemia cardiaca. Un metodo diagnostico molto informativo, anche per la pratica pediatrica, è la determinazione della lipocalina associata alla gelatinasi dei neutrofili (NGAL) nelle urine 2-4 ore dopo lo sviluppo dell'AKI, che consente di identificare i sintomi iniziali 24-46 ore più velocemente. danno rispetto alla rilevazione del livello di creatinina nel sangue e/o della quantità di urina escreta. Un altro marcatore, KIM-1 (molecola del danno renale), apre la possibilità non solo di individuare precocemente il danno ischemico, ma anche di monitorare l’efficacia delle misure di trattamento per l’AKI. Inoltre, è stato riscontrato che il rilevamento di uNGAL è il predittore più accurato di morte con un simultaneo aumento di KIM-1 e il loro livello potrebbe determinare la necessità di iniziare la dialisi.
Lipocalina-2, o siderocalina, o proteina di trasporto del ferro NGAL
Si accumula nei granuli di neutrofili. È espresso da molti tessuti, la sua sintesi da parte delle cellule epiteliali, anche nei tubuli prossimali, è stimolata durante l'infiammazione. Un aumento della concentrazione di proteine nelle urine è un indicatore biochimico precoce di danno renale acuto nei pazienti cardiochirurgici sottoposti a trapianto di rene. Un aumento della concentrazione di lipocalina-2 nelle urine si osserva in caso di insufficienza renale acuta, necrosi tubulare acuta o nefropatia tubulointerstiziale. Nell'insufficienza renale acuta, l'NGAL dal plasma sanguigno entra nei reni, viene filtrato e riassorbito nei tubuli prossimali. È stato chiaramente e ripetutamente dimostrato che quando i tubuli renali sono danneggiati, il livello di NGAL aumenta sia nel siero (7-16 volte) che nelle urine (25-1000 volte!). Nell’insufficienza renale acuta, le fonti di elevati livelli plasmatici di NGAL comprendono il fegato, i polmoni, i neutrofili, i macrofagi e altre cellule del sistema immunitario. Sembra che sebbene l'NGAL plasmatico venga liberamente filtrato dal glomerulo, venga in gran parte riassorbito nel tubulo prossimale per endocitosi. Qualsiasi escrezione di NGAL nelle urine si verifica solo quando è associata a un danno ai tubuli renali prossimali, che impedisce il riassorbimento di NGAL e/o ad un aumento della sintesi renale de novo di NGAL.
I livelli di NGAL sono diagnostici e prognostici nell'insufficienza renale acuta: aumentano rapidamente, 1-2 giorni prima della creatinina e riflettono la gravità e la gravità del danno renale. Tuttavia, i livelli di NGAL nel plasma, nel siero e nelle urine hanno un significato diagnostico e prognostico simile. Pertanto, è possibile utilizzare la determinazione di questo biomarcatore nelle urine e non prelevare il sangue dai neonati. Il livello limite più elevato di NGAL nelle urine dei bambini è pari a 100-135 ng/ml.
Molecola di danno renale KIM-1
KIM-1 (molecola di danno renale-1) è una glicoproteina coinvolta nell'interazione cellula-cellula. La sua concentrazione aumenta nelle parti prossimali del nefrone durante il danno renale acuto di varia origine. Non si trova nei reni di persone e animali sani, ma è molto abbondante nei reni affetti da vari processi patologici. La proteina è anche conosciuta come TIM-1 perché è espressa a bassi livelli da sottoinsiemi di cellule T attivate. KIM-1 viene attivata più fortemente rispetto ad altre proteine quando le cellule renali sono danneggiate ed è localizzata prevalentemente nella membrana apicale delle cellule epiteliali prossimali. È stato stabilito che dopo il danno al tessuto renale, KIM-1 inizia ad accumularsi attivamente nelle cellule epiteliali tubulari. Inoltre, questa sostanza agisce sulle cellule epiteliali che hanno mantenuto la loro vitalità e le trasforma in fagociti capaci di assorbire le cellule morte e le loro particelle. Tutto ciò accelera significativamente il processo di pulizia del tessuto renale dalle masse morte e aiuta a ripristinare la funzionalità renale. Pertanto, la sostanza KIM-1 formata durante il danno renale migliora significativamente la fagocitosi delle cellule morte e aumenta l'intensità dei processi di ripristino della struttura e della funzione del tessuto renale. Una volta danneggiati i tubuli renali, KIM-1 inizia ad essere escreto nelle urine. L’aumento dell’escrezione urinaria di KIM-1 è più specifico per il danno renale ischemico e non dipende da altri fattori dannosi. Le sue elevate concentrazioni predicono anche una prognosi sfavorevole dell’AKI. La concentrazione urinaria di KIM-1 è un fattore predittivo dell’esito del trattamento nei pazienti con danno renale acuto.
La citochina IL-18 (Interleuchina-18) appartiene alle citochine proinfiammatorie prodotte dall'epitelio tubulare prossimale dopo l'azione di fattori nefrotossici e viene rilasciata durante l'ischemia. La determinazione dell'IL-18 nelle urine consente di individuare precocemente i danni renali causati da ischemia o nefrotossine. Inoltre, è un indicatore della gravità dell’insufficienza renale acuta e dell’aumento del rischio di morte. IL-18 viene rilevata nelle urine di pazienti con insufficienza renale acuta di origine ischemica nelle fasi più precoci (4-6 ore, raggiungendo un picco a 12 ore) dopo l'esposizione ad un fattore dannoso. Oltre alla sua funzione diagnostica, l’IL-18 può avere valore prognostico riguardo alla durata dell’AKI e ai tempi di recupero della funzionalità renale. L’aumento delle concentrazioni di IL-18 nelle urine non è solo un indicatore di danno renale acuto, ma anche un predittore di mortalità nei pazienti critici. Il significato diagnostico è soggetto a ulteriori chiarimenti. Sulla base dei dati disponibili, IL-18 può avere una bassa sensibilità ma un’elevata specificità. O in altre parole, in molti pazienti con danno renale acuto, la concentrazione di IL-18 può rimanere entro il range normale relativo, mentre è più probabile che un aumento della concentrazione indichi un danno renale acuto.
Pertanto, l'introduzione di un nuovo concetto in nefrologia - danno renale acuto, consentirà la diagnosi precoce della disfunzione renale con una correzione tempestiva e la prevenzione del peggioramento dell'insufficienza renale. Gli indicatori tradizionali non sono sufficientemente specifici o sensibili per la diagnosi precoce del danno renale acuto. Mentre la terapia iniziata tempestivamente influisce sulla prognosi dei pazienti con danno renale acuto. Ciò è diventato la base per la ricerca di marcatori per la diagnosi precoce del danno renale acuto. Non ci sono conclusioni finali. Ma molti dei marcatori biochimici hanno un potenziale diagnostico piuttosto significativo. In ogni caso, questa è una delle aree attualmente in via di sviluppo per migliorare la terapia intensiva e la rianimazione dei pazienti critici con molte pubblicazioni rilevanti.
BIBLIOGRAFIA
1 Tomilina N.A., Podkorytnaya L.P. Insufficienza renale affilata//Nefrologia e dialisi. – 2009, n. 1. – P. 1-14.
2 Waikar S.S., Liu K.D., Chertow G.M. Diagnosi, epidemiologia e risultati di danno renale affilato//Clin. J Am Soc Nephrol. – 2008. – Vol.3. – P.844-61.
3 Bonventre J.V., Weinberg J.M. Recenti progressi nella fisiopatologia dell'insufficienza renale acuta ischemica // JASN. – 2003. – Vol. 14. – P. 2199–2210.
4 Gohonson R.J., Feehally J. Nefrologia clinica completa; Mosby – Edimburgo: 2003. – P. 200–201.
5 Clermont G., Acker C.G., Angus D.C., Sirio C.A., Pinsky M.R., Johnson J.P. Insufficienza renale nell'ICU: confronto dell'impatto d'insufficienza renale affilata e malattia renale di stadio terminale su risultati di ICU//KidneyInt. – 2002. – Vol. 62. – P. 986–996.
6 Goss C.H., Brower R.G., Hudson L.D., Rubenfeld G.D. Incidenza di danno polmonare acuto negli Stati Uniti. Rete ARDS//Crit Care Med. – 2003. – Vol. 31. – P.1607–1611.
7 Bellomo R., Ronco C., Kellum J.A. et al. Insufficienza renale acuta: definizione, misure di esito, modelli animali, fluidoterapia e esigenze informatiche: la seconda conferenza di consenso internazionale del gruppo Acute Dialysis Quality Initiative (ADQI) // Crit. Cura. – 2004. – V. 8. – R. 204–212.
8 Covic A., Covic M., Segall L., Gusbeth-Tatomir P., “Manual de Nephrologie”, capitolul Insuficienţă renală acută, Editura Polirom//Bios, Iaşi. – 2007. – R.260.
9 Uchino S., Bellomo R., Orafo D. et al., Una valutazione dei criteri RIFLE per insufficienza renale acuta in pazienti ospedalizzati//Crit Care Med. – 2006. –Vol. 34(7). – P.1913-1917.
10 Hoste EA, Clermont G, Kersten A, et al., I criteri RIFLE per il danno renale acuto sono associati alla mortalità ospedaliera nei pazienti critici: un'analisi di coorte // Crit Care. – 2006. – Vol.10(3). – P.73.
11 Cruz DN, Bolgan I, Perazella MAet al., Indagine sull'esito renale dell'ospedale prospettico italiano del Nord Est su danno renale acuto (NEiPHROS-AKI): affrontare il problema con i Criteri RIFLE//Clin J Am Soc Nephrol. – 2007. – Vol. 2(3). – P.418-25.
12 Mehta R.L., Kellum J.A., Shan S.V. et al. Acute Kidney Injury Network: rapporto di un'iniziativa per migliorare i risultati nella lesione renale acuta // Crit. Cura. – 2007. – V. 11. – Pag. 31.
13 Clarkson M.R., Fridewald J.J., Eustace J.A., et al. Danno renale acuto. In: Brenner BM, ed. Il rene, 8a edizione. Saunders Elseiver, Filadelfia a.e. – 2008. – P. 943-86.
14 Bagshaw S.M., George C., Bellomo R. Un confronto tra i criteri RIFLE e AKIN per il danno renale acuto in pazienti critici // Nephrol. Comporre. Trapianto. – 2008. – V. 23. – P. 1569–1574.
15 Bouman C., Kellum J.A., Lamiere N., Levin N. Definizione di danno renale acuto. Iniziativa per la qualità della dialisi acuta. 2a Conferenza Internazionale di Consenso, 2002.
16 Uchino S., Kellum J.A., Bellomo R. et al. Insufficienza renale affilata in pazienti critici: Uno studio multicentrico multinazionale//JAMA. – 2005. –Vol. 294. – P. 813–818.
17 Schneider J., Khemani R., Grushkin C. et al. La creatinina sierica stratificata nel punteggio RIFLE per il danno renale acuto è associata alla mortalità e alla durata della degenza dei bambini nell'unità di terapia intensiva pediatrica // Crit. Cura Med. – 2010. – Vol. 38(3). – P.933–939.
18 Fliser D., Laville M., Covic A., et al. Una dichiarazione di posizione sulle migliori pratiche renali europee (ERBP) sulle linee guida di pratica clinica per il miglioramento degli esiti globali della malattia renale (KDIGO) sulle lesioni renali acute: parte 1: definizioni, gestione conservativa e nefropatia indotta da mezzo di contrasto//Trapianto di Nephrol Dial. – 2012. –Vol. 0. – Pag. 1-10.
19 Snyder S., Pendergraph B. Scoperta e valutazione di malattia renale cronica//Am Fam Physician. – 2005. – V. 72. – P. 1723–1732.
20 Lassnigg A., Schmidlin D., Mouhieddine M. et al. Cambiamenti minimi nella creatinina sierica predicono la prognosi nei pazienti dopo un intervento chirurgico cardiotoracico: uno studio prospettico di coorte // J. Am. Soc. Nefrolo. – 2004. – V. 15. – P. 1597–1605.
Danno renale acuto (AKI)è un danno acuto, potenzialmente reversibile al parenchima renale di varie eziologie (cause) e patogenesi con o senza diminuzione della funzione escretoria dei reni. Il danno renale acuto è caratterizzato da un’improvvisa perdita della funzionalità renale. In precedenza, la malattia veniva chiamata “insufficienza renale acuta”.
Classificazione dell'AKI
Prima che i medici avessero il tempo di abituarsi alla classificazione RIFLE, adottata nel 2004 dal gruppo internazionale Acute Dialysis Quality Initiative (ADQI), ne è apparsa una nuova. Nel 2007, l’Acute Kidney Injury Collaborative (AKIN) ha migliorato i propri criteri per l’AKI. È stato inoltre proposto che qualsiasi paziente sottoposto a terapia sostitutiva renale sia classificato come stadio 3. Un'altra comunità internazionale molto rispettata, KDIGO (Clinical Practice Guideline for Acute Kidney Injury), ha modificato il testo.
|
Tabella 2. Sistema modificato per la diagnosi e la stratificazione della gravità dell'AKI (AKIN, 2007, KDIGO, 2012) |
||
|
Palcoscenico |
Siero di creatinina |
Volume di urina escreta |
|
1,5-1,9 volte superiore alla base o aumento di ≥0,3 mg/dL (≥26,5 µmol/L) |
<0,5 мл/кг/ч за 6-12 часов |
|
|
2,0-2,9 volte superiore alla base |
<0,5 мл/кг/ч за ≥12 часов |
|
|
3,0 volte superiore alla base o aumento a ≥4,0 mg/dl (≥353,6 µmol/l) o iniziare una terapia sostitutiva renale o nei pazienti< 18 лет, снижение скорости фильтрации креатинина до <35 мл/мин на 1,73 м2 |
<0,3 мл/кг/ч за ≥24 часа или anuria per ≥12 ore |
|
Diagnostica
Le seguenti attività dovranno essere completate nel più breve tempo possibile:
- Radiografia dei polmoni;
- Ecografia dei reni (può essere ritardata);
- Analisi generale del sangue, delle urine;
- Creatinina, urea nel sangue;
- Potassio, sodio nel sangue;
- Emogasanalisi e pH arterioso;
- Creatinina, urea urinaria;
- Sodio nelle urine.
Il prelievo di sangue e urina per i test deve essere effettuato contemporaneamente, prima della somministrazione di liquidi e diuretici. Non è consigliabile utilizzare l'urografia escretoria a fini diagnostici: quasi tutti i mezzi di contrasto radioattivo per via endovenosa presentano grave nefrotossicità.
Monitoraggio
- Monitoraggio dell'ECG;
- Contabilità dei liquidi ricevuti;
- Pulsossimetria;
- Monitorare la diuresi, preferibilmente ogni ora.
Attenzione! Quando viene rilevato un AKI, o anuria, si consiglia ai medici di assicurarsi che il catetere inserito nella vescica funzioni correttamente. Ciò è particolarmente importante quando la produzione di urina è inferiore a 100 ml/giorno (anuria), poiché i disturbi renali in rari casi iniziano con anuria (mancanza di produzione di urina).
Trattamento
Le prescrizioni farmacologiche dovrebbero essere ridotte il più possibile e tutti i farmaci nefrotossici dovrebbero essere sospesi. Non utilizzare integratori di potassio e magnesio, ACE inibitori, diuretici risparmiatori di potassio (spironolattone, triamterene), antibiotici nefrotossici (soprattutto aminoglicosidi), analgesici non steroidei, destrani, HES.
Se è ancora necessario utilizzare antibiotici, le loro dosi devono essere adattate di conseguenza. Viene determinato se il paziente presenta iperidratazione, iperkaliemia, edema polmonare, i principali fattori di rischio per la vita del paziente.
Fornire assistenza a un paziente con una minaccia immediata alla vita
Iperkaliemia(potassio > 5,5 mmol/l) - più comune con oligurico (diuresi< 500 мл/сут) и анурическом (диурез менее 50-100 мл/сут) варианте острого повреждения почек. Гиперкалиемия вызывает нарушения ритма сердца и может вызвать остановку сердца. К ЭКГ признакам гиперкалиемии (более 6,5 ммоль/л) относятся: высокий зубец Т, остроконечный, расширяется комплекс QRS. Может снижаться зубец R, иногда выявляются различные блокады сердца.
Livello di potassio nel sangue< 7 ммоль/л:
C. Pericardite (alto rischio di sanguinamento e/o tamponamento);
(indicazione alla dialisi d'urgenza);
D. Diatesi emorragica associata a disfunzione piastrinica uremica (un'indicazione di emergenza, anche se questa condizione può migliorare se l'ematocrito aumenta oltre il 30%).
2. Sovraccarico di liquidi refrattario o progressivo;
3.Iperkaliemia incontrollata;
4. Grave acidosi metabolica, soprattutto in pazienti con oliguria;
B. Declino graduale della funzionalità renale: azoto ureico nel sangue superiore a 25-36 mmol/l o clearance della creatinina inferiore a 15-20 ml/min.
Le indicazioni di emergenza per l'emodialisi comprendono gravi disturbi dei livelli di sodio nel sangue associati all'AKI:< 115 и >165 mmol/l.
Controindicazioni all'emodialisi
Emorragie cerebrali, sanguinamento gastrico e intestinale attivo, gravi disturbi emodinamici.
Azioni quando non esiste una minaccia immediata per la vita del paziente
Determinare la possibile causa e forma dell’AKI. Le cause più comuni di AKI sono:
Avvelenamento di varie eziologie, molto spesso surrogati dell'alcol;
Diabete;
Ipovolemia di qualsiasi eziologia (sanguinamento, vomito, diarrea, malattie chirurgiche degli organi addominali, ecc.);
Varie malattie cardiache (ipertensione arteriosa, insufficienza cardiaca);
Ipossia di qualsiasi origine;
Ipotensione prolungata di qualsiasi eziologia;
Iatrogenesi (uso di destrani, radiocontrasti per via endovenosa, antibiotici nefrotossici, ecc.).
Attenzione! L'anuria si osserva più spesso con ipotensione prolungata e completa ostruzione delle vie urinarie. Se tali cause non possono essere rilevate, ma è presente anuria, questa è spesso associata all'occlusione bilaterale delle arterie renali (ad esempio, dissezione) o alla necrosi dello strato corticale renale (avvelenamento).
È più facile sviluppare tattiche di trattamento se si divide l’AKI nelle forme prerenale, renale (parenchimale) e postrenale (ostruttiva).
AKI prerenale
L’AKI prerenale è un disturbo funzionale derivante da un ridotto apporto di sangue ai reni. È la causa più comune di AKI, rappresentando circa il 60% di tutti i casi.
Ragione principale:
- Ipotensione arteriosa;
- Diminuzione del BCC;
- Insufficienza epatica;
- (pesante);
- Uso di farmaci: bloccanti dei recettori dell'angiotensina, inibitori dell'enzima di conversione dell'angiotensina (ACEI), farmaci antinfiammatori non steroidei (FANS), ecc.
Indicatori di laboratorio
Una diminuzione del flusso sanguigno renale è accompagnata da un aumento del riassorbimento del sodio e da una diminuzione della sua escrezione nelle urine. Un contenuto di sodio nelle urine inferiore a 20 mmol/l con oliguria di solito indica una patologia prerenale. Esame del sedimento urinario: sono caratteristici cilindri ialini o granulari. Altri indicatori caratteristici di questa forma di AKI si riflettono nella tabella seguente.
Livelli di sodio nelle urine superiori a 40 mmol/l possono essere rilevati sia in caso di disturbi prerenali che in presenza dell'azione dei saluretici. Nei pazienti anziani si riscontrano spesso elevate concentrazioni di sodio nelle urine, anche se il flusso sanguigno renale è ridotto. Il sedimento urinario nell'AKI parenchimale contiene un gran numero di cellule epiteliali, cilindri epiteliali e granulari grossolani.
Trattamento
La cosa principale è mantenere attentamente l'equilibrio idrico ed elettrolitico. È necessario provare a convertire l’AKI oligurico in AKI non oligurico, per il quale si ricorre alla somministrazione di furosemide. Se non ci sono effetti, è importante utilizzare metodi di dialisi.
AKI postrenale (ostruttivo).
Il danno renale acuto talvolta (in circa il 5% dei casi) si verifica a causa dell'ostruzione del tratto urinario superiore o inferiore.
Ragione principale:
- Ostruzione degli ureteri (tumore, calcoli, compressione esterna degli ureteri);
- Ostruzione delle vie urinarie inferiori: vescica neurogena, adenoma prostatico, calcoli, carcinoma, stenosi uretrale.
Indicatori di laboratorio
Nell'AKI ostruttivo, il sedimento urinario può contenere leucociti e cilindri leucocitari. I globuli rossi e i cilindri di globuli rossi sono caratteristici della glomerulonefrite acuta, ma possono essere riscontrati anche in altri processi patologici che portano al danno renale acuto.
Trattamento dipende dalla causa dell'AKI e mira a eliminare l'ostruzione.
Varianti del decorso dell'AKI e prognosi
Il decorso del danno renale acuto può essere ciclico, ricorrente e irreversibile. Nella variante ciclica del decorso dell'AKI si distinguono:
- Lo stadio iniziale (primario): durante questo si verifica un danno ai reni. La durata di questo periodo dipende dalla causa e può variare ampiamente;
- Stadio oligurico o anurico: la sua durata va da 2-4 giorni a 2-3 settimane;
- La fase di ripristino della diuresi (poliurica) - da diversi giorni a 2-4 settimane.
Un decorso recidivante è tipico della malattia renale cronica ostruttiva (gotta, nefrolitiasi, papillite necrotizzante cronica). Una varietà di malattie che causano necrosi corticale o papillare totale (ipertensione maligna, ipotensione, avvelenamento, ecc.) Possono portare a un decorso irreversibile.
La prognosi è migliore per il danno renale acuto prerenale e postrenale rispetto al danno renale acuto. Il tasso di mortalità varia ampiamente, ma nell'AKI renale raggiunge il 50-70% nei politraumi, il 30-40% negli avvelenamenti.
Trattamento conservativo dei pazienti con AKI
Normalizzazione dell'emodinamica
Prima di tutto, è necessario normalizzare i parametri emodinamici che determinano il flusso sanguigno nei reni. Si consiglia di eliminare rapidamente l'ipovolemia e l'ipotensione arteriosa somministrando liquidi e (o, se necessario, vasopressori).
I medici determinano la quantità di liquido per l’infusione sulla base di una valutazione clinica del volume sanguigno. La sua diminuzione aggrava l’AKI deteriorando la perfusione renale. Il liquido viene somministrato in un volume corrispondente alle perdite nascoste (circa 500 ml al giorno nei pazienti con temperatura normale) più la quantità di liquido escreto nelle urine e in altri modi.
Nei pazienti con AKI non oligurico, una maggiore diuresi e un effetto più pronunciato dei diuretici rendono possibile un controllo meno rigoroso della quantità di liquidi somministrati e consumati, il che facilita la gestione di questi pazienti. Tuttavia, con AKI non oligurico, i pazienti possono perdere una quantità significativa di liquidi ed elettroliti nelle urine; per compensare tempestivamente queste perdite, il medico deve monitorare attentamente il volume del sangue e il contenuto di elettroliti nelle urine. il siero. Allo stesso tempo, viene effettuato il trattamento della malattia o condizione che ha causato l’AKI.
Stimolazione dei processi glomerulare-tubulari di formazione dell'urina
Stanno cercando di convertire la variante oligurica dell’AKI in una variante non oligurica. Per questi scopi usano. Attiva i processi tubulari di formazione dell'urina e riduce la contropressione. Non è consigliabile utilizzare il farmaco in dosi superiori a 600 mg/die.
Allo stesso tempo, dosi inferiori a 2 mg/kg spesso non portano al risultato desiderato. La soluzione più accettabile è la somministrazione endovenosa lenta di furosemide ad una dose iniziale di 1 mg/kg di peso corporeo del paziente, seguita successivamente da un’infusione a lungo termine. In questo caso, l'effetto diuretico si manifesta solitamente entro un'ora. È possibile assumere la furosemide per via orale, ma in tal caso il dosaggio del farmaco, rispetto alla somministrazione endovenosa, deve essere aumentato di 3-4 volte. In precedenza, piccole dosi di dopamina (1-3 mcg/kg/min) venivano utilizzate per eliminare la vasocostrizione associata all’AKI.
Ma negli ultimi anni questo farmaco si è dimostrato del tutto inefficace per il trattamento e la prevenzione dell’AKI. Ma se il paziente ha una grave insufficienza cardiaca e un danno renale acuto prerenale, questo farmaco può essere efficace nell’aumentare la produzione di urina. Ad oggi, non vi è alcuna evidenza che la somministrazione di antispastici (aminofillina, pentossifillina) possa migliorare gli esiti del trattamento nei pazienti con AKI.
Ipertensione arteriosa e suo trattamento
Innanzitutto bisogna evitare il sovraccarico di volume. Se la funzione di escrezione dell'azoto da parte dei reni è compromessa, viene prescritto un diuretico dell'ansa e (o) un bloccante dei canali del calcio.
I medici di solito usano furosemide (altri diuretici sono inefficaci nella stragrande maggioranza dei casi) in combinazione con antagonisti del calcio - verapamil, amlodipina (eccetto nifedipina corta). Puoi anche usare gli alfa-agonisti centrali: clonidina, metildopa.
Complicanze infettive
Le complicanze infettive si sviluppano frequentemente e rappresentano una delle principali cause di morte nell'AKI. Le manifestazioni più tipiche sono le infezioni del tratto urinario e la polmonite. A scopo preventivo è opportuno evitare, per quanto possibile, l'uso di cateteri (urinario, endovenoso, ecc.).
La scelta della terapia antibatterica dipende dalla natura della malattia infettiva. Per la terapia antibiotica iniziale vengono solitamente utilizzate le cefalosporine di 3a generazione. Cercano di escludere antibiotici con effetti nefrotossici (vancomicina, aminoglicosidi, cefalosporine di 1a generazione, ecc.). Se non viene eseguita l’emodialisi, i medici devono aggiustare la dose della maggior parte dei farmaci in base alla gravità del danno renale.
Sanguinamento gastrointestinale
Il sanguinamento gastrointestinale complica il decorso del danno renale acuto nel 15-30% dei pazienti. L'uremia porta a lesioni erosive delle mucose e compromissione della funzione piastrinica. Come in molte altre condizioni critiche, nell'AKI, a causa di disturbi emodinamici e ipossia, molte persone sviluppano danni da stress alla mucosa gastrointestinale. E prima di tutto: lo stomaco.
Per la prevenzione, è possibile utilizzare un inibitore della pompa protonica, ad esempio una flebo IV alla dose di 40 mg 2 volte. al giorno. In assenza di inibitori della pompa protonica vengono prescritti bloccanti dei recettori H2 dell'istamina: ranitidina 50 mg per via endovenosa ogni 6 ore o famotidina 20 mg per via endovenosa ogni 8 ore. Se le condizioni del paziente lo consentono, questi farmaci possono essere somministrati per via enterale. I bloccanti dei recettori H2 e, in misura minore, gli inibitori della pompa protonica, possono modificare lo stato mentale del paziente e causare trombocitopenia. Dovrebbero essere prescritti con estrema cautela ai pazienti con encefalopatia e trombocitopenia.
Anemia
L'anemia nell'AKI si verifica in casi frequenti. Di solito è causato dalla soppressione dell'ematopoiesi e dalla perdita di sangue. Per i sintomi caratteristici dell'anemia grave, diminuzione dei livelli di emoglobina< 70-80 г/л, назначается гемотрансфузия.
Uremia
Il tasso di mortalità diminuisce se l’urea può essere mantenuta al di sotto di 30 mmol/L. Una volta che il livello di urea nel sangue raggiunge questo livello, di solito viene iniziata la dialisi. L'uremia porta spesso a disturbi neurologici (ad esempio: crisi epilettiformi, sonnolenza, convulsioni cloniche, tremore sbattitore, polineurite), che servono come indicazione alla dialisi.
Pericardite uremica spesso si manifesta solo come uno sfregamento pericardico. L'unico modo per trattare questa complicanza è la dialisi e in questi casi si cerca di mantenere la dose di eparina al minimo.
Nutrire il paziente
Se il paziente non è sottoposto a emodialisi, l'apporto proteico è limitato a circa 0,5-1 g/kg/die, il che riduce la formazione di scorie azotate. Garantire il valore energetico del cibo si ottiene aumentando la quantità di grassi e carboidrati. Per evitare un aumento del catabolismo, il contenuto calorico totale del cibo dovrebbe essere di 35-40 kcal/kg al giorno.
Con un'elevata intensità dei processi catabolici o nei pazienti malnutriti viene prescritta una dieta con un contenuto proteico più elevato e la dialisi inizia anticipatamente. Limitare il sale da cucina nella dieta a 2-4 g/giorno aiuta a ridurre la ritenzione di liquidi. L'assunzione di potassio non deve essere superiore a 40 mmol/giorno. Dovrebbero essere evitati cibi e farmaci contenenti magnesio.
Gestione dei pazienti con AKI nella fase di ripristino della diuresi
È necessario un attento monitoraggio degli elettroliti nel sangue, del bcc, della diuresi e la contabilizzazione delle perdite di elettroliti nelle urine. Se soffri di poliuria, non dovresti limitare l'assunzione di liquidi. Se possibile, dovrebbero essere evitati i farmaci nefrotossici. Una volta ripristinata la diuresi, la funzione renale migliora gradualmente, da alcune settimane a 2-4 mesi.
Danno renale acuto (AKI)- una sindrome che si sviluppa a seguito di una rapida diminuzione (da ore a giorni) della velocità di filtrazione glomerulare, che porta all'accumulo di prodotti metabolici azotati (urea, creatinina) e non azotati (con disturbo degli elettroliti, dell'equilibrio acido-base, volume del liquido) escreto dai reni.
AKI– un problema multidisciplinare, poiché le sue cause sono molteplici e possono essere riscontrate nella pratica di qualsiasi medico. Molto spesso si sviluppa in condizioni critiche nelle unità di terapia intensiva (ICU) ed è un fattore indipendente di morte. Di particolare preoccupazione è la crescente mortalità dovuta all’AKI, nonostante i significativi progressi nella scienza e nella pratica medica, che è rimasta praticamente invariata negli ultimi tre decenni. Tassi di mortalità particolarmente elevati (fino al 50-70%) si osservano tra i pazienti che necessitano di terapia sostitutiva renale ().
Pertanto, era necessario sviluppare metodi oggettivi per determinare le fasi dello sviluppo dell’AKI per la valutazione precoce dei fattori di rischio. La proposta di un nuovo termine per AKI in sostituzione del noto termine “insufficienza renale acuta (AKI)” è stata preceduta dal lavoro dei gruppi ad hoc ADQI (Acute Dialysis Qualite Initiative) e poi AKIN (Acute Kidney Injury Network). Lo studio è stato avviato nel 2000 dall’American Society of Nephrology e dalla Society of Critical Care Medicine. Il nuovo concetto di AKI considera il problema dell’insufficienza renale acuta in modo più ampio, partendo dallo stadio di rischio, l’inizio del danno renale, quando la possibilità di reversibilità del processo è molto più elevata rispetto allo sviluppo dello stadio di insufficienza, che spesso richiede il trasferimento a.
CLASSIFICAZIONE DEL DANNO RENALE ACUTO
Nel 2004, l’ADQI ha proposto il concetto di “danno renale acuto” (AKI), che ha sostituito il termine “insufficienza renale acuta” e una classificazione chiamata RIFLE secondo le prime lettere di ciascuna delle fasi identificate in sequenza dell’AKI: rischio, lesione, insufficienza (Failure), perdita (Loss), malattia renale allo stadio terminale (End stage renal Disease). È stato dimostrato che i criteri per diagnosticare l'AKI sono due semplici criteri: creatinina e diuresi.
Creatinina sierica nel sangue* - creatinina sierica, CF** - filtrazione glomerulare
Viene proposta una nuova definizione di AKI non solo per il nefrologo e l'intensivista, ma anche per i medici che riscontrano AKI non quotidianamente. Gli aspetti positivi della nuova classificazione dipenderanno da quanto questi medici conosceranno i criteri per l’AKI. I criteri per l'AKI avvisano il medico di un possibile AKI e aiutano a diagnosticarlo in modo tempestivo, inclusa la sua variante non oligurica. Lo sviluppo dell'AKI può verificarsi entro 1-7 giorni e il livello di creatinina può aumentare di 1,5 volte o più. Dalla classificazione consegue che la disfunzione renale, esistente anche da più di un mese, può essere considerata “acuta”. La scala RIFLE consente di determinare la linea temporale tra AKI e CKD. L'AKI è presente da meno di 3 mesi. Gli studi condotti sui bambini poco dopo hanno mostrato quasi lo stesso valore dei criteri selezionati per l’AKI durante l’infanzia.
Il gruppo di ricerca AKIN ha fatto un'aggiunta, data la possibilità di un rapido (entro meno di 48 ore) declino della funzionalità renale, e ha proposto come linea guida un aumento assoluto della creatinina durante questo periodo di ≥ 26,5 μmol/L.
Pertanto, secondo le Linee guida di pratica clinica KDIGO per l’AKI, pubblicate nel marzo 2012, l’AKI è definito come:
Aumento di Red.syv. di ≥0,3 mg/dL (≥26,5 µmol/L) entro 48 ore; O
Aumento di Red.syv. fino a ≥ 1,5 volte il basale (se noto o sospettato che si sia verificato nei 7 giorni precedenti); o volume delle urine<0,5 мл/кг/час за 6 часов
Va ricordato che l’AKI può svilupparsi in un contesto di insufficienza renale cronica preesistente. Pertanto, secondo le Linee guida pratiche KDIGO (2012), i pazienti con AKI dovrebbero essere monitorati per 3 mesi per valutare il grado di recupero della funzionalità renale, episodi ricorrenti di AKI o peggioramento della CKD preesistente.
· Se un paziente è affetto da insufficienza renale cronica, il trattamento deve essere conforme alle linee guida pratiche K/DOQI per la gestione dell'insufficienza renale cronica.
· Se un paziente non soffre di insufficienza renale cronica, è necessario tenere presente che il paziente ha un rischio maggiore di sviluppare insufficienza renale cronica e deve essere gestito in conformità con le linee guida pratiche KDOQI.
I pazienti a rischio di sviluppare AKI devono essere attentamente monitorati per la pressione arteriosa. e il volume delle urine. La loro gestione dipende da fattori predisponenti. I pazienti dovrebbero essere valutati innanzitutto per identificare le cause reversibili dell'AKI in modo che questi fattori (p. es., postrenali) possano essere affrontati tempestivamente.
Tenendo conto del lavoro di due gruppi (ADQI e AKIN), si raccomanda la stratificazione degli stadi AKI secondo KDIGO secondo i seguenti criteri:

Fasi Creatinina plasmatica Volume di urina escreta
1 1,5-1,9 volte superiore al basale o un aumento di 0,3 mg/dL (≥26,5 µmol/L).<0,5 мл/кг/час за 6-12 часов
2 2,0-2,9 volte superiore all'originale.<0,5 мл/кг/час за ≥12 часов
3 3,0 volte il basale o aumento a ≥4,0 mg/dl (≥353,6 µmol/l) o all'esordio o nei pazienti<18 лет, снижение расчетной СКФ до <35 мл/мин/1,73м2. <0,3 мл/кг/час за ≥24 часа или анурия в течение ≥12 часов
CAUSE E CLASSIFICAZIONE DEL DANNO RENALE ACUTO
Secondo il principale meccanismo di sviluppo, l'AKI è diviso in 3 gruppi: prerenale, renale e postrenale. Molte ragioni possono portare al loro sviluppo.
Cause prerenali
Le cause prerenali rappresentano la maggior parte dei casi di AKI. Costituiscono la parte predominante (50-60%) dell’AKI. Lo spettro delle cause dell’AKI nei paesi sviluppati è cambiato negli ultimi decenni a causa dell’introduzione di nuove misure diagnostiche e terapeutiche (il cosiddetto AKI “acquisito in ospedale”). La percentuale di casi di AKI grave che necessitano di terapia dialitica è aumentata negli ultimi 30 anni. L’AKI prerenale può verificarsi in pazienti con ipovolemia (diminuzione del volume sanguigno circolante) o normoipervolemia (riempimento insufficiente delle arterie).
Una vera diminuzione del volume del sangue o ipovolemia si sviluppa a causa di sanguinamento, vomito, diarrea, ustioni, aumento della diuresi dopo diuretici, diuresi osmotica (glicosuria), nonché condizioni con ridistribuzione dei volumi di liquidi corporei (sequestro di liquido extracellulare o perdita nell'organismo). il “terzo spazio”) che si verificano quando si manifestano peritoniti, pancreatiti, sindromi nefrosiche e altri casi con grave ipoalbuminemia, sindrome da risposta infiammatoria sistemica.
Il riempimento arterioso insufficiente è una condizione in cui il volume del sangue è normale o addirittura aumentato, ma i fattori circolatori non sono in grado di mantenere un'adeguata perfusione dei reni. Questa variante di AKI prerenale si sviluppa secondariamente in pazienti con cardiopatia con ridotta gittata cardiaca.
La vasodilatazione periferica durante sepsi, insufficienza epatica, shock anafilattico e dovuta all'azione di farmaci antipertensivi e anestetici può anche portare ad azotemia prerenale. Una forma specifica di AKI prerenale, la sindrome epatorenale (HRS), si sviluppa in pazienti con grave insufficienza epatica. Ci sono 2 tipi. La HRS di tipo 1 è la più grave, si sviluppa rapidamente e senza trapianto di fegato, la mortalità entro 3 mesi è del 90% (R. Schreyer, 2009). La HRS di tipo 2 si sviluppa in pazienti con ascite refrattaria e progredisce lentamente.
Nei disturbi emodinamici intrarenali che si sviluppano in seguito all'assunzione di vari farmaci, l'AKI prerenale si verifica a causa di due effetti: costrizione delle arteriole afferenti (effetto preglomerulare) o dilatazione delle arteriole efferenti (effetto post-glomerulare).
Nell’AKI prerenale, la ridotta velocità di filtrazione glomerulare non è accompagnata da danno strutturale o cellulare ai reni. L’AKI prerenale è reversibile quando le condizioni che hanno portato all’ipoperfusione renale si risolvono.
Danno renale acuto
Il danno renale acuto si sviluppa sullo sfondo di disturbi all'interno del rene stesso. Le cause dell’AKI renale possono essere patologie vascolari, glomerulari, interstiziali o tubulari e possono anche essere secondarie a malattie sistemiche. Il decorso dell'AKI in questi casi non dipende da fattori extrarenali (ad esempio, correzione dell'ipovolemia, eliminazione dell'ostruzione, ecc.).
Cause vascolari
Le lesioni dei vasi di grandi e medie dimensioni includono:
Occlusione delle arterie renali (trombosi, embolia, compressione durante l'intervento chirurgico);
Assunzione di ACE inibitori in presenza di malattie renovascolari a 2 code;
Emboli di colesterolo;
Trombosi della vena renale;
Periarterite nodosa.
Malattie che coinvolgono i piccoli vasi:
Microangiopatia trombotica (TMA) sotto forma di sindrome emolitico-uremica (SEU) o trombotica (TTP);
Malattia ateroembolica;
Crisi renale nella sclerodermia;
Ipertensione maligna;
TMA nelle donne in gravidanza (sindrome SEU, TTP e HELLP - emolisi, aumento dell'attività degli enzimi epatici, bassi livelli piastrinici).
Le cause glomerulari o malattie glomerulari sono numerose. Spesso l’AKI può svilupparsi all’esordio della glomerulonefrite. L'azotemia, osservata come parte della sindrome nefritica in pazienti con nefrite postinfettiva acuta (APIGN), scompare rapidamente. Ma in alcuni casi, con APIGN, così come con altri GN primari e secondari (lupus, IgA-GN, vasculite sistemica, sindrome di Goodpasture, ecc.), si sviluppa una GN rapidamente progressiva con la formazione di semilune nei glomeruli e un rapido aumento nei livelli di creatinina.
Cause interstiziali.
La lesione acuta è accompagnata da nefrite interstiziale acuta o nefrite tubulointerstiziale acuta (ATIN). L'ATIN si sviluppa spesso in un contesto di ipersensibilità ai farmaci e può anche essere una conseguenza di malattie infettive (capitolo 13).
Più di 100 farmaci possono causare ATIN. I più comuni: antibiotici, diuretici, FANS, anticonvulsivanti, allopurinolo. Le infezioni che causano ATIN sono batteriche (stafilococchi, streptococchi), virali (citomegalovirus, virus Epstein-Barr).
Cause tubulari.
Un'improvvisa diminuzione della GFR può essere dovuta a un danno tubulare prossimale dovuto a 2 cause: ischemia o esposizione a nefrotossine. Per molto tempo questo tipo di AKI è stato denominato “necrosi tubulare acuta ()”. In questo caso, i cambiamenti istologici sotto forma di necrosi possono essere insignificanti e possono predominare edema, vacuolizzazione, perdita dell'orletto a spazzola, ecc.
Il “supporto renale” utilizzando i metodi RRT consente di: fornire un’alimentazione adeguata, rimuovere i liquidi nell’insufficienza cardiaca congestizia e mantenere un adeguato equilibrio dei liquidi in un paziente con insufficienza multiorgano.
I principi di base della terapia dialitica sono descritti più dettagliatamente nel capitolo 19. Allo stadio attuale di sviluppo, le unità di terapia intensiva dovrebbero essere dotate di attrezzature per il trattamento dell'AKI e i medici dovrebbero essere formati sui metodi.
Esistono due tipi di dialisi: metodi di RRT intermittente (HD intermittente, IHD) e continua (CRRT). Con la RRT intermittente, la rimozione delle tossine uremiche si basa sulla diffusione. Le tossine del sangue passano nel dializzato ultrapuro, i capillari del dializzatore agiscono come una membrana semipermeabile. La rimozione del liquido si basa sull'ultrafiltrazione, che provoca anche una convezione parziale. Con i metodi di RRT continua (emofiltrazione, emodiafiltrazione), al contrario, la base della dialisi è la convezione.
La HD intermittente (IGD) è la stessa forma di dialisi utilizzata per la malattia renale allo stadio terminale. L'IHD viene eseguita in pazienti con AKI con emodinamica stabile, per 4 ore ogni giorno o a giorni alterni. L’IHD è il metodo di scelta per il trattamento dei pazienti ambulatoriali ed emodinamicamente stabili.
I pazienti con AKI in terapia intensiva vengono sottoposti a emodialisi convettiva standard 3-4 volte a settimana per ottenere l'eliminazione della sostanza come nei pazienti con insufficienza renale allo stadio terminale (Kt/V-1,4). Tuttavia, studi recenti dimostrano che sedute giornaliere di emodialisi migliorano la sopravvivenza dei pazienti e riducono i tempi di convalescenza renale.
L'ipotensione può rappresentare un grave problema nei pazienti estremamente malati con concomitante sepsi, ipoalbuminemia, malnutrizione proteico-energetica o grandi perdite di liquidi nel terzo spazio. Quando si gestisce l'ipotensione sindalitica, sono necessari un attento monitoraggio del volume sanguigno (se necessario, monitoraggio invasivo della pressione arteriosa e della pressione venosa centrale), la prescrizione di volumi di ultrafiltrazione realisticamente ottenibili e il monitoraggio continuo della pressione arteriosa durante la dialisi. Se si sviluppa ipotensione, la procedura di filtrazione deve essere immediatamente interrotta, il paziente deve essere posto nella posizione di Trendelenburg e deve essere somministrato un bolo di 250-500 ml di NaCl allo 0,9%.
La dialisi lenta e a bassa efficacia (SLED) è stata sviluppata come un ibrido tra procedure continue e intermittenti. La velocità del flusso sanguigno è di 100-200 ml/min, il flusso del dializzato è di 200-300 ml/min, la durata è di 8-12 ore.Questa emodialisi più lenta, teoricamente, mantiene più costantemente l'emodinamica e migliora la clearance delle sostanze solubili, rispetto all'emodialisi intermittente. emodialisi. La MNGD consente di ottenere lo stesso controllo dell'equilibrio idrico del paziente senza fluttuazioni emodinamiche in un periodo di tempo più breve (6-8 ore - a differenza della CRRT 16-24 ore). MNGD consente anche di fare una pausa tra una seduta e l'altra, necessaria per l'esecuzione di misure diagnostiche e di altro tipo per il paziente.
La durata e la frequenza della procedura per l'AKI dovrebbero superare significativamente quelle delle malattie croniche (per l'insufficienza renale cronica allo stadio terminale, di solito 4 ore 3 volte a settimana), poiché l'AKI è accompagnato da uno stato ipercatabolico e tutti i cateteri temporanei hanno un'elevata tasso di ricircolo. Secondo le raccomandazioni di KDIGO (2012), si dovrebbe
utilizzare la RRT intermittente ed estesa come metodi complementari nei pazienti con AKI.
Metodi continuativi di terapia sostitutiva renale
La terapia sostitutiva renale continua ha il vantaggio di monitorare meglio lo stato dei liquidi e degli elettroliti dei pazienti, ma la CRRT è più costosa dell'HDI. Le attuali indicazioni per la CRRT per l'AKI comprendono instabilità emodinamica, edema cerebrale, stato ipercatabolico e grave sovraccarico di liquidi.
Attualmente vengono utilizzati 4 tipi di CRRT: ultrafiltrazione lenta continua (SCUF), emofiltrazione venovenosa continua (CVHF), HD venovenosa continua (CVHD) ed emodiafiltrazione venovenosa continua (CVHF).
Grazie alle moderne funzionalità per il posizionamento sicuro di cateteri a doppio lume, la CRRT si è evoluta in procedure venovenose continue senza coinvolgere l'accesso arterioso. La pompa renale artificiale fornisce un flusso sanguigno costante e il morsetto sulla linea di ritorno crea una pressione idrostatica per fornire l'ultrafiltrazione.
Anche l’emofiltrazione veno-venosa continua (CVVHF) è costituita da componenti MNUF, ma in aggiunta il fluido sostitutivo viene fornito direttamente al circuito sanguigno extracorporeo del paziente. Come nel caso dell'MNUF, durante la convezione si forma un ultrafiltrato, ma a causa del grande volume del fluido di ricambio, il livello di ultrafiltrazione è molto più elevato. Il miglioramento dello stato dei liquidi e del metabolismo si ottiene aggiungendo liquidi sostitutivi al circuito extracorporeo. Il fluido sostitutivo può essere aggiunto alla linea prima e dopo il dializzatore. Quando si collega il liquido sostitutivo al dializzatore, l'emodiluizione riduce il rischio di trombosi all'interno del dializzatore, ma l'efficienza di eliminazione è ridotta del 15%.
Dialisi peritoneale.
Nei paesi in via di sviluppo, negli adulti e soprattutto nei bambini, un trattamento frequentemente utilizzato per i pazienti con AKI è la dialisi peritoneale, che si riferisce ad un metodo intracorporeo continuo di sostituzione della funzione renale.
Il principio della dialisi peritoneale si basa sulla diffusione, convezione e ultrafiltrazione. I meccanismi principali sono la convezione e l'ultrafiltrazione, come nel caso dei metodi continuativi di terapia sostitutiva renale. Il ruolo della membrana semipermeabile in questo caso è svolto dalla parete dei capillari del peritoneo parietale. L'ultrafiltrazione avviene grazie a
soluzione ipertonica (glucosio), che viene iniettata nella cavità addominale attraverso uno speciale catetere.
I vantaggi del Pd
Non è necessaria la presenza di un nefrologo specializzato o di un dialista (i pazienti con AKI sono ricoverati in terapia intensiva; gli scambi possono essere effettuati da infermieri sotto la supervisione di un intensivista esperto);
Tecnicamente, il posizionamento di un catetere peritoneale è più semplice (negli adulti) rispetto al posizionamento di un catetere vascolare e non è necessaria l'anticoagulazione sistemica;
Nessun cambiamento improvviso nell'emodinamica;
Rimozione più fisiologica dei liquidi e delle scorie azotate (24 ore/giorno rispetto all'HD intermittente 3-4 ore);
Il glucosio nel dializzato fornisce calorie aggiuntive per soddisfare il fabbisogno energetico;
Praticamente l’unico metodo di RRT disponibile per i bambini di peso inferiore a 10 kg nella Repubblica del Kazakistan (non esistono linee specifiche e dializzatori ultra-piccoli).
Gli svantaggi della malattia di Parkinson comprendono il rischio di infezione, la correzione relativamente lenta dell'uremia e dell'iperkaliemia, le difficoltà associate al catetere e altri.
>40:1 o più, raro
www.eurolab.ua
Danno renale acuto (AKI) nei bambini e negli adulti: cause, sintomi, diagnosi, trattamento
una malattia in rapido sviluppo che porta a danni al parenchima renale di varia patogenesi con e senza disturbi della funzione escretoria. Infatti, il termine AKI ha sostituito il termine insufficienza renale acuta.
Danno renale acuto
Il danno d'organo acuto è caratterizzato da un decorso rapido, ma presenta sintomi non specifici. Spesso la malattia viene diagnosticata troppo tardi e si verificano errori durante la diagnosi. Tutto ciò porta ad un aumento della mortalità.
La necessità di sostituire il concetto di insufficienza renale acuta è sorta a causa di diversi fattori. In primo luogo, è necessaria una definizione precisa e unificazione dei criteri diagnostici. Nella letteratura inglese, ad esempio, esistono 30 definizioni di insufficienza renale acuta.
In secondo luogo, i dati accumulati ci permettono di concludere che anche un aumento temporaneo relativamente piccolo della creatinina plasmatica porta ad un aumento della mortalità, sia nel periodo iniziale che a lungo termine. E la causa della morte non è sempre l’insufficienza renale. Ciò significa che in alcuni casi si formano complesse relazioni patogenetiche che portano a danni non solo al tessuto renale, ma anche ad altri organi.
Di conseguenza, l’AKI oggi si riferisce ad una sindrome di declino acuto della funzione renale associata al rischio di mortalità precoce o a lungo termine. Spesso porta alla formazione di insufficienza renale cronica. Il gruppo di lavoro di esperti dell'AKIN, incaricato di sviluppare il problema, ha proposto di classificare il livello di gravità della malattia in base alla concentrazione di creatinina nel plasma sanguigno e al volume delle urine. La clearance della creatinina è stata esclusa come fattore determinante. Pertanto, la diagnosi della malattia è stata ridotta a due semplici metodi che possono essere eseguiti in qualsiasi ospedale.
L'AKI è una diminuzione della funzionalità renale in cui entro 48 ore si verifica un aumento della concentrazione di creatinina di 0,3 mg/dl o più, o un aumento relativo del 50% o più, o una diminuzione della produzione di urina a 0,5 ml/kg/ora per più di 6 ore con un adeguato apporto di liquidi.
Il modello concettuale dell’AKI comprende 5 fasi. La norma non è inclusa nella scala.
- Rischio – caratterizzato da un aumento della concentrazione di creatinina di 1,5–2 r. rispetto al basale o superiore a 0,3 mg/dl. La diuresi è un volume di urina inferiore a 0,5 ml/kg/6 ore. Non ci sono marcatori funzionali, ma gli esami possono rivelare danni.
- Danno – la concentrazione di creatina aumenta di 2-3 volte, la diuresi – meno di 0,5 ml/kg/ in 12 ore. Sono presenti indicatori funzionali e di danno deboli.
- Insufficienza - la concentrazione aumenta 3 volte o più di 4 mg/dl. Con un aumento acuto, aumenta di oltre 0,5 mg/dl. Viene escreto meno di 0,5 ml/kg di urina al giorno oppure si osserva anuria per 12 ore. I biomarcatori indicano danni ai tessuti e i cambiamenti in queste fasi sono potenzialmente reversibili.
- Perdita: insufficienza renale osservata per 4 settimane senza cambiamenti.
- Lo stadio finale è fisso se l'insufficienza renale dura più di 3 mesi senza cambiamenti.
Il danno renale acuto è comune anche nei bambini. La situazione in quest'area è ancora peggiore, poiché non esiste un test diagnostico sufficientemente affidabile per determinare il disturbo. Oggi questa è la determinazione della concentrazione di lipocalina nel sangue, cistatina C sierica, NGAL, una proteina che viene normalmente filtrata nei glomeruli e viene completamente assorbita nei tubuli. Anche l’interleuchina-18 nelle urine e la KIM-1, una molecola che danneggia i reni, possono fungere da marcatori.
La gravità della malattia nei bambini è classificata in base alla velocità di filtrazione glomerulare - clearance della creatina e al volume di urina escreta:
- Il rischio è una riduzione del 25% della filtrazione. La diuresi è inferiore a 0,5 ml/kg/8 ore.
- Danno – Diminuzione del GFR del 50%, meno di 0,5 ml/kg di urina vengono escreti in 16 ore.
- Fallimento - GFR diminuisce del 75% - meno di 35 ml/min 1,73 mq. m, diuresi - meno di 0,3 ml/kg al giorno o anuria per 12 ore.
- La perdita di funzionalità si osserva quando la condizione renale rimane invariata per più di 4 settimane.
- Stadio terminale: la disfunzione rimane invariata per 3 mesi.
L’AKI è una complicanza molto seria. Secondo le statistiche, il tasso di mortalità tra i bambini con diagnosi di AKI è 12 volte più alto. Le statistiche relative ai pazienti adulti sono incomplete e distorte a causa dell'interpretazione ambigua della malattia. Nel complesso, i pazienti adulti con AKI hanno un tasso di mortalità più elevato del 25% rispetto a quelli senza AKI.
Eziologia
Esistono 3 forme di danno renale acuto: prerenale – incidenza del 50–60%, renale – 35–40% e postrenale – inferiore al 5%. La divisione ha senso, poiché ciascuna categoria ha il proprio meccanismo fisiopatologico e, quindi, caratteristiche di trattamento.
Per i bambini il quadro è leggermente diverso. L’AKI prerenale è osservato nell’85% dei casi, l’AKI renale nel 12%, l’AKI postrenale nel 3%.
Forme di danno renale acuto
AKI prerenale
Questa forma di AKI è la più comune e, di fatto, è la risposta funzionale dell'organismo all'insufficiente apporto di sangue ai reni. Di norma, la malattia non è accompagnata da un disturbo strutturale del tessuto renale. Di conseguenza, quando viene ripristinato il normale afflusso di sangue, anche la funzione renale viene ripristinata rapidamente.
Se la malattia si sviluppa in un contesto di carenza grave o prolungata, può provocare necrosi tubulare acuta. AKI e ATN possono essere considerati come stadi dello sviluppo dell’insufficienza renale. Molti pazienti presentano segni di entrambe le forme.
L’AKI può essere causato da qualsiasi malattia che causi un mancato afflusso di sangue ai reni.
Molto spesso ciò si verifica a causa di una diminuzione del volume del sangue arterioso. La sua carenza attiva il sistema renina-angiotensina-aldosterone. Un aumento della concentrazione di angiotensina II porta infine alla vasocostrizione, a seguito della quale la velocità di filtrazione glomerulare non diminuisce. Tuttavia, in un paziente con AKI, questo meccanismo non è più in grado di compensare la mancanza di sangue e la GFR inizia a diminuire.
La causa di una diminuzione del volume del sangue arterioso può essere l'infarto miocardico, pericardico, valvolare, ipertensione polmonare, vasodilatazione sistemica, ipercalcemia e altre malattie. I medicinali possono anche causare problemi alla funzionalità renale.
Nei bambini, la causa principale della malattia è l'ipossia, l'ipotermia, i difetti cardiaci congeniti e vascolari.
Meccanismo di sviluppo dell’AKI prerenale 
AKI renale
La causa dell'AKI renale è il danno al parenchima renale, cioè la malattia è stata preceduta da un qualche tipo di danno renale. Di conseguenza, l'eliminazione dei fattori esistenti - insufficiente apporto di sangue - non porta sempre alla guarigione.
Le cause del danno renale acuto sono le seguenti malattie:
- Necrosi tubulare acuta - molto spesso è causata da un processo ischemico e nefrotico causato da ipotensione, sepsi e altri. È la causa più comune di AKI e ha la prognosi peggiore, poiché è accompagnata da gravi comorbilità. I medici considerano l'ATN come un ulteriore fattore di rischio, poiché la necrosi porta alla morte del paziente nel 50-70%. Dopo la guarigione, la funzione renale viene ripristinata, anche se non completamente, poiché alcuni nefroni sono morti durante la malattia.
- Necrosi tubulare acuta ischemica - è di origine ischemica, cioè è causata anche da un insufficiente apporto di sangue. Nella prima fase, le cellule tubulari sono danneggiate, il che è associato a vasocostrizione e mancanza di sangue. Nel secondo si svolge un processo infiammatorio, non più dipendente dall'azione del fattore ischemico. Il ripristino funzionale è possibile allo stadio 3.
L'ATN ischemica è spesso causata da insufficienza cardiaca. Il diabete mellito, l'insufficienza renale cronica e la chirurgia cardiaca aumentano significativamente il rischio della sua insorgenza.
ATN nefrotossica - può essere causata sia da tossine endogene - farmaci antitumorali, diuretici, antibiotici, sia da infezioni endogene, virus. L'eliminazione del fattore attivo migliora immediatamente la funzionalità renale.
La causa della malattia nei bambini è spesso associata a difetti congeniti: malattia del rene policistico, ipoplasia e anomalie infiammatorie e vascolari. Una caratteristica molto pericolosa del decorso della malattia nei bambini è il passaggio dalla forma prerenale alla forma renale: se entro una settimana il fattore che agisce sui reni non può essere eliminato, allora stiamo parlando di danno organico al rene.
Cause di AKI renale 
AKI postrenale
Questa forma è provocata dall'ostruzione del sistema urinario, cioè dalla difficoltà nella produzione di urina a livello dell'uretra, della vescica, dei reni e degli ureteri. Con l'ostruzione unilaterale, soprattutto a livello dei reni, l'AKI, di regola, non si sviluppa.
Nell’AKI bilaterale, può verificarsi con ostruzione parziale o completa. Nel primo caso si registrano nicturia, minzione frequente, falsi impulsi, nel secondo - anuria.
Le cause dello sviluppo della forma postrenale sono coaguli di sangue, calcoli nella vescica, necrosi papillare, nefrolitiasi e così via.
La causa della malattia nei bambini è anche l'ostruzione bilaterale delle vie urinarie. In tenera età, la forma postrenale rappresenta l'1%. Video sulle cause e i sintomi della lesione renale acuta:
Diuresi
Un segno molto indicativo di malattia renale è la diuresi: il volume di urina escreta al giorno, all'ora, al minuto. In una persona sana, il volume normale di urina è un volume pari al 75% del liquido consumato. Deviazioni in una direzione o nell'altra indicano disfunzione dei reni o delle vie urinarie.
Nell’AKI renale, la diuresi normale viene spesso mantenuta nelle fasi iniziali, il che rende così importanti gli esami delle urine e del sangue.
Nelle lesioni acute si considerano 3 fasi della diuresi:
- Il periodo prodromico è il periodo compreso tra il periodo di incubazione e la malattia stessa. Molto spesso si osserva una diuresi normale. La durata del periodo prodromico dipende dalla causa della malattia, dalla tossicità della tossina e così via.
- Fase oligourica: dura in media 10-14 giorni, ma può durare fino a 8 settimane. Diuresi – 50–400 ml/giorno. La fase oligourica può non verificarsi: in questo caso la mortalità è molto più bassa e la prognosi per la guarigione è molto più favorevole.
- Postoligurico – ripristino della normale diuresi. In questo caso, la concentrazione di creatinina nel plasma e il livello di urea possono rimanere elevati per qualche tempo. Possibile disfunzione dei tubuli renali, poliuria, acidosi ipercoleremica.
Sintomi e segni
L'AKI non è tanto una malattia indipendente quanto uno stadio della stessa o un fattore ad azione secondaria che aumenta il rischio di morte. Il quadro clinico della malattia non è specifico e coincide con i segni della malattia di base o dell'avvelenamento. Se la causa dell'AKI è la sepsi, i suoi sintomi si osservano nel paziente. Se la causa è l'avvelenamento, i sintomi saranno caratteristici dell'avvelenamento con una determinata sostanza. Rilevare l’AKI, soprattutto in fase precoce, è possibile solo con il monitoraggio costante del livello di creatinina e urea nel sangue:
- Segnali specifici si osservano nella fase classificata come cedimento. Questi sintomi sono comuni nell'azotemia: nausea, vomito, gonfiore del grasso sottocutaneo. È possibile sviluppare ipervolemia: un aumento del volume del sangue, accompagnato da sintomi di insufficienza cardiaca. Nei casi più gravi si sviluppa edema polmonare.
- L’iperkaliemia è una complicanza comune dell’AKI e si verifica senza segni esterni. La sua influenza viene spesso rilevata già nella fase di tachicardia o insufficienza cardiaca.
- L'iponatriemia si esprime più chiaramente: il sistema nervoso centrale è interessato, compaiono crampi muscolari e tremori e compaiono disturbi gastrointestinali.
La presenza della malattia può essere determinata con precisione solo mediante metodi diagnostici. Inoltre, a causa della coincidenza di molti segni con i sintomi dell'insufficienza renale cronica, la diagnosi è sempre difficile.
Diagnostica
L’AKI viene diagnosticato se si osserva almeno uno dei seguenti tre fattori:
- un aumento del livello di creatinina nel sangue di oltre 26 µmol/l in 48 ore;
- un aumento della concentrazione di creatinina nel sangue di 1,5 volte rispetto a quello iniziale, osservato o supposto una settimana fa;
- la produzione di urina non supera 0,5 ml/kg/ora per 6 ore.
Quando si diagnosticano i bambini, vengono presi in considerazione il livello di creatinina nel sangue, la diuresi per 8 o 12 ore e la velocità di filtrazione glomerulare, con una diminuzione del 25%.
A seconda della concentrazione di creatinina e della quantità di diuresi, viene specificata la gravità. Tuttavia, sia l'osservazione che l'ulteriore trattamento dovrebbero essere effettuati nell'ambito di un monitoraggio costante dei livelli di creatinina, potassio, sodio e così via.
Primario
 I primi esami eseguiti durante l’esame sono gli esami del sangue:
I primi esami eseguiti durante l’esame sono gli esami del sangue:
- esame del sangue biochimico - determinato dal livello di creatinina, urea, potassio, sodio, frazioni proteiche, bilirubina totale e diretta e così via;
- coagulogramma;
- stato acido-base del sangue;
- gasometria del sangue arterioso;
- analisi generale delle urine: vengono determinati la densità delle urine, la proteinuria, i componenti patologici: cilindri granulari, cilindri eritrocitari, globuli rossi;
- ulteriori studi se è necessario un chiarimento della diagnosi.
È necessario prelevare campioni di urina e sangue per i test prima di somministrare diuretici e liquidi, altrimenti i dati del test verranno distorti.
I pazienti con diagnosi di AKI o quelli a rischio, ad esempio dopo un intervento cardiaco, dovrebbero essere costantemente monitorati.
Il monitoraggio include:
- controllo della diuresi, preferibile ogni ora che ogni giorno;
- il volume di fluido consumato e somministrato - la prima misura preventiva è il ripristino del normale equilibrio idrico, pertanto il volume di fluido introdotto e rimosso deve essere rigorosamente preso in considerazione;
- peso corporeo – misurato a stomaco vuoto due volte al giorno;
- osservazione delle feci;
- pulsossimetria;
Tra i metodi strumentali, viene prescritta l'ecografia: i reni sono solitamente ingranditi nell'AKI, così come la radiografia del torace per rilevare la congestione, il flusso sanguigno e altro.
Diagnosi differenziale
 È importante determinare esattamente in quale categoria rientra la malattia, poiché in caso di AKI prerenale, la funzione renale si riprende non appena viene ripristinato il normale apporto di sangue. Per questo viene utilizzata la diagnosi differenziale. L’AKI prerenale è caratterizzato da:
È importante determinare esattamente in quale categoria rientra la malattia, poiché in caso di AKI prerenale, la funzione renale si riprende non appena viene ripristinato il normale apporto di sangue. Per questo viene utilizzata la diagnosi differenziale. L’AKI prerenale è caratterizzato da:
- diuresi – meno di 400 ml al giorno;
- osmolalità delle urine – più di 500 mOsm/kg;
- densità – più di 1.023 g/ml;
- il rapporto tra urea plasmatica e creatinina plasmatica è superiore a 20;
- il rapporto tra la creatinina nelle urine e la creatinina nel sangue è superiore a 40;
- il rapporto tra l'urea nelle urine e l'urea nel plasma è superiore a 20;
- la concentrazione di sodio nelle urine è inferiore a 20 mmol/l;
- sedimento urinario – nessuna patologia osservata.
L’AKI renale è caratterizzato da:
- diuresi - può variare, non ci sono segni esatti;
- osmolalità delle urine – inferiore a 400 mOsm/kg;
- densità – inferiore a 1,012 g/ml;
- il rapporto tra urea plasmatica e creatinina plasmatica è inferiore a 20;
- il rapporto tra creatinina nelle urine e creatinina nel sangue è inferiore a 40;
- il rapporto tra l'urea nelle urine e l'urea nel plasma è inferiore a 20;
- la concentrazione di sodio nelle urine è superiore a 40 mmol/l;
- sedimento urinario – si osservano cellule epiteliali, ialine, cilindri epiteliali.
Se il paziente ha avuto una malattia renale, in particolare un'insufficienza renale cronica, tutti i criteri sopra indicati non saranno più caratteristici.
La diagnosi di AKI postrenale è alquanto più semplice. La diagnosi è confermata dalla congestione dei reni, della vescica e degli ureteri, che viene determinata con precisione mediante ecografia.
Trattamento
L’obiettivo del trattamento dei pazienti affetti da AKI è multitasking:
- eliminazione dei disturbi metabolici e volumetrici;
- conservazione o ripristino della funzione renale;
- prevenzione dello sviluppo di insufficienza renale cronica.
Le tattiche terapeutiche sono determinate dalla forma della malattia, ma implicano in ogni caso la completa abolizione di qualsiasi farmaco nefrotossico: diuretici risparmiatori di potassio, antibiotici nefrotossici, analgesici non steroidei, ecc.
AKI prerenale
La causa della malattia sono i disturbi nell'afflusso di sangue, quindi l'obiettivo principale della terapia qui è ripristinare il normale afflusso di sangue all'organo. Per fare ciò, è necessario introdurre nel corpo una quantità sufficiente di liquido per ricostituire il volume di sangue perso. A questo scopo vengono utilizzati diversi metodi di terapia sostitutiva.
Il fluido viene somministrato attraverso una flebo. La sua composizione è determinata dalla composizione del liquido escreto. Pertanto, in caso di ipervolemia sullo sfondo di emodinamica instabile, viene somministrata una soluzione con globuli rossi. Se l'emodinamica è stabile, è sufficiente la soluzione salina ordinaria. Il livello di creatinina e urea nel sangue e nelle urine del paziente viene monitorato almeno 1 volta a settimana. In base a questi dati cambia la composizione delle soluzioni.
Le soluzioni colloidali vengono utilizzate con grande cautela poiché possono agire come farmaci nefrotossici. Le soluzioni cristalloidi sono un’opzione più sicura.
L'emodialisi viene prescritta 1 volta al giorno o ogni 2 giorni se non ci sono effetti o in casi di emergenza.Si eseguono emofiltrazione ed emodiafiltrazione. Questi ultimi vengono utilizzati meno frequentemente, poiché impiegano dalle 12 alle 36 ore.
La base del trattamento è la terapia conservativa. Ma nei casi acuti viene prescritta l'emodialisi d'urgenza. Le indicazioni per la procedura sono:
- conferma di laboratorio della disfunzione renale – velocità di filtrazione glomerulare inferiore a 20–25 ml/min;
- disturbi nella concentrazione di sodio nel sangue - inferiore a 115 o superiore a 165 mmol/l;
- il contenuto di urea nel sangue è superiore a 25–36 mmol/l;
- pericardite – tamponamento o alto rischio di sanguinamento;
- iperkaliemia dovuta all'inefficacia dei farmaci;
- acidosi metabolica dovuta a oliguria;
- progressivo sovraccarico di liquidi.
La componente principale del trattamento dell’AKI prerenale è il trattamento della malattia di base. Questo è rilevante sia per i bambini che per gli adulti. I farmaci vengono prescritti tenendo conto di questa malattia, quindi non ci sono raccomandazioni generali su questo argomento. I farmaci vengono somministrati tenendo conto dei livelli di potassio, calcio, sodio, fosfato, ecc., al fine di ripristinare e mantenere l'equilibrio elettrolitico.
Quindi, per l'iperkaliemia, glucosio e insulina vengono somministrati nel rapporto richiesto, cloruro di calcio per via endovenosa, bicarbonato di sodio per acidosi scompensata e così via. Se si verifica una brusca diminuzione dei livelli di potassio - inferiori a 7 mmol/l, la furosemide viene somministrata in assenza di ipovolemia o ostruzione renale. Per l'iperidratazione e l'edema polmonare viene somministrata anche la furosemide.
AKI renale
 Attualmente non esiste una terapia efficace per l’AKI renale. Le raccomandazioni generali sono simili a quelle utilizzate nel trattamento della forma prerenale: mantenimento dell'equilibrio elettrolitico, ripristino del volume dei liquidi in caso di ipovolemia, sospensione dei farmaci nefrotossici.
Attualmente non esiste una terapia efficace per l’AKI renale. Le raccomandazioni generali sono simili a quelle utilizzate nel trattamento della forma prerenale: mantenimento dell'equilibrio elettrolitico, ripristino del volume dei liquidi in caso di ipovolemia, sospensione dei farmaci nefrotossici.
Numerosi farmaci vengono utilizzati per ripristinare la funzione renale.
Tuttavia, l'effetto non è così significativo come previsto, soprattutto nella necrosi tubulare acuta di origine ischemica o nefrotica:
- L'obiettivo principale della maggior parte dei metodi rimane il trasferimento del paziente dallo stadio di oliguria a quello di non oliguria, poiché ciò riduce la mortalità. A questo scopo, la furosemide, un diuretico dell'ansa, viene prescritta in dosi non superiori a 600 mg/die. Allo stesso tempo, le dosi basse sono inefficaci. Di norma, la furosemide viene somministrata per via endovenosa, molto lentamente. Come dimostra la ricerca moderna, il diuretico non ha un effetto terapeutico, ma ripristina solo la diuresi.
- La dopamina è stata utilizzata piuttosto attivamente, ma per i pazienti gravemente malati è potenzialmente tossica e causa tachicardia e ischemia miocardica.
- Peptide natriuretico atriale: aumenta la velocità di filtrazione glomerulare, rallenta il riassorbimento del sodio. Tuttavia, il suo analogo sintetico non ha tale effetto.
- La terapia dialitica non influisce sulla durata della malattia e sulla velocità del recupero. Oggi la dialisi è un mezzo per mantenere e ripristinare l’equilibrio elettrolitico.
- Nel trattamento, la terapia di supporto è di grande importanza, cioè le restrizioni dietetiche che impediscono l'assunzione di determinate sostanze e l'introduzione artificiale delle sostanze mancanti.
Nessuno degli approcci moderni fornisce un effetto benefico sostenibile.
AKI postrenale
L'obiettivo del trattamento in questo caso è eliminare il più rapidamente possibile i disturbi del deflusso delle urine per ridurre al minimo i danni ai reni.
I metodi dipendono dal livello di ostruzione:
- Se il deflusso è compromesso a livello del collo vescicale o dell'uretra è sufficiente l'installazione di un catetere transuretrale.
- Se il livello di violazioni è più elevato, è necessaria la nefrostomia: l'introduzione di un sistema di drenaggio artificiale nel rene.
Di norma, queste misure prevengono danni al rene e portano al completo ripristino della sua funzione.
Trattamento dei bambini
Il trattamento dell’AKI nei bambini piccoli non differisce significativamente dai metodi terapeutici utilizzati per gli adulti.
La prima priorità è supportare e ricostituire il volume intravascolare. Un programma di infusione è il metodo più sicuro e affidabile e, in molti casi, consente di anticipare la transizione dall’AKI prerenale alla necrosi tubulare.
Inizialmente si somministrano fino a 400 ml/mq. M. a temperatura normale, o più con febbre. Quindi il volume di rifornimento viene calcolato in base alle condizioni del bambino e agli esami del sangue e delle urine.
Per i pazienti con diminuzione acuta del volume sanguigno, ciò potrebbe non essere sufficiente:
- L'uso di diuretici per il trattamento non è considerato efficace oggi. Tuttavia, i farmaci vengono utilizzati e prescritti quando necessario per mantenere o ripristinare la diuresi.
- In caso di deficit oligo/anurico o ATN, non è raccomandato prescrivere integratori di potassio o sodio a meno che i pazienti non presentino ipokaliemia o ipofosfatemia. Con la poliuria è necessario il rifornimento di sostanze.
- L'iperkaliemia richiede un trattamento urgente: l'introduzione di gluconato di calcio, bicarbonato di sodio, l'uso di assorbenti e così via.
- Se i metodi terapeutici non sono validi, il corso include l'emodialisi e la dialisi peritoneale.
L’AKI è considerato un fattore che aumenta la mortalità, a parità di altre condizioni. Le forme prerenale e postrenale hanno una prognosi relativamente favorevole, poiché in questi casi si può prevenire il danno al tessuto renale. L’AKI renale ha un tasso di mortalità del 50-70%. Nei pazienti anziani con insufficienza cardiaca o respiratoria, la mortalità raggiunge l'80%.
I pazienti sopravvissuti richiedono osservazione e recupero a lungo termine. Più del 50% sviluppa insufficienza renale cronica. Circa il 5% dei pazienti necessita di dialisi costante. Statistiche di questo tipo sono incomplete e distorte da diagnosi errate e dalla mancanza di attrezzature moderne.
Le statistiche sono migliori per i bambini. Il tasso medio di sopravvivenza è del 79,9%, di cui il recupero completo può essere raggiunto nel 58%. Il 39% dei pazienti sviluppa insufficienza renale cronica.
La prognosi della malattia nei neonati è sfavorevole. Senza dialisi, la mortalità in questo gruppo è dell’80%.
Il danno renale acuto è una malattia grave ma potenzialmente reversibile. Di norma, la malattia accompagna la malattia di base e rende il trattamento molto difficile. Video conferenza sul danno renale acuto:
gidmed.com